שאלון מערכת: שיעורי בית שיטות מחקר 1
שיטות מחקר 1 שאלה 1
מה מהבאים אינו נכון לגבי שיטת האלקטרופורזה (Electrophoresis)?
במה השאלה עוסקת: Electrophoresis.
תשובה ד’. שיטת האלקטרופורזה (Electrophoresis) היא שיטה לאנליזה של חלבונים וחומצות גרעין אשר מבצעת הפרדה לפי גודל. בשיטה זו המולקולות נטענות לתוך הג’ל שנמצא בתמיסה שמוליכה חשמל אשר מועבר בה זרם חשמלי שגורם למשיכת המולקולות לעבר הקטודה שנמצאת בקצה הג’ל. מכיוון שצפיפות הג’ל מונעת או מקשה מעבר של המולקולות, המולקולות הקטנות יותר מבחינת גודל ינועו מהר יותר ולכן ימצאו קרוב יותר לקצה הקטודה (לקצה התחתון של הג’ל), וכך להיפך – מולקולות גדולות יטו להימצא בחלק העליון יותר של הג’ל.
שלילת מסיחים:
א’. בשיטה זו ניתן להפריד ולהבדיל בין גדילי DNA שונים וכן גם בין גדילי RNA שונים. לרוב, בעת הפרדת מקטעים ארוכים (שעולים על 500 נוקלאוטידים) נהוג להשתמש בג’ל אגרוז, ובמקטעים קצרים יותר נהוג לשתמש בג’ל פוליאקרילאמיד (Polyacrylamide) שהוא בעל רזולוציה טובה יותר למקטעים קצרים.
ב’. מכיוון שהחלבונים הם מולקולות מאוד מורכבות שקיימות במגוון רחב מאוד של צורות ומבנים, נהוג לבצע להם דהנטורציה בעזרת חומר שנקרא Sodium dodecyl sulfate (בקיצור SDS) אשר משמש כדטרגנט שפותח את החלבון ומטעין אותו במטען שלילי (מה שמקל על תנועתו בתוך הג’ל – מעלה את יכולת ההפרדה של השיטה). כאשר עושים שימוש גם ב-SDS השיטה תיקרא SDS-PAGE.
ג’. כפי שנאמר מעל, זו שיטת הפרדה הן לחלבונים והן למולקולות של חומצות גרעין. ולכן גם מסיח זה נכון.
להרחבה- Alberts, מהדורה 7, עמ’ 487-489 (Electrophoresis).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – ג׳ל אלקטרופורזה
אלברטס, פרק 8
שיטות מחקר 1 שאלה 2
נתבונן על כרומוזומים של תאים שידוע שעברו אברציות כרומוזומליות (תאים אברנטיים כרומוזומליים), תוך שימוש בשיטת .Fluoresence in situ hybridization (FISH) נשתמש בסמנים לצנטרומר של כרומוזום 18 (ירוק) ול) PARK2 -אדום) לצורך היברידיזציה פלואורסצנטית. במידה והתרחשה מוטציית מחיקה (deletion mutation) בגן ל PARK2 – מה נצפה לראות?
במה השאלה עוסקת: FISH.
תשובה ד’. שיטת Fluorescence in situ hybridization (בקיצור FISH) היא שיטה לזיהוי ואיתור רצפים ספציפיים מאוד. בשיטה זו יוצרים DNA probe אשר מהווה כרצף משלים (Complementary sequence) בצורת חד-גדיל לרצף המטרה (שאותו רוצים לאתר) ואליו מחברים מולקולה פלאורסנטית אשר זוהרת במידה ויש זיווגי בסיסים בין ה-probe לרצף המטרה. חשוב לציין שעל מנת שה-probe יתחבר לרצף המטרה מבצעים דה-נטורציה (denaturation) ל-DNA על מנת שה-probe יוכל להתחבר. מכיוון שהתרחשה מוטציית מחיקה מהגן PARK2 ה-probe הספציפי שלו לא יוכל להתחבר אליו ולכן באותו הכרומוזום לא נראה את הזהירה צבע האדום. אך כן נראה זהירה אדומה בכרומוזום ההומולוגי שלו ולכן נראה פעמיים סיגנל ירוק (2 צנטרומרים של 2 כרומוזומי 18) וסיגנל אחד בלבד של הגן PARK2 התקין.
שלילת מסיחים:
א’. כפי שהוסבר מעל, תתרחש היברידציה (Hybridization) אחת ב-probe של הגן PARK2 ולכן לא יהיו 2 סמנים אדומים.
ב’. גם אם לא בטוחים לגבי הצנטרומר וה-Probe שלו (ואין סיבה שלא להיות בטוחים כי הצנטרומר הוא גם רצף ייחודי שניתן לחבר אליו פרוב ספציפי), לא נראה 2 סמנים אדומים ב-FISH עקב מוטציית המחיקה.
ג’. ניסיון לבלבל. אין ערבוב של צבעים ויצירת צבעים חדשים ב-FISH.
להרחבה- Alberts, מהדורה 7, ע”מ 505-506 (FISH).
נושא – שיטות מחקר, תת-נושא – הקדמה לשיטות מחקר, תת-תת נושא – מבוא ועקרונות עליהן מתבססות שיטות רבות
אלברטס, פרק 8
שיטות מחקר 1 שאלה 3
רצף DNA עבר ליגציה לתוך גדיל DNA מעגלי. גדיל ה DNA- הוחדר על ידי אמצעים כימיקלים לחיידק. בעקבות הליגציה מאות עותקים של המולקולה נוצרו בחיידק. התיאור הטוב ביותר לרצף ה- DNA שהוחדר הינו:
במה השאלה עוסקת: שיבוט של DNA דרך פלסמידים
תשובה ד’. נקודת תחילת השכפול הבקטריאלית (Origin of replication, ORI) דרושה בכדי שהחיידק יתחיל לשכפל את ה-DNA שלו. ואכן בשאלה זו ניתן לראות שלאחר החדרת המקטע, המולקולה המעגלית עברה תהליך של הכפלה בתוך תא החיידק. כפי שיוסבר במסיח ב’, פלסמידים מכילים את נקודה זו, אולם בשאלה זו נתון רצף DNA מעגלי שהוא למעשה פשוט יותר מפלסמיד (שכאמור מכיל כבר את הרצפים הדרושים לצורך שכפול).
שלילת מסיחים:
א. ה-Initiator הוא חלבון הנחוץ לצורך תחילת השכפול ותפקידו הוא להפריד בין שני גדילים ה-DNA באמצעות פירוק קשרי המימן בין הבסיסים. אולם בשאלה נתון שהוחדר רצף DNA ולא חלבון, וכמו כן, תא החיידק כבר מכיל חלבונים אלו.
ב. פלסמידים הינם מולקולות DNA מעגליות הנמצאות באופן טבעי בחיידקים ולעיתים גם באאוקריוטים מסוימים ומשמשים רבות לצורכי מחקר. הפלסמידים הינם בעלי יכולת שכפול עצמית וישנם סוגים שונים של פלסמידים בגדלים שונים. לפלסמידים מספר רצפים בסיסיים כגון ORI, אתר polylinker, שמאפשר חיתוך באמצעות אנזימי רסטריקציה והחדרת מקטעים שונים, וכן רצף המכיל עמידות כנגד אנטיביוטיקה.
ג. פרומוטר הוא מקטע ב-DNA החיידקי שחשוב לצורך תחילת שעתוק ויצירת RNA. שימו לב ש-ORI הוא מקטע ממנו ה-DNA משתכפל למולקולת DNA נוספת, בעוד הפרומטר תורם ליצירת מולקולת RNA. הבדל נוסף הוא ש-ORI הוא האזור עצמו שממנו מתחיל השכפול בעוד הפרומוטר נמצא לרוב במעלה הזרם לאזור תחילת השעתוק.
להרחבה – Alberts, מהדורה 7, עמ’ 272-274 (Replication initiation); 501-503 (Gene cloning).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שיבוט דנ״א
אלברטס, פרק 8
שיטות מחקר 1 שאלה 4
מה מהבאים נכון לגבי החלבון GFP?
במה השאלה עוסקת: GFP.
תשובה ב’. החלבון הפלאורסנטי Green fluorescent protein (בקיצור GFP), הוא חלבון אשר יכול לשמש כגן מדווח (Reporter gene) – כאשר מכניסים את הגן צמוד לפרומוטור מסוים או כסמן למיקומו של חלבון מסוים בתא כאשר מחדירים את הגן שלו לחלבון המטרה.
שלילת מסיחים:
א. ה-GFP אכן חלבון שמקודד מגן יחיד אך הוא דורש מודיפיקציות שונות על מנת להיות פעיל.
ג. חלבון זה מקבל אור כחול ובתגובה פולט אור ירוק.
ד. לא נכון. כפי שנאמר מעל, אחד היתרונות החשובים שלו בתחום המחקר זה עצם היכולת להחדירו לתאים חיים.
להרחבה – Alberts, מהדורה 7, עמ’ 573-575 (GFP).
נושא – שיטות מחקר, תת-נושא – הקדמה לשיטות מחקר, תת-תת נושא – מבוא ועקרונות עליהן מתבססות שיטות רבות
אלברטס, פרק 8
שיטות מחקר 1 שאלה 5
מתי נשתמש בשיטת ה-In situ hybridization?
במה השאלה עוסקת: In situ hybridization.
תשובה ד’. שיטת ה-In situ hybridization משמשת לחקר RNA בתא. היא נשענת על היברידציה של פרובים (Probs) מסומנים שיתחברו לרצפי המטרה. לכן, ניתן לחקור בעזרתה ביטוי גנים ברקמות שונות.
שלילת מסיחים:
א’. כפי שנאמר, זו איננה שיטת ריצוף.
ב’. אחד החסרונות בשיטה זו הוא הצורף בקיבוע (פיקסציה) ולכן לא ניתן לעבוד איתה בתאים חיים.
ג’. שיטה זו אינה מתאימה להחדרת גנים וליצירת יצורים טרנסגנים.
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – חקר תפקוד וביטוי הגנים
אלברטס, פרק 8
שיטות מחקר 1 שאלה 6
מה מהבאים אינו נכון לגבי תהליך ה? PCR –
במה השאלה עוסקת: PCR.
תשובה ב’. סעיף זה נכון כיון שנשאלתם מה לא נכוןבנוגע ל-PCR ואכן הסעיף מציג טענה שאינה נכונה. שיטת ה-PCR (polymerasechain reaction) מאפשרת שכפול (=הגברה) של מקטעי DNA ספציפיים ללא צורך בשימוש בחיידקים. בשיטה זו משתמשים בגדילי ה-DNA שאותם נרצה להגביר, זוג פריימרים ספציפיים,פולימרז עמיד לחום וכן כל מה שנחוץ לפולימרז לעבוד כגון נוקלאוטידים, בופר, מגנזיום (כקופקטור) וכו’. בשיטה זו משתמשים רק בזוג פריימרים, כאשר מיקום הפריימרים קובע את הגבולות של המקטע אותו נשכפל. נקודה זו נכונה כיון שה-DNA פולימרז יכול רק להמשיך לסנתז את הפריימר לכיוון אחד ולכן כל רצף שנמצא לפני הפריימר אינו נכלל בהגברה (בסוף הפתרון מצורפתתמונה המתארת נקודה זו). לסיכום, כיון שיש לנו רק זוג פריימרים אחד, המקטע אותואנו מגבירים הוא מאוד ספציפי ולא מדובר בנקודות שונות לאורך הגנום.
שלילת מסיחים:
א’. שיבוט הוא תהליך שבו נוצרים העתקים של חומר ודוגמה לתהליך כזה בהקשר של DNA היא הגברה באמצעות החדרת פלסמיד לחיידקים שישכפלו את אותו פלסמיד או שיטת PCR. כלומר בשיטת PCR מבצע שיבוט וגם את התוצרים שלו ניתן להמשיך ולשבט במידה ויש בכך צורך במעבדה.
ג’. לאחר שמולקולת DNA דו-גדילית נוצרה במהלך התהליך, הגדילים צריכים להתנתק אחד מהשני באמצעות דנטורציה בחום בכדי שהגברה נוספת של המקטע תוכל להתרחש. להלן רצף התהליכים בהגברת מקטע באמצעות PCR:
1. דנטורציה – מחממים את הדגימה לכ-90⁰C כך גדילי ה-DNA יפרדו. יש צורך בהפרדת הגדילים הקומפלימנטרים בכדי שה-DNA החד גדילים יוכלו לשמש לנו כתבנית לשכפול, והפולימרז יוכל לעבוד ולסנתז על גביו עותקים נוספים.
2. היברידיזציה/annealing – מקררים מעט את הדגימה לטמפרטורה שתאפשר לפריימרים להתחבר לרצף. פריימרים אלה הם רצפי DNA קצרים אשר תוכננו מראש במעבדה והוזמנו מחברה חיצונית.
3. סינטתזה/elongation – ה-DNA פולימרז מאריך את הפריימרים על גבי התבנית וכך מסנתז את כל המקטע.
ד’. הפריימרים הינם אוליגונוקלאוטידים וכפי שטענו הם אלו שקובעים את גבולות המקטע שיוגבר. מצורף איור שיכול לעזור להמחיש זאת.
להרחבה – Alberts, מהדורה 7, עמ’ 506-510 (PCR).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שכפול דנ״א בעזרת PCR
אלברטס, פרק 8
שיטות מחקר 1 שאלה 7
מתי נעדיף להשתמש ב-PFGE ולא ב-Gel electrophoresis? ואיך?
במה השאלה עוסקת: PFGE.
תשובה א’. בשיטת Pulsed-field gel Electrophoresis (בקיצור PFGE) נעשה שימוש באלקטרופורזה שבה משתנים כיווני הזרמים החשמליים באופן תדיר וקבוע על מנת לגרום לתזוזות הגדילים (לרוב כרומוזומים שלמים) על פני הג’ל. כאשר נריץ גדילים ארוכים באלטרופורזה הרגילה נראה “מריחה” של ה-band מכיוון שקצוות הגדילים נעות מהר יותר בתגובה לשדה החשמלי לעומת מרכז הגדיל. ולכן נעדיף להשתמש ב-PFGE בגדילים ארוכים.
שלילת מסיחים:
ב’. אם נגביר את עוצמת השדה החשמלי זה רק יגרום ל”מריחת” הבנדים בצורה מהירה יותר, ולכן מסיח זה אינו נכון.
ג’. כפי שנאמר, שיטה זו נועדה לשפר את ההתמודדות עם גדילים מאוד גדולים וארוכים.
ד’. כנ”ל.
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – ג׳ל אלטרופורזה
אלברטס, פרק 8
שיטות מחקר 1 שאלה 8
מה נכון מהבאים לגבי שיטת ה-Nanopore?
במה השאלה עוסקת: Nanopore
מולקולת DNA חד-גדילית עוברת דרך נקבובית חלבונית זעירה בממברנה.
מתח חשמלי מופעל על פני הממברנה, מה שיוצר זרם דרך הנקבובית.
המעבר של נוקלאוטידים דרך הנקבובית יוצר שינויים קטנים בזרם החשמלי על פני הממברנה.
לכל בסיס נוקלאוטידי צורה ייחודית שמשפיעה בצורה שונה על הזרם.
מדידת השינויים הקטנים הללו בזרם מאפשרת זיהוי של כל נוקלאוטיד כשהוא עובר דרך הנקבובית.
שלילת מסיחים:
א’. השיטה שבה מגבירים ושוברים מקטעים של גנומים שלמים ומרצפים אותם בעזרת אזורי החפיפה ביניהם נקראת Shotgun sequencing (ולא נמצאת בסילבוס החדש)
ב’. השימוש ב-ddNTP הוא בשיטת הריצוף סנגר (Sanger).
ד’. בשיטת ה-Illumina נעזרים בבסיסים שמחוברים למולקולות פלואורסנטיות, ולכן מסיח זה איננו נכון גם כן.
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שיטות לריצוף דנ״א
אלברטס, פרק 8
שיטות מחקר 1 שאלה 9
מה מהבאים נכון לגבי המושג פולימורפיזם (Polymorphism)?
במה השאלה עוסקת: Polymorphism.
תשובה א’. פולימורפיזם (Polymorphism) הוא מושג שמתאר את התופעה שבה אללים רבים באותו גן יבוטאו בפנוטיפים שונים בתוך אוכ’. ישנם סוגים רבים של פולימורפיזם, צריך להכיר את SNP ו-CNV. ה-SNP הוא הכי נפוץ ולכן תשובה זו היא הנכונה.
שלילת מסיחים:
ב’. רוב הפולימורפיזם הם דווקא לא מזיקים (אינם גורמים למחלות) ולכן מסיח זה אינו נכון.
ג’. כפי שנאמר מעל, זו אינה ההגדרה של פולימורפיזם.
ד’. המושג מתאר שינוי נקודתי (SNP) או שינוי קצת יותר רחב (כמו ב-CNV) שגורם לשינוי בפנוטיפ. זה אינו מעיד שבאוכ’ אחרות לא יהיה אותו, ולכן מסיח זה גם איננו נכון.
להרחבה- Alberts, מהדורה 7, עמ’ 525-527 (Polymorphism).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – פולימורפיזם ומחקר גנטי בבני אדם
אלברטס, פרק 8
שיטות מחקר 1 שאלה 10
מה מהבאים נכון לגבי שיטת Cre\LoxP?
במה השאלה עוסקת: Cre\LoxP.
תשובה ד’. שיטת Cre\LoxP (שהתגלתה לראשונה בבקטריופאג’ P1) היא שיטה חשובה בהנדסה גנטית שבה ניתן לבצע שינויים בגן מסוים כגון מחיקות, הכנסות, היפוכים וכדומה. בשיטה זו, יש אנזים מיוחד מסוג רקומבינאז (Recombinase) שנקרא Cre, אשר מסוגל לחתוך רצפי LoxP. ולכן רק כאשר שני אלו נמצאים יחדיו ניתן לבצע מניפולציות שונות על גנים.
שלילת מסיחים:
א’. כפי שנאמר מעל, ה-LoxP הוא הרצף/האתר שבו חותך האנזים Cre. חשוב לזכור כי האנזים חייב 2 אתרי LoxP (בשני צדדי גן המטרה) על מנת שיוכל לחתוך אותו כראוי.
ב’. Cre הוא האנזים בעצם. אומנם בשיטה זו כן מכניסים את הגן שלו יחד עם הפרומוטר שלו, אך הוא ללא ספק אינו מהווה כפרומוטר ל-LoxP שכן האחרון אינו רצף שבא לידי ביטוי אלא משמש כאתר מטרה לאנזים Cre בלבד.
ג’. בדיוק להיפך.
להרחבה-Alberts, מהדורה 7, עמ’ 317-320(Cre-LoxP).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – חקר תפקיד וביטוי הגנים
אלברטס, פרק 8
שיטות מחקר 1 שאלה 11
______ היא שיטה להגברת רצפים שבה ניתן למדוד את כמות השעתוק ברגע נתון בתא.
במה השאלה עוסקת: Quantitative RT-PCR.
תשובה ג’. שיטת ה-Quantitative RT-PCR היא בעצם שיטת PCR שבה משתמשים באנזים רוורס טרנסקריפטאז (כלומר רצף המטרה שלנו יהיה RNA) שבה מוסיפים סמנים פלואורסנטים על מנת לאמוד את כמות התוצרים. כלומר, מפיקים את ה-mRNA המטרה מהתא הנבחר ומגבירים אותו בשיטת ה-PCR, כאשר הסמן הפלואורסנטי יעיד על כמות התוצרים – ככל שמפיקים יותר mRNA מהתא כך תהיה יותר זהירה כלומר יותר תוצרים.
שלילת מסיחים:
א’. זו בעצם שיטת ה-RT-PCR הרגילה ללא יכולת האמידה של כמות התוצרים שעברו שעתוק בתא.
ב’. זו שיטת ריצוף שבה מפרקים את הגנום למקטעים קצרים ומגבירים (בעזרת PCR רגיל). היא איננה מאפשרת לאמוד את רמת ה-RNA בתא מסוים.
ד’. שיטה בהנדסה גנטית להשתקת גנים.
להרחבה-Alberts, מהדורה 7, עמ’ 536 (Quantitative RT-PCR).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שכפול דנ״א בעזרת PCR
אלברטס, פרק 8
שיטות מחקר 1 שאלה 12
התפקיד הביולוגי של אנזימי רסטריקציה הוא:
במה השאלה עוסקת: אנזימי רסטריקציה.
תשובה ב’. אנזימי רסטריקציה (Restriction enzymes) הם אנדונוקלאזות (Endonucleases), כלומר אנזימים החותכים באמצע רצף הדנ”א-רצף ספציפי. הם מזהים רצפי פלינדרום (Palindrome)- רצפים בהם אנו קוראים קוד בגדיל ה-Sense מ-5′ ל-3′ אשר זהה לקוד שאנו קוראים מ-5′ ל-3′ בגדיל ה-Anti-sense. אורך הרצפים הם בין 4-8 נוקלאוטידים (ראו תמונה).
מנגנון זה הוא מנגנון הגנה טבעי של חיידקים- האנזימים חותכים דנ”א זר שנכנס לחיידק. על מנת להימנע מחיתוך עצמי, הרצפים עוברים מתילציה שמגינה עליהם. הקצוות הדביקים, אלו הקצוות שנשארים לאחר החיתוך-לרוב קצה 3′ יהיה קצר יותר מקצה 5′ ונקראים כך כיוון שהם יכולים לחזור להתחבר.
סוג חיתוך נוסף שמשאירים חלק מהאנזימי רסטריקציה זה חיתוך עם קצוות קהים – ראו תמונה.
שלילת מסיחים:
א’. כן משתמשים באנזימי רסטיקציה כדי לבנות פלסמיד רקומביננטי, אך אין זה תפקידם הביולוגי.
ג’. אין קשר בין אנזימי רסטריקציה לבין עמידות לאנטיביוטיקה.
ד’. נזקי UV גורמים למוטציות בחיידקים ומערכת האנזימי רסטריקציה אינה אחראית כדי לתקנם.
להרחבה-Alberts, מהדורה 7, עמ’ 498-499 (Restriction enzymes).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – עבודה עם אנזימי רסטריקציה
אלברטס, פרק 8
שיטות מחקר 1 שאלה 13
ישנם אנזימי רסטריקציה היוצרים קצוות דביקים .(sticky ends) זה אומר שהם:
במה השאלה עוסקת: אנזימי רסטריקציה.
תשובה ג’. אנזימי רסטריקציה (Restriction enzymes) הם אנדונוקלאזות (Endonucleases), כלומר אנזימים החותכים באמצע רצף הדנ”א-רצף ספציפי. הם מזהים רצפי פלינדרום (Palindrome)- רצפים בהם אנו קוראים קוד בגדיל ה-Sense מ-5′ ל-3′ אשר זהה לקוד שאנו קוראים מ-5′ ל-3′ בגדיל ה-Anti-sense. אורך הרצפים הם בין 4-8 נוקלאוטידים (ראו תמונה).
מנגנון זה הוא מנגנון הגנה טבעי של חיידקים- האנזימים חותכים דנ”א זר שנכנס לחיידק. על מנת להימנע מחיתוך עצמי, הרצפים עוברים מתילציה שמגינה עליהם. הקצוות הדביקים, אלו הקצוות שנשארים לאחר החיתוך-לרוב קצה 3′ יהיה קצר יותר מקצה5′ ונקראים כך כיוון שהם יכולים לחזור להתחבר.
סוג חיתוך נוסף שמשאירים חלק מהאנזימי רסטריקציה זה חיתוך עם קצוות קהים – ראו תמונה.
שלילת מסיחים:
א’. האנזים לא יכול לחתוך באותו בסיס כיוון שיש לו אתר ספציפי לחיתוך.
ב’. אין קשר לכמות ה-GC שיש בגדיל לבית תבנית חיתוך האנזים רסטריקציה.
ד’. לכל אנזים רסטריקציה יש את תבנית החיתוך המיוחדת שלו.
להרחבה- Alberts, מהדורה 7, עמ’ 498-499 (Restriction enzymes).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – עבודה עם אנזימי רסטרקציה
אלברטס, פרק 8
שיטות מחקר 1 שאלה 14
חוקרים ניסו לשבט גן לאנטרוטוקסין חדש שהתגלה שנקרא “pupicktoxin” מהגנום של חיידק פתגוני מאוד.”salmonella typhii” על מנת לשבט את הרצף המבוקש החוקרים הגבירו את הגן באמצעות .PCR שני הפריימרים (FOR-pu, REV-pu) שהשתמשו בהם להגברה של גן ה”pupicktoxin” – (תמונה (aשהיו מבוססים על רצף גנומי של כרומוזום חיידקי, הכילו אתרי חיתוך ל- BamHI על קצה 5′ של הפריימר. החוקרים יצרו פלסמיד שמכיל מרקר סלקציה לעמידות לפניצילין ואתר חיתוך בודד ל BamHI- הממוקם בדיוק ליד הפרומוטור החיידקי. החוקר חתך את הפלסמיד ואת התוצר המוגבר עם אנזים הרסטריקציה ,BamHI ניטרל את האנזים, ביצע ליגציה ועשה טרנספורמציה ל- E- Coli קומפטנטים. לאחר לילה 6 מושבות הצליחו לגדול על מצע אגרוז LB עם אמפיצילין. למען אישור נוסף בוצעו שתי ריאקציות PCR על כל פלסמיד. ריאקציה אחת עם הפריימרים FOR-pu ו) REV-pu -תמונה (b- . הבנד השני משמאל הוא ביקורת חיובית שמכילאת הגן. הריאקציה השניה בוצעה עם הפריימר FOR-pu ועם הפריימר REV-pl הממוקם על גבי הפלסמיד (תמונה .( c
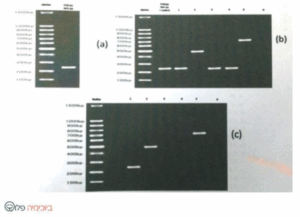
בוצע Northen blot על גנום של salmonella typhii ועל חיידק E-Coli מכל מושבה עם פרוב ל-RNA של “pupicktoxin” לאיזו מושבה יהיה בנד זהה באורך לבנד הביקורת מהחיידק salmonella typhii ?
במה השאלה עוסקת: Electrophoresis.
תשובה ג’. זו שאלה עם מלל מאוד ארוך ומבלבל, אך חשוב להישאר ממוקדים. מבקשים להסתכל על הג’ל שמסומל באות b. בג’ל זה ניתן לראות את סקאלת הביקורת שנמצאת בצד שמאל (רואים הרבה בנדים), ולצידה הבנד של ביקורת חיובית לגן ואחריה את כל המושבות. כפי שניתן לראות, המושבה הראשונה זהה לבנד של הביקורת החיובית לגן ולכן ניתן להסיק כי יש להם את אותו האורך (250 נוקלאוטידים).
שיטת ה-Northern blot איננה בחומר, אך לא צריך להכיר אותה על מנת להבין את השאלה ולהסיק את התשובה מכך. בכללי, שיטה זו היא המקבילה ל-Western blot אך בה ניתן להריץ RNA. כזכור ב-Western blot מריצים חלבונים בג’ל.
להרחבה- Alberts, מהדורה 7, עמ’ 499-500 (Electrophoresis).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – ג׳ל אלטרופורזה
אלברטס, פרק 8
שיטות מחקר 1 שאלה 15
משתמשים באנזימי רסטריקציה לבדיקות קליניות כאשר:
במה השאלה עוסקת: Restriction enzymes.
תשובה ב’. אנזימי הגבלה (Restriction enzymes) הם אנזימים מסוג אנדונוקלאזות אשר יודעות לזהות ולחתוך רצף ספציפי של נוקלאוטידים מהגנום. אנזימים אלו מסוגלים לחתוך ב-2 צורות עיקריות את הגנום, האחת נקראת Blunt ends שבה תוצרי החיתוך “ישרים”, והשנייה נקראת Sticky ends שבה החיתוך הוא “מדורג”, לעיתים נקרא “דביק” – במצב זה נראה חלק קצר שהוא בעצם חד-גדיל (לעומת ב-Blunt ends שבו אין חלק כזה). מבין אנזימי הרסטריקציה הנפוצים אפשר למצוא את HaeIII, EcoRI, HindIII ועוד. ישנם הרבה תפקידים לאנזימי הרסטריקציה הן בטבע והן במעבדה, למשל אחד השימושים הנפוצים שלהם במעבדה הוא להכנסה והוצאתו וקטורים מתוך גנומים, ואף כמרקר סלקציה שבו רואים האם הגנום קיבל את הווקטור שניסו להכניס אליו. אם תתרחש מוטציה אשר תגרום לשינוי אתר הזיהוי לאנזימי ההגבלה האנזים לא יעבוד ולא נראה את הווקטור בתמיסה ולכן האנזים משמש לבדיקה קלינית האם הכנסת הווקטור או הוצאתו הצליחה או לא, ולכן תשובה זו נכונה.
שלילת מסיחים:
א’. כפי שנאמר מעל, משתמשים באנזימי הרסטריקציה כדי להכניס או להוציא גנים/ווקטור מסוימים.
ג’. אין קשר למודיפיקציות שנמצאות באתרי החיתוך, כלומר לא משתמשים באנזימי ההגבלה כי יש מתיל באתר החיתוך. כמו כן, ישנם אנזימי הגבלה שיכולים להתחבר לאתר הזיהוי/חיתוך רק כאשר יש עליו מתיל.
ד’. כפי שנאמר מסיח א’, אנזימי ההגבלה חותכים רצפים ספציפיים ואינם מבדילים בין אקסון לאינטרון לרבות האם יש בו מוטציה כזו או אחרת, ולכן מסיח זה אינו נכון.
להרחבה- Alberts, מהדורה 7, ע”מ 498-499 (Restriction enzymes).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – עבודה עם אנזימי רסטרקציה
אלברטס, פרק 8
שיטות מחקר 1 שאלה 16
מהי מטרת השימוש ב-PCR בתחום הזיהוי הפורנזי?
במה השאלה עוסקת: PCR
תשובה ב׳. בזיהוי פורנזי, משתמשים ב-PCR כדי להגביר אזורים גנומיים שבהם יש STR — רצפים חוזרניים קצרים שמספר החזרות שלהם משתנה מאדם לאדם.
מכיוון שהפריימרים מתוכננים להיקשר מחוץ למקטע החזרתי, תוצרי ה-PCR יהיו באורכים שונים בהתאם למספר החזרות של כל אדם.
כך ניתן לבצע אנליזה על ג’ל (או בטכנולוגיות אחרות) ולהשוות בין תבניות אורכים שונות — מה שמאפשר לזהות אם דגימת ה-DNA מזירת האירוע תואמת לחשוד מסוים.
שלילת מסיחים:
א’. ה-PCR במקרה הזה לא נועד לרצף את כל הגנום, אלא רק להגביר אזורים קטנים ומוגדרים מאוד (STR).
ריצוף מלא של הגנום הוא תהליך אחר (כגון Whole Genome Sequencing) ואינו מתבצע בשגרה לצורכי פורנזיקה.
ג’. זיהוי Point Mutations נעשה בשיטות אחרות (כגון Allele-specific PCR או ריצוף), ולא במערכת זיהוי מבוססת STR.
מטרת ה-PCR כאן היא להבחין לפי אורך התוצר — לא לפי שינויים ברצף.
ד’. השוואת רמות ביטוי עוסקת ב-RNA, לא ב-DNA. לשם כך יש להשתמש ב-RT-PCR (Real-Time PCR או Reverse Transcription PCR).
במקרה שלנו אין שום קשר לרמות ביטוי — מדובר בזיהוי DNA גנומי קבוע.
להרחבה- Alberts, מהדורה 7, עמ’ 536-537 (Microarray) ועמוד 514-515 (Illumina sequencing).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שכפול דנ״א בעזרת PCR
אלברטס, פרק 8
שיטות מחקר 1 שאלה 17
מהו סדר הפעולות הנכון בשיטת ה-ChIP?
במה השאלה עוסקת: ChIP.
תשובה א’. שיטת ה-Chromatin Immunoprecipitation מאפשרת לחקור ביטוי גנים ואיתור הרצפים שאליהם נקשרים פקטורים שונים. תחילה מבצעים קשרים קוולנטים חזקים בין החלבונים לכרומטין בתא החי (in-vivo), לאחר מכן, מפרקים את התאים ושוברים את הדנ”א למקטעים קצרים (בסביבות ה-200 בסיסים). לבסוף מבודדים את המקטעים שאליהם קשורים חלבונים (ע”י שימוש בנוגדנים ספציפיים שיקשרו את פקטור השעתוק), מפרקים את קשרי הצילוב (Cross-link) ומנתקים את החלבון, כך שניתן יהיה לשלוח את מקטע המטרה לריצוף.
שלילת מסיחים:
ב’. נדרש לקבע (לבצע Cross-linking) בין החלבון לכרומטין לפני ביצוע חיתוך המקטעים מכיוון שאז נאבד את החלבון ולא נצליח לבודד את רצף המטרה שקושר אותו.
ג’. רוב המסי נכון, אך מטרת השיטה היא לאתר את רצף הקישור של פקטורי השעתוק ולא לרצף את הפקטור.
ד’. כנ”ל – מטרת השיטה אינה לרצף חלבונים.
להרחבה- Alberts, מהדורה 7, עמ’ 538 (ChIP).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – הנדסה גנטית וחיות טרנסגניות
אלברטס, פרק 8
שיטות מחקר 1 שאלה 18
מה מהבאים אינו נכון לגבי שיטת ה-CRISPR?
במה השאלה עוסקת: CRISPR.
תשובה ג’. מערכת ההגנה החיידקית CRISPR משמשת כיום בתחום ההנדסה הגנטית כשיטה לעריכת גנים. בשיטה זו משתמשים באנדונוקלאז Cas9 שמחזיק gRNA שתואם לרצף המטרה. את ה-Cas9 מבטאים בתאי גזע יחד עם ה-gRNA הרצוי ובמקביל לפעולתו מחדירים את הגן שרוצים לאתר החיתוך. לחילופין, ניתן פשוט להשתמש ב-Cas9 להפסקת פעילות הגן שנחתך ללא החדרת גן חדש. בנוסף, ניתן לחבר את אנזים הנ”ל לאקטיבטור או רפרסור (מה שיגרום לחיברו לגן המטרה) וע”י כך לשלוט בביטוי הגן – להפעילו או לעכבו. ולכן מסיח זה אינו נכון – זו התשובה שאותה נסמן.
שימו לב, ששיטת Tet off (שגם היא במקור מחיידקים) אכן משמשת להפעלה ודיכוי שעתוק גנים.
שלילת מסיחים:
א’. כפי שנאמר מעל, אכן ניתן לחבר את האנדונוקלאז Cas9 לרפרסור או אקטיבטור.
ב’. זו בדיוק צורת השימוש באנזים זה כאשר רוצים להמתמש במנגנון ה-CRISPR.
ד’. ה-Cas9 אכן משמש במקור כאנזים חיידקי שמגן מוירוסים בעלי גנום DNA. הוא עושה זאת ע”י פעילות של דנ”א אנדונוקאלז (מבקע את הגנום הויראלי).
להרחבה – Alberts, מהדורה 7, עמ’ 530-531 (CRISPR) ועמ’ 527-528 (Tet repressor).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא הנדסה גנטית וחיות טרנסגניות
אלברטס, פרק 8
שיטות מחקר 1 שאלה 19
באיזו שיטה מהבאות ניתן לחקור ביטוי גנים בשלב התרגום?
במה השאלה עוסקת: Ribosome profiling.
תשובה ד’. בשיטת ה-Ribosome profiling ניתן לחקור את ביטוי הגנים לפי מיקומו של הריבוזום על גדיל ה-mRNA, כלומר בשלב התרגום (Transcription). בשיטה זו, מבודדים את ה-mRNAs מהתא וחותכים אותם למקטעים קצרים ע”H נוקלאזות כך שרק המקטעים שעליהם נמצאים הריבוזום ישארו. לאחר מכן, מפרידים בין הגדיל לריבוזום ומכניסים ל-PCR.
שלילת מסיחים:
א’. סנגר היא שיטת ריצוף ולא שיטה לחקירת ביטוי גנים בשלב התרגום.
ב’. ה- Cre/LoxP היא שיטה בהנדסה גנטית שבה ניתן להשתיק גנים.
ג’. שיטת ה-Shotgun היא גם שיטת ריצוף גנים ולכן מסיח זה גם איננו נכון.
להרחבה – Alberts, מהדורה 7, עמ’ 538-540 (Ribosome profiling).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, שיטות למחקר ביטוי גנים ותרגום חלבונים
אלברטס, פרק 8
שיטות מחקר 1 שאלה 20
פלסמיד נחתך עם אנזימי רסטריקציה שונים, והתוצר רץ בג’ל אגרוז. התאם בין המספרים בבאריות לאנזים רסטריקציה בו השתמשו:
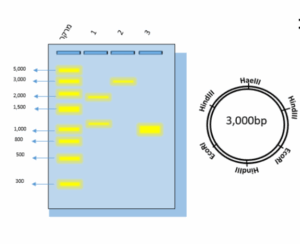
במה השאלה עוסקת: אנזימי רסטריקציה
תשובה ד’. הסבר: נתחיל לאסוף ניתונים :
גודל המקטע הינו 3000 בסיסים. הפלסמיד מכיל כמה אזרי חיתוך ע”י אנזימי רסטרקציה.
א. 3 אזורי חיתוך ע”י HIND3 : המרחק ביניהם שווה. מה שאומר שאם חותכים פלסמיד מעגלי ע”י 3 אנזימים נקבל שלושה מקטעים של DNA . אם המרחק שווה אז גודל המקטעים יהיה שווה. 3000 חלקי 3 שווה ל 1000, לכן החיתוך ע”י HIND3 יתן לנו 3 מקטעים שווים בגודל 1000. הבנד המייצג הינו מספר 3.
ב. HEA3 חותך את הפלסמיד באיזור אחד ויחיד. לכן החיתוך ע”י אנזים הרסטרקציה הזה יתן לנו שרשרת DNA באותו גודל של הפלסמיד אך במקום מעגל סגור שרשרת פתוחה. מה שאומר נצטרך לחפש על מקטע בגודל 3000 בסיסים בג”ל. הבנד המייצג הינו 2.
ג. ECORI חותך את הפלסמיד בשני אזורים, במרחק שאינו שווה, לכן מצפים כאן לראות שני בנדים בג”ל. בארית מספר 1 הינה היחידה שנותנת תוצר של שני בנדים.
Take home massage
חיתוך פלסמיד ע”י אנזים רסטרקציה במקום אחד ויחיד ייתן לי מקטע DNA ליניארי (במקום מעגלי) באותו גודל של הפלסמיד
חיתוך פלסמיד ע”י אנזים רסטרקציה בשני מקומות ייתן לנו 2 מקטעים ליניארים. לכן בפלסמיד מעגלי מספר המקטעים שווה ל מספר החיתוכים.
. בג’ל במקרה ויש לנו מקטעים שהם שווים בגודל ייוצגו ע”י אותו בנד.
להרחבה-Alberts, מהדורה 7, עמ’ 498-499 (Restriction enzymes).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – עבודה עם אנזימי רסטרקציה
אלברטס, פרק 8
שיטות מחקר 1 שאלה 21
חוקרים שיבטו רצף DNA upstream לגן דווח בפלסמיד Expression vector, החדירו אותו לחיידקים וראו כי ביטוי הגן עלה. במקביל הם שיבטו את אותו רצף DNA Downstream לרצף גן דווח וגם הפעם ביטוי הגן עלה.
מהו מקטע ה-DNA?
במה השאלה עוסקת: Expression vector.
תשובה ד.
אם ביטוי הגן עלה אז אנחנו מחפשים על איזור רגלטורי שמבצע בקרה חיובית. לכן פוסלים ג. ( אופרטור הינו האיזור שנקשר אליו סופרסור = בקרה שלילית שגורמת ברוב רובם של המקרים לירידה בביטוי הגן.נשארנו עם א ו ב ו ד.
עכשיו , אנו מחפשים על איזור רגלטורי שמבצע בקרה חיובית שאינה תלויית מיקום. א . פרומוטור הינו איזור רגלטורי החיובי לתחילת השיעתוק אך מאוד חשוב שיהיה UPSTREAM לגן. לכן נצפה אם נעביר הפרומוטור לסוף הגן שיהיה ירידה בביטוי הגן. נשארנו עם, ד. הגן המקודד לאקטיבטור.
האקטיבטור הינו אלמנט טרנס- הוא מתורגם לחלבון והחלבון מבצע תפקיד בביטוי הגן. לפי כך, אין חשיבות למקומו אלה רק לכך שהוא ימצע בגנום של אותו תא.
נשים לי כי הרצף יכול להיות גם אנהנסור- האנהנסר הינו אלמנט ציס- הוא רצף DNA אשר עליו יושבים חלבונים רגולטורים. מיקומו חשוב והוא חייב להיות על גבי אותו כרומוזום עליו הגן, אך לעיתים הוא יכול להיות גם Upstream וגם Downstream, ובפעמים רבות גם התזוזה שלו (אם לא רחוק מידי מהגן) עדיין יתרום להגברת הביטוי.
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שיבוט וחקר דנ״א
אלברטס, פרק 8
שיטות מחקר 1 שאלה 22
איזה חומרים / מכשירים צריך ע”מ לבצע PCR?
במה השאלה עוסקת: PCR
תשובה ד’. התשובה הנכונה היא ד. כל התשובות נכונות
הסבר: לצורך ביצוע ריאקציות PCR יש צורך ב:
טמפלט – יכולה להיות DNA או RNA
פריימר – רצף נוקלאוטידים החיוני לתחילת העבודה של האנזים DNA-POLYMERASE.
אנזים הנפוץ בשימוש במעבדה נקרא TAQ-POLYMERASE. יש לו יכולת לעבודה בטמפרטורות גבוהות. הוא הופק מיצורים טירמופילים. לכן הוא עמיד לטמפרטורות גבוהות ואין צורך להוסיף אותו בכל שלב. מוספים רק פעם אחת.
נוקלאוטידים – בכדי לבנות את הגדילים
מכשיר ה PCR- לשינוי הטמפרטורות
להרחבה – Alberts, מהדורה 7, עמ’ 506-510 (PCR).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שכפול דנ״א בעזרת PCR
אלברטס, פרק 8
שיטות מחקר 1 שאלה 23
איזה אנזים לא משתמשים בו במהלך ראקציית RT?
במה השאלה עוסקת: Reverse Transcription
תשובה ג. מכיוון שיש צורך POLY T PRIMER שישב על זנב ה-Poly A של ה-mRMA
להרחבה – Alberts, מהדורה 7, עמ’ 504.
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שיבוט וחקר דנ״א
אלברטס, פרק 8
שיטות מחקר 1 שאלה 24
על מנת לבדוק אם המחדר של רצף נכנס באופן נכון לתוך פלסמיד, נעשה PCR ונשתמש בזוג פריימרים. באיזה שני פריימרים נשתמש?
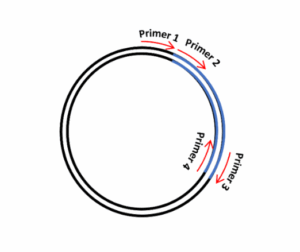
במה השאלה עוסקת- cloning DNA
תשובה א. התשובה א. חשוב מאוד לדעת כמה נקודות לפני שמתחילים לפתור את השאלה ע”מ שיווצר לנו תוצר בראקציית PCR צרוך שהפריימרים יהיו אחד FORWORD ואחד REVERSE. זה אומר צריכים שני פריימרים שתוחמים את המקטע. אחד על גדיל אחד מקצה ‘5 ל ‘3 . והשני מקצה ‘5 ל ‘3 אך על הגדיל השני ( דוגמה פריימר 2 שהינו FORWORD ופריימר 4 שהינו REVERSE). בנוסף, ע”מ לבדוק מקטע שהוחדר לתוך פלסמיד יש לעשות PCR באמצעות פריימר אחד שנמצא על הפלסמיד עצמו ופריימר אחר שנמצא על ה INSERT. אם נשתמש ב-2 ו-4 לדוגמא, נקבל תוצר לש הגברת המקטע, גם עם המקטע לא נכנס לפלסמיד.
שלילת מסיחים:
ב. שני הפריימרים יושבים על ה INSERT . זה יכול להיות אינדקציה שהמקטע קיים אך לא בהכרח הוכנס לתוך הפלסמיד
ג. שני הפריימרים באותו כיוון , לא יתן לנו תוצר PCR אלא במקרה והמקטע נכנס באופן הפוך
ד. שני הפריימרים יושבים על ה INSERT. בנוסף שני הפריימרים הם Forward.
להרחבה- Alberts, מהדורה שביעית, עמ’ 501-503 (DNA cloning using bacteria)
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שיבוט וחקר דנ״א
אלברטס, פרק 8
שיטות מחקר 1 שאלה 25
שימוש באילו שני פריימרים ילמד אותנו אם המחדר נכנס הפוך?

במה השאלה עוסקת: DNA cloning
תשובה ג’. בשאלה זו נעבוד עם אותם עקרונות כמו בשאלה הקודמת רק שהפעם אנו רוצים לדעת באיזה פריימרים משתמשים בכדי לגלות עם המחדר נכנס הפוך.
נשתמש בפריימר 1 כפריימר Forward- מכיוון שהוא היחיד מחוץ למחדר.
בנוסף נדמיין מה יקרה עם נהפוך את המחדר פעמיים (ראש-זנב, ולמעלה למטה). במקרה הזה נראה כי פריימר 2 יהיה במיקומו של פריימר 4 ובו אפשר להשתמש כפריימר Reverse.
להרחבה- Alberts, מהדורה שביעית, עמ’ 501-503 (DNA cloning using bacteria)
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שיבוט וחקר דנ״א
אלברטס, פרק 8
שיטות מחקר 1 שאלה 26
מה רצף הטמפלט אותו ריצפו ב-?Sanger
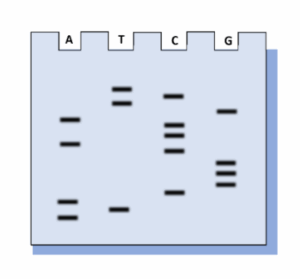
במה השאלת עוסקת: ריצוף על שם sanger.
תשובה ד’. תחילה יש לזכור שרצף תמיד נכתב מ-5′ (שמאל) ל-3′ (ימין).
לאחר מכן יש להבין איזה רצף מבקשים בשאלה- את הרצץ ה-“מקורי” (original)- בעצם “רצף הטמפלט”- הרצף האפור.או את תוצר הריצוף- הרצף הירוק. אם מבקשים את רצף הטמפלט- יש לקרא את הג’ל מלמעלה למטה כשמחליפים G ב-C ו-A ב-T ולהפך. אם מבקשים את תוצר הריצוף, קוראים את הג’ל מלמטה למעלה מבלי להחליף בין החומצות גרעין הקומפלמנטריות. בשאלה זו ביקשו את רצף הטמפלט. לבסוף כותבים את הרצף מ-5′ ל-3′- על כן בשאלה זו התשובה היא ד.
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – ריצוף דנ״א
אלברטס, פרק 8
להרחבה – Alberts, מהדורה 7, עמודים 512-513
שיטות מחקר 1 שאלה 27
באילו מהשיטות הבאות אין צורך בהיברידיזציית מולקולת DNA קצרה למולקולת DNA ארוכה כחלק מהשיטה?
במה השאלה עוסקת: אינטגרציה בין שיטות
תשובה ב’. נבצע סריקה לשיטות: ( ההמלצה – להכיר את השיטות האלה מאוד טוב: מבחינת חומרים שמשתמשים בהם , תהליך השיטה, מטרת השיטה)
בשיטת FISH אנו משתמשים בפרובים שמסומנים פלורוסנטית שנקשרים לאיזורים קומפלמנטרים ב DNA . בשיטה הזו אנו בודקים חסרים גדולים או דופלקציות ( שינויים גנומיים גדולים) . מדגישה שוב – לא משתמשים בשיטה הזו לבדיקת שינויים גנטים קטנים כמו החסרות של כמה בסיסים / missense mutation / nonsense / synonymous
גן דווח – הינו גן שמקודד לחלבון מדווח ( פלורסנטי / רדיואקטיבי). יש לו כמה מטרות מהן : בדיקת מיקום של חלבון , חלק תפקיד פרומוטרים .
ב PCR משתמשים בפריימרים ( באורך של 20 נוקלאוטדים בערך) שעוברים היברידיזציה לאזורים קומפלמנטרים וחיוניים לביצוע ה PCR
ה-Microarray גם תלוי מאוד בקומפלמנטציה וקשירת מקטעים שהם קומפלמנטרים .
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שיבוט וחקר דנ״א
אלברטס, פרק 8
שיטות מחקר 1 שאלה 28
הוכלאו שתי זיקיות בעלי פנוטיפ מוטנטי לבן, כל הצאצאים בדור F1 היו בעלי פנוטיפ WT- בעלי צבע ירוק, איך זה אפשרי?
במה השאלה עוסקת: מבחן קומפלמנטציה
תשובה א’. לשים לב שמבחן קומפלמנטציה רלוונטי למוטציות רציסיביות. ניכנס קצת לעולם הגנטיקה. במידה ויש שני יצורים בעלי פינוטיפ דומה (פינוטיפ חולה). והיוולד להם צאצאים שכולם בריאים זה יכול להיות רק במקרה ויש לנו מוטציות רציסיביות בגנים שונים. במקרה ויש לנו שתי מוטציות רציסיביות שונות באותו גן : נצפה שכל הצאצאים יהיו חולים. במקרה והמוטציות דומננטיות בגנים שונים – נצפה ש 50% מהצאצאים יהיו חולים. במקרה שתי מוטציות דומיננטיות שונות באותו הגן – נצפה שיהיה לנו חצי מהצאצאים חולי ובנוסף – אם זה רלוונטי לבני אדם יהיה מקרים חוזרים של הפלות כי צאצאים שיקבלנו שני אללים מוטנטים לא ישרדו.
להרחבה – Alberts, מהדורה 7, עמוד 521
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – גנטיקה
אלברטס, פרק 8
שיטות מחקר 1 שאלה 29
באיזה שיטה ניתן להשתמש בכדי להפריד מולקולות DNA ארוכות במיוחד לפי גודל?
במה השאלה עוסקת: הפרדת מקטעי DNA
תשובה ג’.
נעבור על המסיחים:
א. משתמשים בו להפרדת חלבונים ב Western blot
ב. ב-ChIP- חוקרים רצפים על גבי ה-DNA שנקשרים לחלבונים קושרי כרומטין- אין קשר להפרדת מולקולות DNA לפי גודל.
ג. הפרדת מולקולות DNA גדולות ( כרומוזום למשל – ב”כ חותכים אותו לכמה חתיכות לפני) על ידי שימוש בשני שדות חשמליים מכיוונים שונים- התשובה הנכונה.
ד. GWAS חקר אסוציאציות בין וריאנטים גנטים למחלות מורכבות- אין קשר להפרדת מולקולות DNA לפי גודל.
להרחבה – Alberts, מהדורה 7, עמ’ 500
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – ג׳ל אלקטופורזה
אלברטס, פרק 8
שיטות מחקר 1 שאלה 30
באיזה חומרים משתמשים בריצוף סאנגר?
במה השאלה עוסקת: ריצוף סאנגר.
תשובה ד’. הסבר: בריצוף סאנגר משתמשים בעודף DNTP , מעט ddNTP , ג’ל polyacrylamide , ו DNA POLYMERASE.. משתמשים במעט ddNTPs בכדי שהעצירה של הפילמור לא יקרה לעיתים קרובות מידי ולא נוכל לרצף את המשך הרצף.
להרחבה – Alberts, מהדורה 7, עמודים 512-513
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – ריצוף דנ״א
אלברטס, פרק 8
שיטות מחקר 1 שאלה 31
איזו מבין האפשריות הבאות מתארת בצורה המדוקית ביותר את עקרון הפעולה של שיטת הריצוף SMRT?
במה השאלה עוסקת: shotgun sequencing.
תשובה ב’. בשיטת SMRT (Single Molecule Real Time) משתמשים בדנ״א פול׳ שמבצע סינתזה של מולקולה בודדת של דנ״א. כאשר נוקלאוטיד מסומן בפלואורופור מצטרף לגדיל הדנ״א החדש, נפלט פולס פלואורסצנטי קצר.
מערכת אופטית רגישה מזהה את הפולס הזה בזמן אמת ומאפשרת לקבוע איזה נוקלאוטיד נוסף.
כך מתבצע ריצוף – תוך כדי סינתזה, פולס אחרי פולס.
שלילת המסיחים:
א – יש שימוש בדנ״א פול׳ בשיטה
ג – בשיטת SMRT אין שימוש בג’ל אלקטרופורזה. אין צורך להפריד לפי גודל, כי מזהים בזמן אמת איזה נוקלאוטיד הוסף.
ד – מסיח זה מתייחס לשיטת Nanopore.
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – ריצוף דנ״א
אלברטס, פרק 8
שיטות מחקר 1 שאלה 32
מה לא נכון לגבי illumine
במה השאלה עוסקת: illumine.
תשובה ב’. בשיטה יש שימוש ב-dNTP מיוחד בעל פלורופור וחסם על גבי ה-OH של עמדה 3. לאחר כל סיבוב יש הסרה של הפלורופור והחסם והמשך הסינתזה.
להרחבה – Alberts, מהדורה 7, עמ’ 514-515
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – ריצוף דנ״א
אלברטס, פרק 8
שיטות מחקר 1 שאלה 33
באיזה אנזים לא משתמשים בשיטת ה Ribosome profiling?
במה השאלה עוסקת: ribosome profiling
תשובה ד’. בשיטת Ribosome profiling ניתן לחקור את ביטוי הגנים בשלב תרגום החלבון על ידי מציאת מיקום הריבוזום על גבי ה-mRNA וכך לגלות אילו רצפים עוברים תרגום בפועל.
מהלך השיטה- בשלב הראשון הפקת mRNA מתאים וחשיפתו לנוקלאזות שיעקלו את המקטעים ב-RNA שאינם מוגנים על ידי הריבוזום (כלומר, אינם באמצע תרגום בזמן בקיבוע). בשלב הבא, מפרידים את ה-mRNA מהריבוזומים, יוצרים ממנו cDNA על ידי (Reverse Transcriptase). לבסוף ריצוף ה-cDNA וזיהוי המקטעים המרוצפים.
יש להכיר את כל החומרים שמשתתפים בתהליך
להרחבה – Alberts, מהדורה 7, עמ’ 538-540 (Ribosome profiling).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – שיטות למחקר ביטוי גנים ותרגום חלבונים
אלברטס, פרק 8
שיטות מחקר 1 שאלה 34
לין הכליאה שני ינשופים בצבע לבן וקיבלה צאצאים שכולם הציגו פנוטיפ בצבע חום, מה הסיבה לכך (הWT- הינו הינשוף בצבע חום)?
במה עוסקת השאלה: זיהוי מוטציות בגנים שונים
תשובה: ג’. רוב המוטציות הקיימות הינן רצסיביות, וישנן לא מעט מוטציות הגורמות לאותו פנוטיפ. כדי לדעת האם למשל שתי מוטציות שגורמות לאותו פנוטיפ קיימות באותו הגן, או שמא בשני גנים נפרדים כדי שניתן יהיה לטפל בצורה טובה יותר, אפשר לבצע מבחן קומפלימנטציה- אם שתי המוטציות נמצאות על גנים שונים, אז בהכלאה של אמא ואבא בעלי המוטציות, נצפה לקבל צאצא שלא יראה את הפנוטיפ המוטנטי, ולכן נוכל להגיד שיש קומפלינטציה. בשאלה זו, אכן נראה שהכלאה של שני ינשופים לבנים הובילה לצאצא עם פנוטיפ בצבע חום.
שלילת המסיחים:
א. אילו היו אלו מוטציות באותו הגן, היינו מצפים לקבל צאצא בצבע לבן
ב+ד. אם מדובר במוטציות דומיננטיות, לא היה זה משנה היכן הם ממקומים, והיינו מצפים לקבל צאצא בצע לבן
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – גנטיקה
אלברטס, פרק 8
שיטות מחקר 1 שאלה 35
איזו סוג מוטציה מחייבת על מנת להשתמש באנליזת אספיסטזיס?
במה עוסקת השאלה: קביעת סדר פעולות של גנים
תשובה: א. מוטציית NULL מביאה להפסקת פעילות מוחלטת של אותו חלבון. כאמור, אנליזת אפיסטזיס- תפקידה לבדוק מהו סדר הפעולות של אנזימים שונים באותו המסלול. לדוגמה : מסלול הפרשה של חלבון מסוים. ( להיזכר: ER> גולגי’> וסיקולות הפרשה> חוץ התא). כדי לבדוק את סדר הפעילות של האנזימים הפועלים בכל מדור, נגדיר שאנזים בER- הינו A ואנזים בגולג’י B. שימוש בקומבינציית מוטציות : פעם רק A מוטנט, פעם רק B מוטנט, ופעם גם A וגם B מוטנטים. התוצרים הסופיים מראים שאם B מוטנט, נראה הצטברות בER, אך גם A מוטנט נראה הצטברות בER, וכנל גם בשניהם. משמע, סדר פעילות הגנים מתחיל בER, שהכרחי לפעילות תקינה של הגולג’י. כך אפשר לגלות תהליכים רבים בתאים.
שלילת מסיחים:
ב-מוטציה הגורמת לפנוטיפ של Loss of function, גם אם יש אלל אחד תקין. זוהי תופעה שמתרחשת כאשר תוצר הגן המוטנטי מפריע לפעילות תוצר הגן התקין.
ג- מוטצייה סופרסורית- גורמת לביטול פנוטיפ מוטנטי אחר שקיים. כלומר מוטציה אחת ממסכת על מוטציה אחרת שכבר הייתה קיימת, ולכאורה נצפה לקבל פנוטיפ רגיל. לכן לא נוכל לזהות את האפיסטזיס בעזרתה
ד- מוטציית LOF- להבדיל ממוטציית NULL, יש ירידה\הפסקה של פעילות החלבון, אך לא בצורה מוחלטת, ולכן עדיין נראה פעילות בזאלית של החלבון, מה שעלול לפגום בהסקה שלנו עבור אותו התהליך.
להרחבה: Alberts 7th edition מוטציות (עמ’ 521), אנליזת אפסיטזיס ( עמ’ 523-524)
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – גנטיקה
אלברטס, פרק 8
שיטות מחקר 1 שאלה 36
מי מהבאים הוא דוגמה לREVERSE GENETIC?
במה השאלה עוסקת: Reverse genetics.
תשובה ב’. שיטת ה”גנטיקה לאחור” (Reverse genetics) היא שיטה שבה נקודת המוצא של החוקר היא גן מוכר ותקין שבו הוא מבצע מוטציה. זאת בניגוד, לגנטיקה הקלאסית שבה החוקר מתחיל לחקור פנוטיפ מוטנטי ע”י סקירת המוטציות והגנים שגרמו לו. בגנטיקה לאחור הגן שנבחר למחקר הוא גן שמוכר וידוע ומבצעים בו מוטציה אשר תגרום להפסקת פעילותו על מנת לקבוע את מעורבותו והשפעתו על תהליכי התא. בצורת מחקר זו ניתן לבצע לגן Knock-out, Knock-in ו-Knock-down על מנת להפסיק את פעילותו.
שלילת מסיחים:
א’. נקודת המוצא של שיטת הגנטיקה לאחור היא גן ידוע, ולכן זיהוי הגן שממנו משועתק mRNA מסוים אינו נכנס תחת שיטה זו. כמו כן, ההתחלה היא ממקור לא מוטנטי, אלא מגן פעיל נורמלי שבו נעשה מוטציה מכוונת על מנת לבדוק את ההשפעה שלו על פעילות התא.
ג’. שוב, בשיטה הנ”ל נקודת הפתיחה חייבת להיות משהו תקין, או גן תקין או חלבון תקין ואז יצירת מוטציה מכוונת, ולכן מסיח זה אינו נכון. כמו כן, חשוב להכיר את המושג מוטציה סופרסורית (Suppressor mutation) אשר מתאר את התופעה שבה מוטציה חדשה גורמת להעלמות פנוטיפ מוטנטי שנגרם ממוטציה קודמת, כלומר 2 מוטציות שאחת מתקנת את השנייה וגורמת להופעת פנוטיפ נורמלי.
ד’. כפי שנאמר מעל, כאשר המחקר מתחיל מפנוטיפ לא תקין, שזו המחלה סיסטיק פיברוזיס (Cystic fibrosis) במקרה זה, זו דוגמה לגנטיקה קלאסית (Classical genetics) ולא ל-Reversed genetics.
להרחבה- Alberts, מהדורה שביעית, עמ’ 518-519 (Reverse genetic) ועמוד 521 (Mutations).
נושא – שיטות מחקר, תת-נושא – שיטות בביולוגיה מולקולרית, תת-תת נושא – גנטיקה
אלברטס, פרק 8
