שאלון מערכת: שיעורי בית ביוכימיה 3
ביוכימיה 3 שאלה 1
היכן ובאילו חומצות אמינו מפרק האנזים כימוטריפסין (chymotrypsin) קשרים פפטידים?
במה השאלה עוסקת: מנגנונים אנזימטיים
תשובה ג. אנזימים פרוטאוליטים (אנזימים המפרקים חלבונים) נבדלים ביניהם באזור בו חותכים בקשר הפפטידי (צד קרבוקסילי או אמיני) ובספציפיות לחומצות האמיניות בהם נוטים לחתוך את הקשר הפפטידי. כימוטריפסין הינו פרוטאז אשר חותך בצד הקרבוקסילי של הח”א האמיניות הארומטיות – פנילאלנין, טריפטופן וטירוזין. במבנה של כימוטריפיסין ישנו כיס הידרופובי המתאים לקישור חומצות אמיניות אלו (כזכור, חומצות אמיניות ארומטיות הן גם הידרופוביות).
שלילת מסיחים:
א. האנזים אשר חותך בצד הקרבוקסילי של החומצות האמיניות ארגינין וליזין הוא טריפסין. טריפסין הינו פרוטאז בעל דמיון לכימוטריפיסין, כאשר ההבדל העיקרי הוא באתר הקישור לסובסטרט. בטריפיסין מדובר באתר קישור טעון שלילית (אספרטט) המייצב את המטען החיובי של שייר ליזין/ארגינין.
ב. האנזים Cyanogen Bromide חותך בצד הקרבוקסילי של מתיונין.
ד. האנזים אנדופרוטיאנאז (Endoproteinase) חותך בצד הקרבוקסילי של ליזין.
להרחבה – Lehninger, מהדורה שישית, עמוד 100 (Table 3-6).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: כימוטריפסין.
להרחבה – Lehninger, מהדורה שמינית, פרק 3, עמוד 424 (Table 3-6).
ביוכימיה 3 שאלה 2
הסכמה הבאה מתארת את השלב הראשון בריאקציה המזורזת ע”י הפרוטאז כימוטריפסין (chymotrypsin).
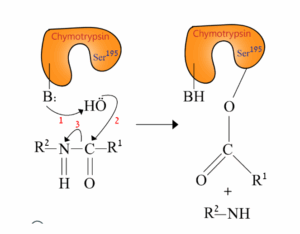
קטליזת בסיס כללית (general base catalysis) מתוארת ע”י המספר _______, ואילו קטליזה קוולנטית (covalent catalysis) מתוארת ע”י המספר ______.
שים /י לב שסדר המספרים הרלוונטיים בסעיפים נכתב מימין לשמאל.
תשובה א. בקטליזת בסיס כללית ישנה חומצה אמינית באתר הפעיל אשר מקבלת פרוטון. ניתןלראות שבמספר ‘1’ ישנו B (Base) בעל זוג אלקטרונים לא קושר. הבסיס משתמשבזוג אלקטרונים אלו בשביל לקבל פרוטון מהסובסטרט והופך ל-BH. בקטליזה קוולנטית נוצר קשר כפול בין האתר הפעיל לסובסטרט. ניתןלראות שמספר ‘2’ יוצר קשר קוולנטי בין החמצן של סרין באתר הפעיל לבין הסובסטרט.
שלילת מסיחים:
א. מספר1 מתאר קטליזת בסיס כללית כפי שתואר, אך מספר 3 מתאר ביקוע של קשר פפטידי (פירוקקשר קוולנטי) ולא יצירה של קשר קוולנטי.
ב. מספר2 מתאר קטליזה קוולנטית כפי שתואר, ומספר 3 מתאר ביקוע של קשר פפטידי (פירוק קשרקוולנטי) ולא יצירה של קשר קוולנטי.
ג. מספר 3 מתארביקוע של קשר קוולנטי, ומספר 2 מתאר קטליזה קוולנטית.
להרחבה – Lehninger, מהדורה שישית, עמוד 216-217 (How to ReadReaction Mechanism)
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמוד 833 (How to read reaction mechanism),
762-769 (מנגנוני קטליזות).
ביוכימיה 3 שאלה 3
כיצד מכונה מנגנון העיכוב בו המעכב יכול להיקשר לקומפלקס האנזים-סובסטרט בלבד, ליצירת קומפלקס אנזים-סובסטרט-מעכב (ESI complex)?
במה השאלה עוסקת: מעכבים
תשובה ב. מעכב היכול להיקשר רק לקומפלקס אנזים סובסטרט (ES) הוא מעכב בלתי תחרותי (Uncompetitive). מעכב זה נקשר לאתר באנזים שאינו האתר הפעיל ומוביל לירידה בערך Km ולירידה בערך Vmax.
שלילת מסיחים:
א. בעיכוב תחרותי המעכב נקשר רק לאנזים החופשי, ובקישורו מתקבל קומפלקס אנזים-מעכב (EI). בעקבות קישור המעכב לאתר הפעיל חל עליה בערך Km אך אינו משפיע על Vmax.
ג. עיכוב לא תחרותי הוא תת סוג של עיכוב מעורב. בעיכוב מעורב, המעכב יכול להיקשר גם לאנזים החופשי (לקבלת EI) וגם לקומפלקס ES (לקבל ESI). מכיוון שבשאלה מדובר במעכב הנקשר לקומפלקס ES בלבד מסיח זה נפסל.
ד. בעיכוב מעורב, המעכב יכול להיקשר גם לאנזים החופשי (לקבלת EI) וגם לקומפלקס ES (לקבל ESI). מכיוון שבשאלה מדובר במעכב הנקשר לקומפלקס ES בלבד מסיח זה נפסל.
להרחבה – Lehninger, מהדורה שישית, עמוד 208 Figure 6-15))
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמוד 804 (Figure 6-19), 808 (Figure 6-20), 810 (Figure 6-21).
ביוכימיה 3 שאלה 4
מי מבין הבאים אינו ידוע כמנגנון המשמש ליצירת שינוי הפיך (reversible alteration) בפעילות אנזים?
במה השאלה עוסקת: בקרה אנזימטית
תשובה א. חיתוך של זימוגן מצורתו הלא פעילה לצורתו הפעילה הינו סוג בקרה בלתי הפיכה. לאחר שהזימוגן עובר חיתוך הוא לא יכול לעבור הרכבה חזרה לזימוגן, ולכן האנזים יישאר פעיל עד שיפורק או יופרש ע”י הגוף (אופציה נוספת לעצירת פעילות האנזים היא שינוי הסביבה בה יכול לעבוד – כגון pH).
שלילת מסיחים:
ב. בבקרה אלוסטרית מולקולה קטנה נקשרת לאתר רגולטורי באנזים בצורה לא קוולנטית. קישור זה נעשה באמצעות קשרים חלשים והינו הפיך. בקרה אלוסטרית נפוצה מאוד באנזימים.
ג. קצב בנייה ופירוק של חלבונים יכול להיות מווסת ע”י בקרים שונים (כגון פקטורי שעתוק שיעודדו ביטוי של אנזימי בנייה או אנזימי פירוק). בקרה זו הינה הפיכה כתלות בתנאים בהם נמצא התא.
ד. מודיפקציה קוולנטית הינה בקרה הפיכה. דוגמא נפוצה היא זרחון של אנזימים (הוספת קבוצת פוספט בקשר קוולנטי לאנזים). הזרחון יכול להפעיל או לעכב את האנזים (כתלות באנזים המדובר), ודה-זרחון יכול לבטל את השפעת הזרחון.
להרחבה – Lehninger, מהדורה שישית, עמוד 226 (Regulatory Enzymes)
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמוד 852 (Regulatory Enzymes).
ביוכימיה 3 שאלה 5
מי מבין מנגנוני העיכוב הבאים הינו בלתי-הפיך?
במה השאלה עוסקת: מעכבים
תשובה ד. מעכבים אשר נקשרים לאנזים באינטרקציות חלשות (אינטרקציות לא קוולנטיות) הינם מעכבים הפיכים מכיוון שלאחר פרק זמן מסוים המעכב יתנתק מהאנזים והאנזים יוכל לחזור לפעול. לעומת זאת, מעכבים הנקשרים בקשרים קוולנטים לאנזים לרוב מובילים לעיכוב בלתי הפיך – האנזים לא יכול להשתחרר מהמעכב ולא יחזור להיות פעיל.
שלילת מסיחים:
א. עיכוב תחרותי הינו עיכוב הפיך וניתן להתגבר עליו ע”י העלאת ריכוז הסובסטרט.
ב. עיכוב לא תחרותי הינו מקרה פרטי של עיכוב מעורב. בעיכוב זה המעכב נקשר בקשרים חלשים לאנזים (קשרים לא קוולנטים) ולכן זהו עיכוב הפיך.
ג. מעכב בלתי תחרותי נקשר בקשרים חלשים לאנזים (קשרים לא קוולנטים) ולכן זהו עיכוב הפיך.
להרחבה – Lehninger, מהדורה שישית, עמודים 207-210 (Enzymes Are Subject to Reversible or Irreversible Inhibition)
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמודים 802-814 (Enzymes Are Subject to Reversible or Irreversible Inhibition).
ביוכימיה 3 שאלה 6
חוקרים ביצעו ניסוי בו בדקו את פעילות האנזים טריפטאז בנוכחות מעכב כלשהו בריכוז קבוע. להלן הנתונים הקינטיים של האנזים בנוכחות מעכב ובהיעדרו. בשני הניסויים נעשה שימוש באותו ריכוז אנזים.
![]()
בהסתמך על נתונים אלו, אילו מבין ההיגדים הבאים נכון?
במה השאלה עוסקת: קינטיקה אנזימתית, מעכבים.
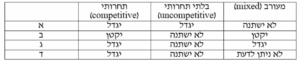
תשובה ב’. שאלה זו דורשת ניתוח מידע. השלב הראשון בפתרון הוא קביעת סוג המעכב. ניתן לראות שערך Km וערך Vmax קטנים בנוכחות המעכב, מה שמשאיר שתי אופציות: עיכוב בלתי תחרותי (Uncompetitive) או עיכוב מעורב (mixed).
בשביל להבדיל בין השניים נקבע האם Km ו-Vmax קטנים באותו היחס ואז מדובר בעיכוב בלתי-תחרותי, או שהם קטני ביחס שונה אחד מהשני ואז מדובר בעיכוב מעורב.
אנו רואים ש-Km קטן פי 2, ו-Vmax קטן פי 3, כלומר השינוי בשיעור העיכוב על כל מרכיב שונה ולכן ניתן להסיק שמדובר על מעכב מסוג Mixed.
בשלב הבא, נקבע את הגודל של α ו α’ וכך נוכל לקבוע האם למעכב אפיניות גבוהה יותר לקומפלקס ES או לאנזים החופשי. α מבטאת את מידת עיכוב האנזים החופשי ו-α’ את מידת עיכוב קומפלקס ES. המהירות המקסימלית במהלך עיכוב מעורב (Vmax app) שווה
ל-Vmax/a’=Vmax app. ערך Km במהלך עיכוב (Km app) שווה ל-αKm/α’=Km app.
לפי הנתונים נציב במשוואות הנ”ל ונקבל:
Vmax app=6/α’=2 ולכן α’ שווה ל-3.
מכאן ניתן לחשב את α:
Km app=(α*2)/3=1 ומכאן נקבל כי α שווה 1.5.
ניתן לראות כי ערך α’, המתאר את עיכוב קומפלקס ES, גדול פי 2 מערך α, המתאר את מידת עיכוב האנזים החופשי, ומכאן ניתן להסיק כי למעכב יש אפיניות גבוהה יותר לקומפלקס ES מאשר לאנזים החופשי.
כבר פה ניתן לפסול את שלושת המסיחים האחרים ולסמן את המסיח הנותר – קבוע הדיסוציאציה של קומפלקס ESI קטן פי 4 מקבוע הדיסוציאציה של קומפלקס EI.
על מנת שנפתור את השאלה עד הסוף נכיר את ההגדרה של α ו-α’ בקצרה בכדי להבין זאת:
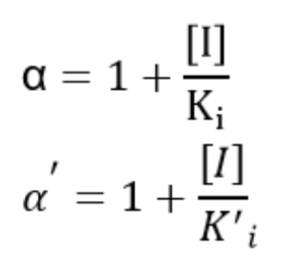
לפי הגדרה זו, אנחנו רואים ששתי האלפות תלויות ביחס הפוך ב-Ki, המהווה את קבוע הדיסוציאציה, ומדד לאפיניות, של הקומפלקס EI (אנזים-מעכב). ערך K’i הוא קבוע הדיסוציאציה של קומפלקס ESI (אנזים-סובסטרט-מעכב). במילים אחרות, ככל שהאפיניות, שמבוטאת ע”י קבוע הדיסוציאציה, גבוהה יותר (ולכן קבוע הדיסוציאציה קטן יותר), כך α או α’ תהיה גדולה יותר, וכך העיכוב יהיה חזק יותר.
כעת נחשב את היחס בין Ki ו-K’i:
מכיוון שמדובר באותו ריכוז מעכב ([I]) בשתי המשוואות ניתן להציב מספר שרירותי (למשל [I]=1) שיצטמצם בהמשך. שאר הנתונים ידועים לנו. לאחר הצבה ובדיקת היחס K/K’i נקבל כי קבוע הדיסוציאציה של קומפלקס ESI קטן פי 4 מקבוע הדיסוציאציה של קומפלקס EI (נזכיר כי ככל שקבוע הדיסוציאציה קטן יותר כך האפיניות גבוהה יותר).
שלילת מסיחים:
א. להפך. כפי שראינו, האפיניות של המעכב לקומפלקס ES גדולה פי 2 מהאפיניות לאנזים החופשי ולכן מסיח זה נפסל.
ג. מעכב בלתי תחרותי (Uncompetitive) נקשר רק לקומפלקס ES ולכן ערך Km מושפע רק מ-α’ (Vmax בכלמקרה מושפע רק מ-α’). לו היה מדובר בעיכוב בלתי תחרותי היינו רואים ירידה שווה בערך Km ו-Vmax.
ד. מכיוון שערך α שונה מערך α’ האפיניות של המעכב לאנזים החופשי ולקומפלקס ES שונה.
להרחבה – Lehninger, מהדורה שישית, עמודים207-209 (EnzymesAre Subject to Reversible or Irreversible Inhibition).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמודים 802-811 (Enzymes Are Subject to Reversible or Irreversible Inhibition).
ביוכימיה 3 שאלה 7
חוקרים מצאו מעכב חדש שפועל על אנזים הפרוטאז של וירוס ה- HIV. נמצא, שמעכב זה יוצר מספר רב יותר של אינטראקציות חלשות עם האתר הפעיל של האנזים מאשר הסובסטרט ולכן האפיניות שלו לאנזים גבוהה יותר. בהסתמך על כך, איזה מבין ההיגדים הבאים סביר בנוגע למעכב זה?
במה השאלה עוסקת: אנזימים – שיקולים תרמודינמיים, מעכבים.
תשובה א’. מצב המעבר הוא הצורה הכי פחות יציבה (בעלת הכי הרבה אנרגיה חופשית, שערכה מהווה את אנרגיית האקטיבציה של הריאקציה) שהסובסטרט צריך לעבור דרכה כדי להפוך לתוצר. מטרת האנזים הוא יצירת מספר מקסימלי של אינטראקציות עם מצב המעבר וע”י כך ייצוב שלו, הורדת האנרגיה החופשית שלו וכך מעבר מהיר יותר שלו לתוצר, ובסה”כ זירוז קצב הריאקציה. יצירת המספר המקסימאלי של האינטראקציות צריך לקרות במצב המעבר, ולא בצורת הסובסטרט: מכיוון שהסובסטרט הוא בעל אנרגיה חופשית יחסית נמוכה, אם האנזים ייצור איתו מספר מקסימאלי של אינטראקציות, יווצר קומפלקס ES בעל אנרגיה חופשית מאוד נמוכה, כלומר קומפלקס מאוד יציב, ולכן לא ימשיך הלאה לכיוון של יצירת תוצר.
תרופות רבות שמששמות בתור מעכבים תחרותיים של אנזימים הן למעשה אנלוגים של מצב המעבר – מול’ שדומות מבחינת המבנה שלהן למצב המעבר, ולכן האפיניות שלהן לאתר הפעיל של האנזים גבוהה משל הסובסטרט כי כאמור במצב המעבר נוצר המס’ המקסימאלי של האינטראקציות.
שלילת מסיחים:
ב. מעכב mixed לא נקשר לאתר הפעיל של האנזים.
ג. האנלוג של מצב המעבר יוצר מס’ מקסימאלי של אינטראקציות עם האנזים, יותר מאשר הסובסטרט יוצר, ולכן השינוי באנרגיה החופשית עבור הקישור שלו שלילי יותר מעבור השינוי של קישור הסובסטרט.
ד. זהו מעכב תחרותי ולכן מגדיל את Km ולא משפיע על Vmax
להרחבה: Lehninger 6th edition, ע”מ 210, 212
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, 804 (Figure 6-19 מעכב תחרותי),754-755 (השפעת האנזים על מצב המעבר), 818-819 (transition state analogs).
ביוכימיה 3 שאלה 8
איזה מבין המשפטים הבאים נכון בנוגע למעכב מסוג non-competitive?
במה השאלה עוסקת: קינטיקה אזימתית, מעכבים.
תשובה ד’. ראה הסבר מפורט לגבי מעכבים לשאלה 3. מעכב non-competitive הוא מקרה פרטי של מעכב mixed שבו α=α’ ולכן המעכב משפיע רק על ה-Vmax ולא על ה-Km. המשמעות ש- α=α’היא ש-Ki=k’i כלומר שקבוע הדיסוציאציה של המעכב מהקומפלקס ESI שווה לקבוע הדיסוציאציה של המעכב מהקומפלקס EI, מה שאומר שהאפיניות של המעכב לקומפלקס ES שווה לאפיניות לאנזים החופשי E.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמוד 809.
ביוכימיה 3 שאלה 9
כיצד ישתנה השיפוע של עקומת לינוובר-ברק (Linweaver-Burk) בנוכחות מעכב תחרותי (competitieve), בלתי תחרותי (uncompetitive) ומעורב (mixed)?
במה השאלה עוסקת: קינטיקה אנזימתית, עקומת לינוובר-ברק.
תשובה ג’. השאלה עוסקת בעקומת לינוובר ברק: תיאור ליניארי של משוואת מיכאליס-מנטן. ניתן לייצג את משוואת מיכאליס-מנטן כקו ישר ע”י הצבת 1/Vo במקום Vo ו-1/[S] במקום [S]. נקבל קו ישר שחותך את ציר Y ב:
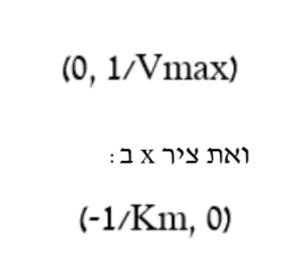
השיפוע של הישר הוא: Km/Vmax.
השפעת כל אחד מהמעכבים על שיפוע העקומה:
מעכב תחרותי – מעלה את Km ולא משנה את Vmax ולכן השיפוע גדל.
מעכב בלתי תחרותי (uncompetitive) – מקטין את Km ואת Vmax באותו סדר גודל (פי 1/ α’), ולכן לא משנה את השיפוע
מעכב מעורב (mixed) – מקטין תמיד את Vmax. יכול להגדיל או להקטין את Km כתלות ביחס α/ α’. אם גם אם Km יגדל וגם אם יקטן הוא אף פעם לא יעשה זאת היחס כמו ש-Vmax קטן ולכן השיפוע תמיד יגדל!
להרחבה: lehninger 6th edition, ע”מ 209
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמודים 782-783 (עקומת ליוונבר ברק), 804 (Figure 6-19), 808 (Figure 6-20), 810 (Figure 6-21)- מעכבים הפיכים.
ביוכימיה 3 שאלה 10
במערכת אנזימטית בה k2<<k-1 השתמשו במעכב מעורב (mixed inhibitor). נתון כי a=2 ו-α’=4. מהמהבאים נכון?
תשובה: ב’ (הזיקה בין האנזים והסובסטרט תגדל). מעכב מעורב (mixed inhibitor) הינו מעכב היכול להיקשר גם לאנזים החופשי וגם לקומפלקס ES. מקדם עיכוב α מתייחס לעיכוב האנזים החופשי ומקדם עיכוב α’ מתייחס לעיכוב קומפלקס ES. קישור מעכב לאנזים החופשי מוריד את היכולת שלו לקשור סובסטרט ולכן מקדם עיכוב α יוביל לעלייה בערך Km, בעוד קישור מעכב לקומפלקס ES מעודד היווצרות של קומפלקס ES נוספים (לפי עקרון לה-שטלייה) ומכאן שα’ יוביל לירידה בערך Km.
בעיכוב מעורב נקבל Kmapp שווה לalphaKm/alpha והיחס בין המקדמים יקבע מה תהיה ההשפע העל Km.
במקרה שלנו: 2Km/4=Km/2. ערך Kmapp קטן מערך Km ומכיוון שk2<<k-1, Km מייצג זיקה הזיקה בין האנזים לסובסטרט תגדל.
שלילת מסיחים:
א. בעיכוב לא תחרותי ערכי α ו-α’ שווים ולכן לא נצפה שינוי ב-Km. בשאלה זו ערכי α וα’ אינם שווים ולכן זהו לא עיכוב לא תחרותי.
ב. המהירות המקסימלית מושפעת מעיכוב קומפלקס ES. אם הקומפלקס מעוכב יווצר פחות תוצר מה שיוריד את מהירות הריאקציה. לכן נצפה שבנוכחות מעכב מעורב המהירות המקסימלית תרד.
ד. ערך Km עלול לעלות, לרדת או להשאר זהה בעיכוב מעורב. במקרה המדובר בשאלה, לפי היחס בין α ל-α’ ערך Km יורד
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמוד 810 ׁׁׁ(Figure 6-21), עמוד 811 (Table 6-9).
ביוכימיה 3 שאלה 11
מה נכון לגבי עיכוב לא תחרותי (noncompetitive)?
תשובה: ג’ (בעקומת מיכאליס מנטן הנקודה בה המהירות ההתחלתית שווה ל-0.5Vmax זהה בעקומה עם המעכב ובעקומה ללא מעכב). עיכוב לא תחרותי הינו תת סוג של עיכוב מעורב בו אין שינוי ב-Km (מקדם עיכוב α ו-α’ שווים) אך יש ירידה במהירות המקסימלית. Km זהו הריכוז בו מהירות הריאקציה שווה לחצי מהמהירות המקסימלית, ולכן אם אין שינוי ב-Km הריכוז הדרוש לקבלת 0.5Vmax יישאר זהה.
שלילת מסיחים:
א. בנוכחות מעכב לא תחרותי המהירות המקסימלית תרד. בעקומת LB ציר Y מתייחס ל-1/Vmax ולכן ככל שמתקרבים לראשית הצירים המהירות המקסימלית עולה. בנוכחות המעכב נקודת החיתוך עם ציר Y תתרחק מראשית הצירים.
ב. מעכב מעורב נקשר גם לאנזים החופשי וגם לקומפלקס ES. המעכב נקשר באתר שהוא אינו האתר הפעיל.
ד. בעיכוב לא תחרותי יש ירידה במהירות המקסימלית אך אין שינוי בערך Km.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמוד 809-810.
ביוכימיה 3 שאלה 12
אילו חומצות אמינו יכולות לעבור זרחון (phosphorylation) כחלק מהבקרה על החלבון/אנזים בו הן נמצאות?
במה השאלה עוסקת: זרחון חומצות אמינו
תשובה א. כדי לענות על שאלה זו חשוב לזכור את הקיצורים של חומצות האמינו וכן להכיר את התכונות שלהם. חומצת אמינו שונות אחת מהשניה בקבוצות ה-R שהיא גם האזור שעובר זרחון. כדי לעבור זרחון, המולקולה צריכה להכיל אטום ריאקטיבי (כמו חמצן או חנקן), שקבוצת הפוספט תתחבר אליו. בסעיף הראשון חומצות האמינו הן – טירוזין (TYR), סרין (SER) וטראונין (THR) ולשלושתן אטום חמצן חפשי בשייר ה-R אליו קבוצת פוספט יכולה להתחבר. ניתן לחלק את חומצות האמינו לקטגוריות בהתאם למטען ולמידת הפולאריות שלהן, כאשר סרין וטראונין הן תחת הקטגוריה של חומצות אמינו פולאריות, לא טעונות. טירוזין היא בעלת מעמד מיוחד כיון שהיא מוגדרת כארומטית, ולפיכך הידרופובית, אך יש לה אטום חמצן ריאקטיבי ולכן היא יותר פולארית משאר חומצות האמינו הארומטיות. תכונה שמשותפת לכל חומצות האמינו הארומטיות היא בליעת גלי UV באיזור 280nm (בעיקר טירוזין וטריפטופן).
שלילת מסיחים:
ב. טירוזין וסרין יכולות לעבור זרחון, אך טריפטופן (TRP) היא מולקולה בעלת שייר צד ארומטי וכן היא חסרת אטום ריאקטיבי אליו קבוצת הפוספט יכולה להתחבר.
ג. אספרגין (ASN) היא פולארית ולא טעונה, כמו סרין ותראונין, יש לה אטום חמצן בשייר ה-R, אולם אטום זה מחובר בקשר כפול לפחמן ולפיכך לא פנוי ליצירת קשרי מימן או לחיבור קבוצת פוספט. כלומר, תנאי נוסף בכדי שקבוצת הפוספט תוכל להתחבר הוא קיומו של קשר יחיד בין הפחמן לחמצן שבשייר ה-R.
ד. פניאלאנין (PHE), כמו טריפטופן, היא מולקולה ארומטית ללא שיר צד ריאקטיבי ולכן לא יכולה לקבל קבוצת פוספט. היסטדין (HIS) יכולה לעבור זרחון על אחד משני החנקנים שבקבוצת ה-R שלה (למשל בשלב 5 של מעגל קרבס), אך המסיח נפסל עקב כך שפניאלנין לא יכולה לעבור זרחון.
להרחבה – Lehninger, מהדורה 6, עמודים 75-81 (חומצות אמינו).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: חומצות אמינו.
להרחבה: Lehninger מהדורה שמינית, פרק 3- עמוד 365-372 (חומצות אמינו), פרק 6- 864-865 הרחבה על פוספורילציה).
זרחון (phosphorylation) הוא שם התהליך בו מתווספת קבוצת פוספט תוך יצירת קשר פוספואסטרי עתיר אנרגיה. המולקולה אשר מקבלת את הפוספט יכולה להיות סוכר, חלבון, נוקלאוטיד או תוצר ביניים מטבולי. התהליך ההופכי הינו דה-זרחון (de-phosphorylation) בו מוסרת קבוצת פוספט. מודיפיקציות אלו חשובות מאוד בבקרת מסלולי סיגנל ופעילות חלבונים (כדוגמת פתיחה/ סגירה של תעלה) ומבוצעות ע”י אנזימים מסוג קינאזות (לרוב תוך שימוש ב- ATP כתורם פוספט) ופוספטאזות (בריאקציית הידרוליזה ושבירת הקשר הפוספואסטרי). לפחות מחצית מהאנזימים עוברים שפעול בעקבות זרחון או דה-זרחון ומדובר במודיפיקציה קוולנטית לאחר תרגום.
הערת מחבר – מומלץ לעבור על המודיפיקציות הקוולנטיות העיקריות אשר מוזכרות בעמוד 229 בספר.
הערת מחבר – מומלץ לעבור על המודיפיקציות הקוולנטיות העיקריות אשר מוזכרות בעמוד 862 בספר.
