שאלון: סימולציה 1
פיזיולוגיה 4 שאלה 11
בהינתן ממברנה פלסמתית סטנדרטית וריכוזי יונים סטנדרטים, מה יהיה בקירוב פוטנציאל ההיפוך של תעלה הנמצאת על גבי הממברנה ומוליכה נתרן ואשלגן?
במה השאלה עוסקת: פוטנציאל היפוך
תשובה ד’. גם לתעלה יש פוטנציאל היפוך, זהו המתח בו הזרם נטו דרך התעלה הוא אפס (זרמי הנתרן והאשלגן שווים והפוכים בכיוונם), ובהתאם פתיחת התעלה לא תוביל לשינוי מתח. כלומר, במידה ונקבע את התא הפוסט-סינפטי על מתח ההיפוך ונגרה את התא הפרה-סינפטי כך שיפריש נוירוטרנסמיטורים, נראה כי לא מתקבלים זרמים פוסט-סינפטים.
בתמונה- זרמים דרך תעלת אצפטור לאצטיל כולין. ככל שהמתח שלילי יותר- כוח המניע של נתרן גבוה יותר ויש יותר דהפולריזציה. ככל שמתח הממברנה עולה- הכוח המניע של נתרן יורד ושל אשלגן יורד- עד שהזרם הוא 0 (מתח ההיפוך) ואז הופך להיות היפרפולריזציה (זרם חיובי).
איך נחשב את מתח ההיפוך? במידה והמוליכויות של היונים שוות- מתח ההיפוך יהיה ממוצע של פוטנציאלי נרנסט של היונים- בדיוק במרכז. במידה והמוליכויות שונות- מתח ההיפוך יהיה קרוב יותר לפוטנציאל נרנסט של היון בעל החדירות הגבוה יותר.
בסינפסות אקסיטטוריות מתח ההיפוך הוא לרוב סביב 0mV כיוון שהוא ממוצע משוקלל של מוליכות התעלה ליונים השונים עם מתח שיווי המשקל שלהם. שימו לב, נניח ויש תעלה שמוליכה נתרן ואשלגן באופן שווה, אז פוטנציאל ההיפוך שלה (ממוצע פוטנציאלי שיווי המשקל של אשלגן ונתרן) יהיה שונה מאפס. המשוואה:
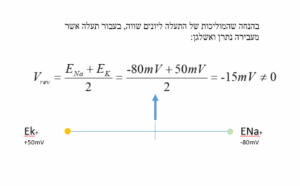
להרחבה – Bern & Levy, מהדורה 8 עמודים 22-25
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: שמירה על הומאוסטזיס
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 2
פיזיולוגיה 1 שאלה 30
הומאוסטזיס הוא מצב של-
במה עוסקת השאלה: שמירה על הומאוסטזיס
תשובה ב’. הומאוסטזיס – תהליך שמירת נפח, תכולה וטמפרטורות מדורי המים בגוף קבועים. הומאוסטזיס נשמר באמצעות השקעת אנרגיה, כלומר מדובר במצב יציב (steady state).
פיזיולוגיה 4 שאלה 9
מטופל קיבל תמיסה בעירוי. כתוצאה מכך נפח כל מדורי המים בגוף עלה. איזו תמיסה קיבל המטופל?
במה השאלה עוסקת: תמיסות בשימוש קליני
תשובה ב. בשאלה זו מטופל קיבל תמיסה בעירוי דרך הוריד. נתון שנפח כל מדורי המים בגוף עלה (הפלזמה, הנוזל הבין תאי והנוזל התוך תאי). החומר שיכול ליצור אפקט כזה צריך להיות חומר היפוטוני, אשר גורם למעבר של מים באוסמוזה ממדור הפלזמה (אליו הוא הוכנס) למדורים הנוספים בגוף. תמיסת Dextrose 5%, היא למעשה תמיסה היפוטונית על אף האחוז הגבוה. הסיבה לכך היא שדקסטרוז מתמוסס ל-CO2 ומים ולכן זה דומה להכנסה של מים מזוקקים. כיון שמדובר בתמיסה היפוטונית, התמיסה תיצור לחץ אוסמוטי יחסי גבוה במדור ה- ICF עקב כך שהתמיסה הפכה את הפלסמה להיפוטונית, ונראה מעבר של מים למדור זה. התוצאה תהייה עלייה בנפח כל מדורי הגוף וירידה באוסמולריות שלהם.
שלילת מסיחים:
א. סליין (Saline) היא תמיסה איזוטונית לנוזלי הגוף המכילה ריכוז של NaCl 0.9%. המשמעות היא שב-100ml תמיסה יש NaCl 0.9g, ויותר נוח לטעון שב-1L תמיסה יש NaCl 9g. כיון שהתמיסה איזוטונית לגוף היא רק תגדיל את הנפח של המדור החוץ תאי ולא תגרום לשינוי במדור התוך תאי. הסיבה לכך היא שגם לאחר הכנסת התמיסה חוץ התא ופנים התא עדיין איזוטוניים אחד לשני ולכן לא יהיה מעבר מים ביניהם. אולם, כיון שנתרן וכלור עוברים את קירות כלי הדם, העלייה בנפח תתרחש גם בנוזל הבין תאי ולא רק בפלסמה, או במילים אחרות בכל המדור החוץ תאי ולכן מסיח זה נפסל.
ג. כזכור, קירות כלי הדם מחוררים ומאפשרים מעבר של מולקולות קטנות, ולכן ישנו מעבר חפשי של מים ומולקולות (עד גודל מסוים), בין התווך הבין תאי והפלסמה המרכיבים יחד את ה-ECF. Dextran 5% הוא פולימר גדול עשוי מגלוקוז. החומר הוא גדול, כך שאינו עובר את כלי הדם ולא עובר בדיפוזיה לנוזל הבין תאי. בנוסף, החומר הוא היפרטוני ביחס לשאר המדורים. כלומר- הכנסתו תגרום לעלייה באוסמולריות של המדור אליו הוא הוכנס בלבד (הפלזמה) מכיוון שאינו חוצה את דפנות כלי הדם. לחץ אוסמוטי גבוה בפלזמה יוביל למעבר של מים מיתר המדורים למדובר הפלזמה. כתוצאה מכך נפח הפלזמה יעלה בעוד שנפח המדור הבין תאי והתוך תאי יפחתו (מים עזבו את המדורים הללו ונכנסו לפלסמה שנפחה עלה).
ד. תמיסת 5% NaCl היא אכן תמיסה היפרטונית לפלסמה, אך בשונה מדקסטרן היא תוביל לעלייה באוסמולריות של כל המדור החוץ תאי ולא רק של הפלסמה. הסיבה לכך היא חדירות כלי הדם לנתרן וכלור. בשאלה זו חפשנו תמיסה שתעלה רק את נפח הפלסמה ולא את נפח המדור החוץ תאי כולו ולכן מסיח זה נפסל.
להרחבה – Bern & Levy, מהדורה 8 עמוד 22 (“In The Clinic”).
פיזיולוגיה 1 שאלה 8
מה כוללת התגובה של תא לתמיסה היפוטונית וכיצד היא נקראת?
במה השאלה עוסקת: תגובות מסוג RVI ו-RVD
תשובה א. טוניות היא מדד השוואתי לריכוז מומסים אפקטיביים בשתי תמיסות שונות. מומסים אפקטיביים הם מומסים שיוצרים לחץ אוסמוטי כיון שאינם חוצים את הממברנה. כאשר מדברים על טוניות קיימים שלושה יחסים בין שתי תמיסות: איזוטוני, היפרטוני והיפוטוני. תמיסות איזוטוניות הן תמיסות עם אותה כמות מומסים אפקטיביים, תמיסה היפרטונית היא תמיסה עם יותר מומסים אפקטיביים ביחס לתמיסה אחרת ותמיסה היפוטונית היא תמיסה עם פחות מומסים אפקטיביים ביחס לתמיסה אחרת. כאשר מכניסים תא לתמיסה היפוטונית (כלומר תמיסה בעלת פחות מומסים אפקטיביים), מים נכנסים באופן כמעט מידי לתוך התא כדי להגיע למצב שתוך התא וחוץ התא הם איזוטונים אחד לשני. בכדי למנוע התנפחות נוספת של התא בעקבות כניסת מים, קיים מנגנון המכונה RVD (regulatory volume decrease). במנגנון זה מוצאים מומסים אפקטיביים מהתא ובכך מופחת הלחץ האוסמוטי בתוך התא ונפח התא חוזר לנפח נורמלי. לאחר הוצאת המומסים מהתא, שתי התמיסות (חוץ ופנים התא) הן איזוטוניות, כאשר האוסמולליות שלהן נמוכה מהערכים הסטנדרטים של התא. ישנם טרנפורטרים רבים שמוערבים בתגובה זו וכמו כן מולקולות רבות הכוללות יונים ומולקולות אורגניות שונות. דוגמה ליונים שיוצאים מהתא כחלק מתגובת RVD היא יציאה של אשלגן וכלור (KCl), בין אם זה באמצעות סימפורטר או באמצעות תעלות ספציפיות לכל יון.
שלילת מסיחים:
ב. בתגובת RVD התא מוציא מומסים ומים ובכך מפחית את גודלו וכל זאת כיון שהוא נחשף לתמיסה היפוטונית. בתמיסה היפוטונית יש ריכוז מומסים אפקטיביים נמוך באשר בתא, ומים נכנסים כדי להשוות ריכוזים. התא רוצה למנוע התנפחות נוספת והמנגנון לעשות זאת הוא באמצעות הוצאת מומסים. במידה והתא יכניס מומסים התוצאה תהיה הפוכה כיון שמים יוסיפו להיכנס לתא ונפחו יגדל. תהליך זה של גדילת התא מכונה RVI (regulatory volume increase) והוא מתרחש באופן טבעי בתגובה לחשיפת התא לתמיסה היפרטונית. במקרה של חשיפת התא לתמיסה היפרטונית, בתמיסה החיצונית של התא יש יותר מומסים אפקטיביים ומים נעים החוצה מהתא כדי ליצור מצב בו התמיסות איזוטוניות. ביציאת מים יש סכנה של איבוד נפח ולכן התא מכניס מומסים כגון נתרן וכלור (NaCl). הכנסת המומסים מעלה את הלחץ האוסמוטי בתא כיון שהמומסים גוררים אחריהם מולקולות מים. חשוב לציין שהכנסה זו של מומסים מעלה את אוסמולליות התא לערך גבוה מהערך הסדנרטי של התא. כלומר, אמנם חוץ ופנים התא איזוטוניים, אך לשניהם ערכים אוסמולליים גבוהים מהנורמה וזאת בעקבות חשיפת התא לתמיסה היפרטונית.
ג. ב-RVD יש תנועה של נוזלים החוצה מן התא אך הנוזלים נעים בעקבות המומסים. הרעיון המרכזי בתגובה זו הוא מעבר מהיר של מומסים אפקטיביים החוצה מהתא או הכנסתם לתוך התא. ניתן להניח שבמידה ונוזלים היו הרכיב המרכזי בתגובה, היינו מצפים למנגנון אחר כמו למשל רגולציה על תעלות מים.
ד. ב-RVI יש תנועה של נוזלים פנימה אל התא אך הנוזלים נעים בעקבות המומסים. הרעיון המרכזי בתגובה זו הוא מעבר מהיר של מומסים אפקטיביים החוצה מהתא או הכנסתם לתוך התא. ניתן להניח שבמידה ונוזלים היו הרכיב המרכזי בתגובה, היינו מצפים למנגנון אחר כמו למשל רגולציה על תעלות מים.
פיזיולוגיה 4 שאלה 24
תא הומני הועבר מתמיסה איזוטונית (תמיסה א’) לתמיסה היפוטונית (תמיסה ב’) ובחזרה לתמיסה א’. באילו מנגנונים התא ישתמש בכדי לשרוד את המעברים?
במה השאלה עוסקת: טוניות ומנגנוני RVD ו-RVI
תשובה ד. תא הועבר מתמיסה איזוטונית לתמיסה היפוטונית (כלומר תמיסה בעלת פחות מומסים אפקטיביים), עקב כך מים נכנסים באופן כמעט מידי לתוך התא כדי להגיע למצב שתוך התא וחוץ התא יהיו איזוטונים. בכדי למנוע התנפחות נוספת של התא בעקבות כניסת מים, קיים מנגנון המכונה RVD (regulatory volume decrease). במנגנון זה מוצאים מומסים אפקטיביים מהתא ובכך מופחת הלחץ האוסמוטי בתוך התא ונפח התא חוזר לנפח נורמלי. לאחר הוצאת המומסים מהתא, שתי התמיסות (חוץ ופנים התא) הן איזוטוניות, כאשר האוסמולריות שלהן נמוכה מהערך ההתחלתי של התא. ישנם טרנפורטרים רבים שמוערבים בתגובה זו וכמו כן מולקולות רבות הכוללות יונים ומולקולות אורגניות שונות. דוגמה ליונים שיוצאים מהתא כחלק מתגובת RVD – אשלגן וכלור (KCl), כאשר היציאה יכולה להתרחש באמצעות סימפורטר או באמצעות תעלות ספציפיות לכל יון.
בשלב הבא התא מועבר חזרה לתמיסה א’ שהיא כעת היפרטונית ביחס אליו. הסיבה לכך היא שתמיסה א’ הייתה איזוטונית לתא באוסמולריות מסוימת, אך לאחר החשיפה לתמיסה היפוטונית (תמיסה ב’) אוסמולריות התא ירדה עקב כניסת מים והוצאת מומסים. כאשר התא נחשף לתמיסה היפרטונית, מים נעים החוצה מהתא וזאת כדי ליצור מצב שפנים ותוך התא יהיו איזוטוניים. ביציאת מים יש סכנה של איבוד נפח ולכן התא מכניס מומסים כגון נתרן וכלור (NaCl). הכנסת מומסים אלו גורמת לכניסה של מולקולות מים ולשמירה על נפח התא. תהליך זה של גדילת התא מכונה RVI (regulatory volume increase).
שלילת מסיחים:
א. מנגנון RVI משמש להתמודדות מול תמיסה היפרטונית ולא היפוטונית כמו שכתוב במסיח. כאשר התא נמצא בתמיסה היפרטונית, מים עוזבים את התא ויש צורך בהכנסת מומסים בכדי לשמור על נפח התא.
ב. לאחר החשיפה לתמיסה ב’, התא כבר אינו איזוטוני לתמיסה א’ כיון שלמעשה הוא איזוטוני לתמיסה ב’. לפיכך כאשר התא נחשף בשנית לתמיסה א’, הסביבה הינה היפרטונית עבורו וזאת כיון שבמהלך שהייתו בתמיסה ב’ הוא איבד מומסים במנגנון RVD. עקב כך, בחשיפה השנייה לתמיסה א’, התא משתמש במנגנון המכונה RVI בכדי להכניס מומסים לתוך התא ובכך הוא נהיה בשנית איזוטוני לתמיסה א’.
ג. למעשה מסיח זה מתאר הפוך את המתרחש. תחילה התא משתמש במנגנון RVD וזאת כאשר הוא נחשף לסביבה היפוטונית. בהמשך התא משתמש במנגנון RVI וזאת כאשר הוא נחשף לסביבה היפרטונית. להסבר התהליך ראו פתרון לסעיף ד’.
להרחבה – Bern & Levy, מהדורה 8 עמודים 12-16 (אוסמוזה); 26 (RVD, RVI).
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: שמירה על הומאוסטזיס
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1
פיזיולוגיה 1 שאלה 9
היכן בתא האפיתליאלי (Epithelial cell) ממוקמת ברוב המקרים המשאבה Na-K-ATPase?
במה השאלה עוסקת: טרנספורט אפיתליאלי
תשובה א. תאי האפיתל חוצצים בין הסביבה החיצונית לסביבה הפנימית של הגוף. דוגמאות לכך הן תאי אפיתל העור שחוצצים בין הבגדים שאנו לובשים לבפנוכו, תאי אפיתל המעי שחוצצים בין האוכל שאנו אוכלים למחזור הדם וכמובן שיש דוגמאות נוספות. הצד שמופנה לסביבה הפנימית, כלומר לתוך הגוף, הוא הצד הבזאלי ואילו הצד שמופנה לסביבה החיצונית, כמו האויר והמעי, הוא הצד האפיקלי. תפקיד נוסף שיש לתאי האפיתל הוא להוות מחסום בררני שמכניס חומרים שצריך לספוג בחזרה לגוף ולא מכניס חומרים שיש להוציא מהגוף. לדוגמה, נתרן כמעט אינו מופרש בשתן ורובו נספג בחזרה על ידי תאי האפיתל שבכליות. האופן שבו הוא נספג חזרה הוא באמצעות תעלות נתרן שמכניסות נתרן עם המפל האלקטרוכימי שלו. מבחינת הפרשי ריכוזים, כיון שבתוך התא ריכוז הנתרן נשמר נמוך, יש לנתרן כוח מניע להיכנס לתא. מבחינה חשמלית, תוך התא יותר שלילי ביחס לחוץ התא והסיבה לכך הן תעלות הדלף לאלשגן שמוציאות אשלגן באופן קבוע מן התא (מהממברנה הבאזולטרלית) ובכך משפיעות על מתח הממברנה. כלומר, המפל האלקטרוכימי של נתרן הוא פנימה לתוך התא ולכן לא נדרשת השקעת אנרגיה כדי להכניסו ומספיק לבטא תעלות בצד האפיקלי בכדי שנתרן יכנס לתא. כדי לשמור על ריכוזי יונים קבועים, התא מבטא משאבות נתרן אשלגן והוא עושה זאת בצד הבאזולטרלי. הסיבה לכך היא שהתא לא מעוניין להפריש נתרן החוצה מהגוף ואף להפך, הוא מעוניין לספוג נתרן שהופרש. ביטוי משאבות נתרן-אשלגן בצד הבאזולטרלי מאפשר מעבר של נתרן מהסביבה החוץ תאית, דרך הממברנה האפיקלית עד הממברנה הבאזולטרלית שם משאבות נתרן-אשלגן מוציאות אותו מהתא ומחזירות אותו לגוף. סוג כזה של מעבר, שחוצה את הממברנה האפיקלית ואת הממברנה הבאזולטרלית, מכונה מעבר טרנסצלולארי (trnascellular). ישנו סוג מעבר נוסף דרך תאי אפיתל המכונה פאראצלולאר (paracellular). במעבר מסוג זה חומרים אינם עוברים דרך ממברנות התא, אלא דרך חלבונים שנמצאים במרווחים שבתאי האפיתל ומכונים tight junctions. חשוב לסייג את הנאמר בכך שמשאבות נתרן אשלגן ממוקמות בצד הבאזולטרלית, כיון שעקרון זה נכון לכל תאי האפיתל בגוף מלבד התאים ב-choroid plexus. ה-choroid plexus זה מבנה השייך לחדרי המוח והוא אחראי על יצירה והפרשה של ה-cerebrospinal fluid (CSF). בתאי אפיתל אלו, משאבת הנתרן-אשלגן נמצאת בצד האפיקלי.
שלילת מסיחים:
ב. התא מעוניין לספוג נתרן מהצד האפיקלי ועל כן זה יחשב בזבזני מצדו לבטא משאבות נתרן-אשלגן בצד זה. כמו כן, ביטוי המשאבות בצד הבאזולטרלי מאפשר לספוג את הנתרן בחזרה לגוף.
ג. התא מעוניין לספוג נתרן מהצד האפיקלי ועל כן זה יחשב בזבזני מצדו לבטא משאבות נתרן-אשלגן בצד זה. כמו כן, ביטוי המשאבות בצד הבאזולטרלי מאפשר לספוג את הנתרן בחזרה לגוף.
ד. כפי שכתוב בתשובה לסעיף א’, משאבות נתרן-אשלגן קיימות רק בצד הבאזולטרלי.
פיזיולוגיה 4 שאלה 8
נתונות ארבע תמיסות שונות של 1% אחוז משקלי- תמיסת אוראה, (Mw=60 ) תמיסת KCl (Mw=4 ) , תמיסת HCl(Mw=3 ) ותמיסת גלוקוז. (Mw=180 ) מי מבין התמיסות היא בעלת האוסמולריות הנמוכה ביותר?
במה השאלה עוסקת: אוסמולריות
תשובה ד. תמיסה המכילה 1% משקלי מכילה גרם אחד ב-100ml. כמובן שזה יכול להיות גם עשרה גרם ב-1L אבל נשאר עם הדוגמה של 1g/100ml. כמו כן לשם התזכורת, אוסמולריות נמדדת ב-osmol/L, כאשר osmol היא יחידת מידה למספר החלקיקים בתמיסה. בשאלה זו למשל החומר KCl יתפרק לאשלגן וכלור ולכן בתמיסה בריכוז של 1 mol/L של KCl נקבל אוסמולריות של 2 Osmol/L. כלומר ניתן לחשב בקלות את אוסמולריות התמיסה על ידי הכפלת הריכוז במספר החלקיקים שהמולקולה מתפרקת אליה בתמיסה. כעת אנחנו מחפשים את התמיסה עם האוסמולריות הנמוכה ביותר, כלומר עם הכי פחות חלקיקים. לשם כך נבחר את המולקולה הכבדה ביותר שלמעשה “תיכנס” הכי מעט פעמים בתוך 1g. לפיכך נבחר בגלוקוז כיון שהיא המולקולה הכי כבדה וכן אינה מתפרקת בתמיסה (מה שהיה מוביל להגדלה של האוסמולריות). כיון שגלוקוז הכי כבדה, פחות מולקולות גלוקוז נכנסות בגרם אחד ולכן זו התשובה הנכונה. ניתן לראות זאת גם בחישוב מספרי, אולם לצורך המבחן ההבנה האינטואיטיבית עדיפה. MW מבוטא בגרם למול אך כדי לחשב ריכוז, ניתן לכפול את התמיסה בהופכי של MW (כלומר מול חלקי גרם). כמו כן שימו לב שמטעמי נוחות הוחלפו היחידות מ-100ml ל-0.1L.
![]()
כדי לחשב את האוסמולריות אין צורך לכפול את הריכוז שקבלנו, כיון שגלוקוז אינו מתחלק בתמיסה ולכן האוסמולריות של גלוקוז היא הקטנה ביותר:
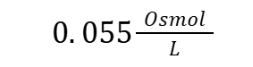
שלילת מסיחים:
א. אוראה כמו גלוקוז אינה מתחלקת לעוד מולקולות ולכן גם אותה לא צריך לכפול אותה בעת חישוב האוסמולריות. ניתן לראות שכיון שהמשקל שלה נמוך פי 3 מאשר של גלוקוז (60=MW), הרבה יותר מולקולות של אוראה יכנסו בתוך גרם אחד ולכן האוסמולריות שלה תהיה גבוהה יותר מאשר של גלוקוז. כאמור עדיפה ההבנה אך נראה זאת גם באמצעות החישוב:
![]()
כעת את הריכוז שקבלנו אין צורך להכפיל כיון שאוראה לא מתחלקת בתמיסה והאוסמולריות שלה:
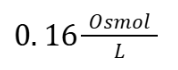
ב. החומר KCl כן מתחלק לשני יונים ולכן צריך לכפול בשניים בעת חישוב האוסמולריות. גם אם לא מחשבים את האוסמולריות, המשקל של KCl נמוך מאוד (4=MW), ולכן גם במקרה זה הרבה יותר מולקולות של KCl יכנסו בתוך גרם אחד. כלומר, האוסמולריות של חומר זה תהיה גבוהה יותר מאשר של גלוקוז. הבא נראה זאת בחישוב:
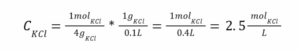
כעת את הריכוז שקבלנו צריך להכפיל פי 2 כיון ש-KCl מתחלקת בתמיסה לשני יונים ולכן האוסמולריות היא:
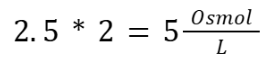
ג. החומר HCl גם הוא מתחלק לשני יונים ולכן גם אותו צריך לכפול בשניים בעת חישוב האוסמולריות. גם אם לא מחשבים את האוסמולריות, המשקל של HCl נמוך מאוד (3=MW), ולכן גם במקרה זה הרבה יותר מולקולות של KCl יכנסו בתוך גרם אחד. כלומר, האוסמולריות של חומר זה תהיה גבוהה יותר מאשר של גלוקוז. בחישוב:
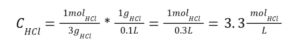
את הריכוז שקבלנו צריך להכפיל פי 2 כיון ש-HCl מתחלקת בתמיסה לשני יונים והאוסמולריות היא:
![]()
להרחבה – Bern & Levy, מהדורה 8 עמודים 12-15 (אוסמוזה).
פיזיולוגיה 1 שאלה 32
מי מהתמיסות הבאות תשמש כטיפול במטופל מיובש שהתייצג עם נוזלי גוף היפרטונים?
במה עוסקת השאלה: שמירה על הומאוסטזיס
תשובה ב’.
אוסמולריות תקינה של נוזלי הגוף סביב 300 מיליאוסמולר. ולכן המטופל התייצג עם נוזלי גוף היפרטונים.
דקסטרוז – תמיסה היפוטונית (דקסטרוז הוא סוכר שמתפרק למים ולפחמן דו חמצני שחדיר את ממברנות מדורי הגוף). מתן תמיסה של דקסטרוז מגדילה את נפח ה-ECF וה-ICF וגורמת לירידה באוסמולריות נוזלי הגוף.
הרחבה על יתר התמיסות בסרטון ‘מדורי המים בגוף’ ובערכי הידע בערך זהה.
שלילת מסיחים –
דקסתרן- תמיסה היפרטונית (סוכר גדול מאוד) שלא חודר את ממברנת הפלסמה. ניתנת במקרה שיש צורך להעלות את נפח הפלזמה בלבד, וגורמת לעלייה באוסמולריות של נוזלי הגוף של המטופל.
נתרן כלוריד 5%- תמיסה היפרטונית שחודרת את ממברנת הפלסמה (אך לא את ממברנת התא) ניתנת במקרה של נוזלי גוף היפוטונים על מנת להעלות את אוסמולריות נוזלי הגוף. גורמת למעבר של נוזלים מה-ICF ל-ECF ובכך להגדלת נפל מדור ה-ECF והקטנת נפח המדור התוך תאי.
מניטול- כאשר מטופל עובר ניתוח מוח או סובל משבץ, לרוב יש הצטברות של נוזל בין רקמתי במוח (בצקת). בגלל קשיחות הגולגולת לא ניתן להגיל את נפח המדור ומתחיל להיווצר לחץ הפוגע בנוירונים. נוזל המוח מופרד משאר הגוף ע”י ה-BBB (blood brain barrier) אשר חדיר למים ולמעט מאוד חומרים נוספים. כאשר ישנה הצטברות נוזלים במוח נרצה להעלות את האוסמולליות של שאר המדורים בגוף, כך שתיווצר זרימה של מים מהמוח החוצה. לצורך כך משתמשים הרופאים במניטול שהינו סוכר שלא חודר לתאים או למוח (אינו חוצה את ה-BBB). המניטול מעלה את האוסמולליות של הנוזל החוץ תאי (לא כולל את סביבת המוח) ומוביל לזרימת מים מהמוח החוצה.
להרחבה – Berne&Levy, מהדורה 8, עמודים 18-22 (מדורי מים בגוף)
פיזיולוגיה 1 שאלה 4
חוקר גילה טרנספורטר (transporter) חדש בחיידק Namibienssis אשר מעביר גם טריפטופן (Tryptophan) וגם גליצין (Glycine) דרך דופן תא החיידק, שניהם באותו כיוון. מה נכון?
תשובה ב. טרנספורטרים ניתנים לשתי סוגי חלוקות (כמעט) בלתי תלויות: חלוקה ראשונה בהתאם לדרישות האנרגטיות (פסיבי, אקטיבי שניוני ואקטיבי ראשוני) וחלוקה שניה בהתאם למנגנון הפעולה (תעלות – חור סלקטיבי בממברנה, נשאים – אנזימים ומשאבות – אנזימים עם פעילות ATPase). בפתרון זה נדון בעיקר בסוג החלוקה הראשון, כלומר בחלוקה על פי דרישות אנרגטיות. תחילה נבדיל בין טרנספורט פסיבי לטרנספורט אקטיבי: טרנספורט פסיבי הוא מעבר של חומר עם המפל האלקטרוכימי שלו, ללא השקעת אנרגיה. טרנספורט פסיבי שמתרחש דרך טרנספורטר מכונה גםfacilitated diffusion (מונח זה מתייחס למעבר פאסיבי דרך כל טרנספורטר, בין אם נשא ובין אם תעלה). טרנספורט אקטיבי דורש השקעת אנרגיה ומחולק לשניים: טרנספורט אקטיבי ראשוני (primary active transport) וטרנספורט אקטיבי שניוני (secondary active transport). טרנספורט אקטיבי ראשוני הוא שימוש בהידרוליזת ATP לצורך העברת חומר מסוים לצד השני של הממברנה כנגד המפל האלקטרוכימי שלו (הטרנספורטרים שמבצעים זאת מכונים גם משאבות). טרנספורט אקטיבי שניוני הוא מעבר שיש בו שימוש במפל ריכוזים של חומר אחר (אשר הושג באמצעות הידרוליזת ATP), לצורך העברת חומר מסוים לצידה השני של הממברנה כנגד המפל האלקטרוכימי שלו.
כעת, מתוך שלושת מנגנוני הפעולה (תעלות, נשאים ומשאבות) נתמקד בנשאים ונעבור על עוד כמה מושגים בסיסיים הנוגעים אליהם. ישנם שלושה מנגנוני העברה של נשאים: יוניפורטר (Uniporter), סימפורטר (co-transporter/symporter) ואנטיפורטר (antiporter). במנגנון מסוג יוניפורטר, נשאים מעבירים מולקולה אחת מצד אחד של הממברנה לצידה השני. נשא מסוג זה תמיד מעביר מולקולות עם המפל האלקטרוכימי שלהן. חשוב להדגיש שהעברה באמצעות יוניפורטר היא אינה העברה אקטיבית ראשונית כיון שיוניפורטר מעביר לפי המפל האלקטרוכימי של המולקולה, כלומר באופן פסיבי. במנגנון סימפורטר נשאים מעבירים בו זמנית מספר מולקולות לאותו הכיוון. נשא מסוג זה תמיד מעביר לפחות מולקולה אחת בניגוד למפל האלקטרוכימי שלה “על חשבון” מולקולה אחרת שנעה עם מפל הריכוזים שלה. במנגנון אנטיפורטר נשאים מעבירים בו זמנים מספר מולקולות אך לכיוונים הפוכים. כמו סימפורטר, נשא מסוג זה תמיד מעביר מולקולה אחת בניגוד למפל האלקטרוכימי שלה.
בשאלה מוצג מצב בו טריפטופן (Tryptophan) וגליצין (Glycine) מועברים דרך דופן התא באותו כיוון. כיון שמדובר בשתי מולקולות שמועברות באותו הכיוון, ניתן להסיק שמדובר בסימפורטר ולא באנטיפורטר או ביוניפורטר. כעת בהסתמך על הידע שלנו אודות העברה אקטיבית שניונית, אנחנו יכולים להסיק שהסיבה שהתא מכניס את שתי המולקולות באותו טרנספורטר, היא שימוש במפל האנרגטי של אחת מן המולקולות בכדי להכניס את המולקולה הנוספת כנגד המפל האלקטרוכימי שלה. סוג כזה של העברה מכונה העברה אקטיבית שניונית.
שלילת מסיחים:
א. הטרנספורטר הוא אכן מסוג סימפורטר אך ההעברה היא העברה אקטיבית שניונית. העברה אקטיבית ראשונית דורשת שימוש ישיר על ידי הטרנספורטר ב-ATP לצורך המעבר. במידה וזה היה המקרה, אין סיבה ששני החומרים יועברו יחדיו דרך אותו טרנספורטר. העובדה שמדובר בשני חומרים שמועברים יחדיו אמורה לרמוז כי מדובר בסימפורטר ובהעברה אקטיבית שניונית.
ג. הטרנספורטר הוא אכן מסוג סימפורטר אך בניגוד לכתוב במסיח יש שימוש באנרגיה בעת ההעברה. כאמור, העובדה שמדובר בשני חומרים שמועברים יחדיו אמורה לרמוז כי מדובר בסימפורטר ובהעברה אקטיבית שניונית. דוגמה להעברה אקטיבית שניונית ע”י סימפורטר היא באמצעות הנשא SGLT1 שמעביר נתרן וגלוקוז מהמעי הדק והכליה, פנימה אל תאי האפיתל. במקרה זה, הסימפורטר משתמש בכוח המניע של נתרן לתוך התא, כדי להכניס גלוקוז כנגד מפל הריכוזים שלו. הריכוז הנמוך של נתרן בתוך התא נשמר על ידי משאבת נתרן-אשלגן, שבעזרת ATP מוציאה נתרן מהתא ומכניסה אשלגן, כנגד מפל הריכוזים של שניהם.
ד. אמנם ההעברה היא אקטיבית שניונית אך הטרנספורטר הוא סימפורטר ולא אנטיפורטר וזאת כיון שהוא מעביר את שתי המולקולות באותו הכיוון, דרך דופן התא, ולא בכיוונים מנוגדים.
פיזיולוגיה 2 שאלה 18
נתונים הנתונים הבאים: Ecl= -30, Ek= -90, ENa=+60. חוקר מעוניין לקבע את מתח הממברנה על מתח שבו כל היונים שחדירים את הממברנה יצאו החוצה מהתא. מה יכול להיות המתח שבו צריך החוקר לקבע את הממברנה?
במה השאלה עוסקת: פוטנציאל אלקטרוכימי
תשובה ד. על מנת להבין את כיוון תנועת היון, יש להשוות בין מתח הממברנה לבין פוטנציאל נרנסט של היון. כל עוד פוטנציאל נרנסט של היון שונה ממתח הממברנה, ליון יש כוח מניע ותנועה נטו לכיוון מסוים. היון “מנסה” להביא את מתח הממברנה לפוטנציאל נרנסט שלו. נעבור על כל התשובות בניסיון להבין מה תהייה כיוון התנועה של כל אחד מהיונים, וניווכח כי לא קיים מתח ממברנה בו תנועת כל היונים תהייה כלפי חוץ התא.
שלילת מסיחים:
א. במידה ומתח הממברנה יקובע על -50mV: פוטנציאל נרנסט של יון הנתרן יהיה גבוהה יותר ממתח הממברנה, ומכיון שנתרן הוא יון חיובי, הוא ייכנס לתא במטרה להביא לדה-פולריזציה ולקרב את מתח הממברנה לפוטנציאל נרנסט שלו. לעומתו, אשלגן יצא מהתא במטרה להביא להיפר-פולריזציה (כיון שהוא טעון חיובית) ולקרב את מתח הממברנה לפוטנציאל שיווי המשקל של אשלגן.
ב. במידה ומתח הממברנה יקובע על -100mV: פוטנציאל נרנסט של אשלגן ושל נתרן יהיה גבוה יותר ממתח הממברנה. כיוון שהם יונים חיוביים, הם ייכנסו אל התא על מנת לגרום לדה-פולריזציה ולקרב את מתח הממברנה לפוטנציאל נרנסט של כל אחד מהם. לעומתם, כלור טעון שלילית ולכן הוא יצא מן התא כדי לגרום לדה-פולריזציה ולקרב את מתח הממברנה לפוטנציאל שיווי המשקל שלו.
ג. במידה ומתח הממברנה יקובע על +80mV: פוטנציאל נרנסט של כלור יהיה נמוך יותר ממתח הממברנה, ומכיוון שכלור טעון שלילי, הוא יכנס אל התא על מנת לגרום להיפר-פוריזציה במטרה לקרב את מתח בממרנה לפוטנציאל נרנסט שלו. נתרן ואשלגן במקרה זה יצאו כיון שפוטנציאלי שיווי המשקל שלהם נמוכים ממתח הממברנה, ובעזיבתם הם למעשה גורמים להיפר-פולריזציה.
להרחבה – Berne& Levy, מהדורה 8, עמודים 22-27 (פוטנציאל הממברנה).
פיזיולוגיה 1 שאלה 34
מה מהבאים אינו מהווה תפקיד של תאי האפיתל?
במה עוסקת השאלה: העברה אפיתלאלית
תשובה ד’. תאי האפיתל מהווים את החוצץ בין הסביבה החיצונית לבין הסביבה הפנימית. תפקידיהם המרכזיים של תאי האפיתל הם להוות מחסום בפני מיקרוארגניזמים, למנוע איבוד מים ולשמור על סביבה פנימית קבועה. את התפקיד האחרון הם מצליחים למלא על ידי תהליכי טרנספורט מבוקרים- העברה וקטוריאלית מצד אחד של תאי האפיתל לצד השני.
להרחבה – Bern & Levy, מהדורה 8 עמודים 27-33 (טרנספורט דרך תאי אפיתל).
פיזיולוגיה 1 שאלה 15
המערכת הבאה מתארת מערכת דונן הנמצאת בש”מ בטמפרטורת החדר (27oC). יוני הנתרן והכלור חדירים דרך הממברנה, ואילו החלבון (P2-) אינו חדיר. מה ריכוז הכלור בתא
A?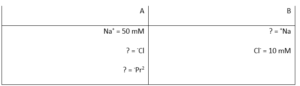
במה השאלה עוסקת: שיווי משקל גיבס דונן
תשובה ד. במערכת גיבס דונן שמתוארת בשאלה ישנם שני מיכלים: מיכל A המכיל חלבונים שאינם חודרים את הממברנה, נתרן וכלור, ומיכל B המכיל נתרן וכלור. נתון לנו שהמערכת נמצאת בשיווי ולכן חשוב לציין שבמקרה זה קיים הפרש אוסמולריות בין התאים, אך לא קיים הפרש מטענים וזאת כיון שכל תא הוא אלקטרוניטרלי (כלומר מכיל את אותה כמות של מטענים חיוביים ושליליים). כלומר, כל תא בנפרד מאוזן מבחינת המטענים, אולם כן יש הבדלי ריכוזים של היונים שבמערכת בין התאים. על פי עקרון האלקטרוניטרליות ניתן להסיק שריכוזו של נתרן במיכל B הוא 10mM. כשמערכת גיבס דונן נמצאת בשיווי משקל, מכפלת שני היונים במיכל A שווה למכפלת שני היונים במיכל B. כלומר ניתן לנסח את המשוואה באופן הבא:
ומכאן ניתן להסיק כי ריכוז כלור הוא כ- 2mM בתא A. כעת נרצה להבין את הדינמיקה בין היונים במערכת שלב אחר שלב. תחילה כלור, שנמצא במכיל B ולא נמצא במיכל A, רוצה לעבור למיכלA בגלל הבדלי ריכוזים. נתרן, בעקבות ההפרש החשמלי שנוצר לאחר מעבר כלור, נע גם הוא ממיכל B למיכל A. אולם, על נתרן פועלים שני כוחות, האחד חשמלי שמושך אותו להיכנס למיכל A והשני נובע מהנתרן שכבר נמצא במיכל A לפני המעבר ומקשה על נתרן נוסף להיכנס. בסופו של דבר המערכת מגיעה לשיווי משקל וריכוז זהה של נתרן וכלור עוברים ממיכל B למיכל A.
שלילת מסיחים:
א. מסיח זה מבלבל כיון שהוא מציג מצב בו ריכוז כלור שווה בשני התאים שזה לכאורה מצב בו כלור נמצא בשיווי משקל. אולם, חשוב להבין את מה שמתואר בפתרון לסעיף ד’, לפיו נתרן שבמיכל A מתנגד לכניסה של נתרן ממיכל B. נתרן חייב לעבור עם כלור ממיכל B למיכל A בגלל עקרון האלקטרוניטרליות. לפיכך, במצב שיווי משקל ריכוז כלור לא יהיה זהה בין שני המיכלים ומיכל B יכיל ריכוז גבוה יותר של כלור.
ב. במערכת גיבס דונן אנו מתחילים עם אניון (למשל כלור) וקטיון (למשל נתרן) בתא מסוים ובתא האחר ישנה מולקולה טעונה שלילית שאינה חודרת את הממברנה (למשל חלבונים) וקטיון זהה לזה שבתא האחר. כלור עובר לעבר התא בו נמצאים החלבונים, ונתרן יחד איתו, עד להגעה לשיווי משקל. בגלל שילוב הכוחות שפועלים על נתרן, כפי שמתואר בסעיף ד, היינו מצפים למצוא ריכוז נמוך יותר של כלור במיכל A, לעומת מיכל B, ולא ריכוז גבוה של 20mM. כמו כן, במידה ובמיכל A היה ריכוז כלור של 20mM לא היה מדובר בשיווי משקל כיון שאין כוח שיתנגד מכלור ונתרן לעבור מתא A לתא B.
ג. אוסמול (Osmol) הוא מדד למספר המומסים בתמיסה ולא לריכוז המולקולה. כך למשל, אם יש מול אחד של מלח (NaCl), יש שני אוסמול חלקיקים כיון שכל מולקולה של NaCl מתפרקת ל-Na ו-Cl. בשאלה נשאלתם על ריכוז כלומר אנחנו מחפשים ערכים של מולר. על אף שבשאלה המולקולה אינה מתפרקת לחלקיקים נוספים, לא ניתן להשתמש באוסמול במקום במולר. להלן רענון היחידות השונות: במולר הכוונה היא מספר מולים לליטר (mol/L), אוסמול (Osmol) היא מספר החלקיקים אליה המולקולה מתפרקת ואוסמולריות היא מספר אוסמול לליטר Osmol/L.
ה. במערכת גיבס דונן אנו מתחילים עם אניון (למשל כלור) וקטיון (למשל נתרן) בתא מסוים ובתא האחר ישנה מולקולה טעונה שלילית שאינה חודרת את הממברנה (למשל חלבונים) וקטיון זהה לזה שבתא האחר. כלור עובר לעבר התא בו נמצאים החלבונים, ונתרן יחד איתו, עד להגעה לשיווי משקל. בגלל שילוב הכוחות שפועלים על נתרן, כפי שמתואר בסעיף ד, היינו מצפים למצוא ריכוז נמוך יותר של כלור במיכל A, לעומת מיכל B, ולא ריכוז גבוה של 50mM. כמו כן, במידה ובמיכל A היה ריכוז כלור של 50mM לא היה מדובר בשיווי משקל כיון שאין כוח שיתנגד מכלור ונתרן לעבור מתא A לתא B.
להרחבה – Bern & Levy, מהדורה 8 עמודים 10-12 (דיפוזיה).
מומלץ לקרוא על מערכת גיבס דונן בספר הקורס שנמצא באתר ולקריאה נוספת ניתן לקרוא מהמקורות המצוינים שנמצאים בספריה של אוניברסיטת תל אביב. Bern & Levy אינם המקור המועדף בנושא זה.
Aidley, David J. The Physiology of Excitable Cells. Cambridge University Press, 1998. pp. 26-28
Sperelakis, Nicholas. Cell Physiology Sourcebook: A Molecular Approach. Gulf Professional Publishing, 2001. pp. 243-246.
פיזיולוגיה 1 שאלה 26
מה מנגנון הפעילות של הנשא NHE-1 הנמצא בכל תא בגוף?
במה עוסקת השאלה: טרנספורט ממברנלי
תשובה ג’. הנשא NHE-1 הוא אנטיפורטר הנמצא בכל תאי הגוף ומכניס יון נתרן במקביל להוצאת פרוטון . האנרגיה לפעילותו מגיעה ממפל הריכוזים של הנתרן שנוצר בעזרת פעילות משאבת הנתרן אשלגן הדורשת ATP. הנשא משחק תפקיד חשוב בקביעת ה-PH בתוך התא.
להרחבה – Berne & Levy, מהדורה 8, עמוד 7, 26-27
פיזיולוגיה 1 שאלה 35
מי מהבאים אינו מהווה מנגנון דרכו הקפילרות יכולות להעביר מים?
במה עוסקת השאלה: מעבר נוזלים בין מדורי נוזל בגוף
תשובה ג’. מעבר מים ומומסים בין הנימים (קפילרות) משתנה בהתאם לסוג האיבר. למשל בכבד ישנם נימים בעלי רווחים גדולים המכונים discontinuous capillary, דרכם מים ואלמנטים תאיים יכולים לעבור. בכליה למשל יש נימים בעלי חרירים המכונים fenestrations בקוטר של 80-100 nm ובמוח ישנו מחסום המאפשר מעבר של מים, יונים ומולקולות הקטנות מ-4 nm. בנוסף תאי האנדותל המרכיבים את הנימים מכניסים מים באמצעות פינוציטוזה.
להרחבה – Berne & Levy Physiology, מהדורה 8, עמודים 19-20
פיזיולוגיה 4 שאלה 4
תא דם אדום הוכנס לתמיסת אוריאה איזואוסמוטית. אוריאה חוצה ממברנה בקלות. מה מהבאים יתרחש?
במה השאלה עוסקת: אוסמוזה
תשובה ג. תא דם אדום הוכנס לתמיסה איזואוסמוטית של אוראה. כיון שקיימים טרנספורטרים לאוראה בדופן התא, אוראה תיכנס בעקבות מפל הריכוזים שלה. לאחר כניסת אוראה מים יכנסו כדי להשוות את האוסמולריות התאית לזו שמחוץ לתא. למעשה, כניסת האוראה העלתה את אוסמולריות התא וכניסת המים נועדה להשוות בין חוץ ותוך התא. אולם, לאחר כניסת המים ריכוז האוראה בתוך התא יורד כיון שלמעשה האוראה “נמהלה” בכך שמים נכנסו לתוך התא. לפיכך, אוראה נוספת נכנסת לתא במטרה להשוות את ריכוז האוראה משני הצדדים והמעגל הזה ממשיך בכניסה נוספת של מים ואוראה עד שהתא מתפוצץ.
שאלה נוספת שנרצה לענות עליה היא מדוע מים עוברים אחרי אוראה אם היא אינה מומס אפקטיבי. מומס אפקטיבי הוא מומס שאינו חודר את הממברנה ולכן יוצר לחץ אוסמוטי וכן המושג טוניות מתייחס רק לריכוז המומסים האפקטיביים בתמיסה. התשובה לכך היא שאוראה אמנם אינה מומס אפקטיבי אבל הפרשי הריכוזים שלה הופכים את התנועה שלה לחד כיוונית, כלומר לתוך התא ולא החוצה ממנו. למעשה, אפשר לחשב על זה כאילו מפל הריכוזים של אוראה הופך אותה להיות מומס בלתי חדיר. לסיכום, למרות שאוריאה היא (בהגדרה) מומס לא אפקטיבי, היא יכולה להוביל לאוסמוזה במצבים כמו אלו המתוארים מעלה.
שלילת מסיחים:
א. נפח התא יגדל וזה בגלל מפל הריכוזים של אוראה וכן בגלל קיומם של טרנספורטרים לאוראה בדופן התא. במידה ולא היו טרנספורטרים לאוראה, נפח התא לא היה משתנה כיון שפנים וחוץ התא הינם איזואוסמוטיים. חשוב לציין שבשונה מהכתוב במסיח, בשאלה זו מדובר באיזואוסמוטיות (ולא באיזוטוניות) וזה כיון שאוראה יכולה להיכנס לתוך התא, בעוד שבטוניות המומס אינו יכול לחדור את הממברנה ומתייחסים רק לתנועת מים.
ב. מסיח זה שגוי משני היבטים. תחילה התא כן חדיר לאוראה וזהו נתון שמצוי בשאלה. שנית, במידה והתא לא היה חדיר לאוראה, הוא לא היה מתכווץ כי פנים וחוץ התא הם איזואוסמוטים, ולכן לא תהיה תנועה של מים.
ד. ההגעה לשיווי משקל לא תתרחש כיון שאוראה תמשיך להיכנס ובכך לגרום להגדלת אוסמולריות התא שתוביל לכניסת מים ולהקטנת ריכוז אוראה בתא וחוזר חלילה. תא דם יכול לגדול בערך עד פי 1.5 מגודלו ולכן בנקודה מסוימת בתהליך זה הוא יתפוצץ.
להרחבה – Bern & Levy, מהדורה 8 עמודים 12-13 (אוסמוזה).
פיזיולוגיה 4 שאלה 5
מדוע כדוריות דם אדומות מתנפחות כאשר מקררים אותן ל-4 מעלות צלזיוס?
במה השאלה עוסקת: שמירה על נפח תאים בתנאים איזוטונים
תשובה ד’. השאלה הזאת מציגה לנו את החשיבות של משאבת נתרן אשלגן בשמירת נפח התא בסביבה איזוטונית. במידה ואנחנו מצננים את התמיסה, הקצב המטבולי של התא יורד כיון שאנזימים פועלים לאט יותר בקור ולכן מיוצר פחות ATP בתא. כלומר, יש פחות ייצור אנרגיה בתא ויש פחות ATP זמין למשאבת נתרן/אשלגן. כאשר המשאבה פועלת לאט יותר, ריכוזי המומסים משתנים והדבר משפיע גם על תנועת המים. כתוצאה מכך התאים מתנפחים בגלל אפקט דונן שהחלבונים התוך תאיים גורמים לו. למדנו שעל מנת שהתאים לא יתפוצצו, הם פיתחו שיטה להגן על עצמם והיא לא להיות חדירים לנתרן ובכך לשמור על ריכוז מומסים גבוה מחוץ לתא (אפקט גיבס דונן כפול). נתרן חדיר קצת לתא ולכן במצב תקין, המעט נתרן שכן מצליח להיכנס יוצא החוצה על ידי המשאבה. כיון שהמשאבה פעילה פחות, מים יכנו לתא בעקבות תנועת נתרן והתאים מתנפחים.
להרחבה – Bern & Levy, מהדורה 8, עמ’ 25, Isotonic Cell Volume Regulation.
פיזיולוגיה 4 שאלה 39
נתונה ממברנה החדירה ליון מסוים אשר ריכוזו מחוץ לתא גבוה מריכוזו בתוך התא, כמתואר באיור למטה. איזו עקומה מבין העקומות הבאות מתארות את שטף היון לתוך התא כתלות בזמן?
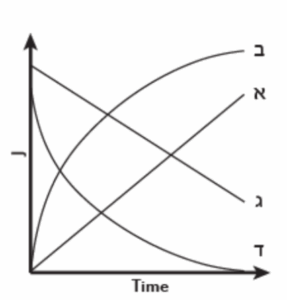
במה השאלה עוסקת: שטף דרך ממברנה
תשובה ד. בשאלה זו נתון יון הנמצא משני צדדיה של ממברנת התא, כאשר ריכוזו מחוץ לתא גבוה מריכוזו בתוך התא. כלומר, יש לו מפל ריכוזים שכיוונו פנימה לתוך התא. כעת נשאלתם איזו מן העקומות מתארת בצורה טובה יותר את שטף המולקולה. כזכור שטף תלוי במפל הריכוזים לפי הנוסחה הבאה: 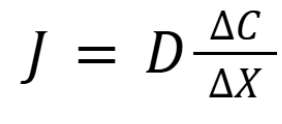
ואכן הפרמטר היחידי שמשתנה במערכת הזו לאורך זמן הוא מפל הריכוזים. הסיבה לכך היא שהיון חודר את הממברנה ולמעשה מקטין את מפל הריכוזים לאורך זמן וזה יגרום גם להקטנה של השטף. לפיכך כבר בנקודה זו ניתן לבודד שתי עקומות מתוך השאלה שהן ג’ ו-ד’ פשוט כיון ששתיהן מראות מגמת ירידה של השטף לאורך זמן כפי שאנו מצפים לראות. כעת ננסה להבין מדוע דווקא עקומה ד’ היא הנכונה ולשם כך ניעזר בחוק השני של פיק. החוק השני של פיק מתאר את השינוי במפל הריכוזים כפונקציה של זמן. על פי החוק הראשון של פיק, השטף תלוי במפל הריכוזים כך שככל שמפל הריכוזים גדל כך גדל גם השטף. מאידך, השטף עצמו מקטין את מפל הריכוזים שמניע אותו, ועל כן ככל שעובר הזמן כך השטף קטן, כי הריכוזים בשני המדורים משתווים בהדרגה. בהתחלה מפל הריכוזים הוא הכי גדול ובהתאמה גם השטף הוא הכי גדול, אולם לקראת ההגעה לשיווי משקל, כמעט ואין תנועה של היון והשטף איטי יותר כפועל יוצא של מפל הריכוזים שקטן.
שלילת מסיחים:
א. עקומה זו מציגה עליה של השטף לאורך זמן. מגמה זו בעייתית כיון שמפל הריכוזים קטן ככל שיותר יונים חוצים את הממברנה, וככל שמפל הריכוזים קטן השטף גם הוא קטן.
ב. עקומה זו מציגה עליה של השטף לאורך זמן. מגמה זו בעייתית כיון שמפל הריכוזים קטן ככל שיותר יונים חוצים את הממברנה, וככל שמפל הריכוזים קטן השטף גם הוא קטן.
ג. עקומה זו מציגה מגמה נכונה של ירידה בשטף לאורך זמן, אך המגמה הינה ליניארית וזאת בניגוד למה שהיינו מצפים לראות במצב זה. הסיבה לכך כאמור היא שהשטף תלוי במפל הריכוזים אך גם משפיע עליו. כאשר השטף מקטין את מפל הריכוזים הוא למעשה גם מקטין את עצמו.
להרחבה – Bern & Levy, מהדורה 8 עמודים 6-8 (מכניזם של טרנספורט ממברנלי); 10-11 (דיפוזיה).
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: דיפוזיה, טרנספורט ממברנלי
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1
פיזיולוגיה 4 שאלה 33
נתונות ארבעת תמיסות שונות של 0.1% אחוז משקלי- תמיסת אוראה, (Mw=60 ) תמיסת ,NaCl (Mw=58 ) תמיסת CaCl2 (Mw=110 ) ותמיסת גלוקוז (Mw=180 ) .מי מבין התמיסות היא בעלת האוסמולריות הגדולה ביותר?
במה השאלה עוסקת: אוסמולריות
תשובה ב. תמיסה המכילה 0.1% משקלי מכילה 0.1g ב-100ml או לחילופין 1g ב-1L. בשאלה זו אנו מחפשים את התמיסה בעלת האוסמולריות הגבוהה ביותר. כלומר, חומר “שיכנס” הכי הרבה פעמים בתוך גרם אחד. לפיכך, נחפש את החומר הקל ביותר וכן זה שמתפרק להכי הרבה אטומים. ניתן לראות שנתרן עונה על כל הקטגוריות האלו.
הבא ננסה לראות זאת גם באופן חישובי:
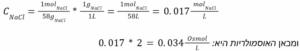
שלילת מסיחים:
א. אוראה כבדה יותר מ-NaCl ולכן תפיק אוסמולריות נמוכה יותר כיון שהיא נכנסת פחות פעמים בגרם אחד. כמו כן היא אינה מתפרקת בתמיסה. כאמור נראה זאת בחישוב:
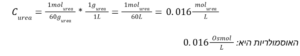
ג. CaCl2 הוא חומר שניתן להתבלבל בו בקביעת האוסמולריות כיון שהוא מתחלק לשלושה יונים שונים. תחילה נראה חישובית מדוע האוסמולריות נמוכה יותר מאשר של NaCl ואז נראה כיצד יכולנו לדעת זאת ללא חישוב.

ניתן לראות שהאוסמולריות נמוכה מאשר מאשר של NaCl וכאמור אנו מחפשים את האוסמולריות הגבוהה ביותר. לאחר שראינו זאת נרצה לדעת כיצד לענות על השאלה בלי חישוב. כיון שבחישוב האוסמולריות אנו כופלים את הריכוז פי מספר החלקיקים, ניתן בתור חישוב תיאורטי בראש או על הנייר, לחלק מראש את המסה המולקולרית במספר החלקיקים. כלומר אם היינו מחלקים את המשקל של NaCl פי 2 היינו מקבלים משקל של 29 g/mol ואם היינו מחלקים את CaCl2 היינו מקבלים 36.6 g/mol. כפי שטענו, ככל שהמשקל של החומר קטן יותר, כך האוסמולריות הסופית גדולה יותר. באופן זה, אנחנו עוקפים את כל החישוב ורואים כיצד הפירוק לחלקיקים ישפיע על האוסמולריות.
ד. גלוקוז היא המולקולה הכבדה ביותר ולכן תניב את האוסמולריות הקטנה ביותר. בכל זאת נציג את החישוב:
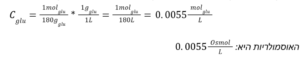
להרחבה – Bern & Levy, מהדורה 8 עמודים 12-16 (אוסמוזה).
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: אוסמוזה, אוסמולליות, אוסמולריות וטוניות
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1
פיזיולוגיה 4 שאלה 21
לפניך תיאור סכימטי של נפח תאי דם אדומים לאור זמן לאחר שבזמן 0 הרחיפו 1 מ”ל דם בליטר של תמיסות שונות. התאם את התמיסות הבאות לעקומה המתארת באופן הטוב ביותר את השתנות נפחה של כדורית דם אדומה:
1. 600 mOsmol Urea
2. 0.8% NaCl
3. 300 mOsmol Urea
4. 220 mMOL NaCl
5. 0.7% NaCl + 1/3 M Urea
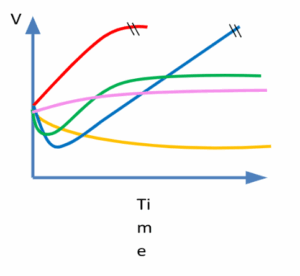
במה השאלה עוסקת: אוסמוזה ותמיסות בשימוש קליני
תשובה ד .
כחול
סגול
אדום
כתום
ירוק
1. כחול. מבחינה אוסמולרית- היפראוסמוטית. טוניות- היפוטונית. לכן התוצאה הסופית- כניסה של אוריאה, כניסה של מים ופיצוץ התא. עם זאת, תחילה יש כמה מילישניות בהן האוריאה עדיין לא נכנסה בדיפוזיה פשוטה בהן המים, שנעים מהר יותר- יצאו החוצה מהתא אל עבר המדור בעל ריכוז המומסים הגדול יותר. אך מיד עם כניסת האוראה לתא- מים יכנסו והתא יתפוצץ.
2. סגול. תמיסה היפואוסמוטית והיפוטונית. מים ינועו לעבר המדור עם הלחץ האוסמוטי הגבוה יותר- שזה המדור התוך תאי. ולכן נפח התא יגדל קצת ויתייצב על נפח גבוה יותר (0.8%) זו תמיסה לא רחוקה מאיזוטונית.
3. אדום. אמנם איזואוסמוטית אבל היפוטונית ולכן מים יכנסו לתוך התא עד כדי פיצוץ. אין את השלב ההתחלתי בו מים יצאו החוצה כיוון שהתמיסה איזואוסמוטית ולא היפראוסמוטית.
4. כתום. קודם בנוגע ליחידות- נתון במולר ואנחנו צריכים להמיר לאוסמולר (נכפול פי 2). 440 אוסמולר. תמיסה היפארוסמוטית והיפרטונית. מים יצאו החוצה מהתא והתא ייתכווץ.
5. ירוק. תמיסה היפראוסמוטית והיפוטונית. מכיוון שהיא היפראוסמוטית- שוב, עד שהאוריאה תכנס מים יצאו החוצה ונפח התא ייקטן. לאחר מכן, האוריאה תכנס לתוך התא ואחריה מים. הפעם לא עד כדי פיצוץ כי יש הגנה אוסמוטית כלשהי- תמיסת 0.7% nacl שהוא מומס אפקטיבי (אבל עדיין היפוטוני). ולכן התוצאה הסופית תהייה גדילה קלה בנפח התא.
נשים לב כי על מנת לענות על השאלה יש להמיר את יחידות האוראה ממולר (M) למיליאוסמולר-
נזכור כי 1M=1000mM ולכן-
1\3M= 330mM= 330 mOsmol
להרחבה – Berne and Levy, Physiology , מהדורה 8, עמודים 12-16.
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: אוסמוזה, אוסמולליות, אוסמולריות וטוניות
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1
פיזיולוגיה 1 שאלה 2
כיצד יושפע הנוזל התוך תאי מהוספה של תמיסה היפרטונית לפלסמה? הנח כי האוסמלליות המקורית של הפלסמה הינה 300 mOsm /Kg.
במה השאלה עוסקת: טוניות ומדורי המים בגוף
תשובה א. מדורי המים בגוף מחולקים לשניים, תוך התא וחוץ התא ויחד הם מהווים כ-60% ממשקל הגוף. המדור החוץ תאי מחולק גם הוא לשני תת מדורים, הפלסמה (plasma) והנוזל הבין רקמתי (interstitial fluid). תתי המדורים במדור החוץ תאי מופרדים על ידי קירות מערכת הדם שחדירות ליונים ומולקולות קטנות ואינן חדירות לחלבונים. כעת, כדי לענות על השאלה נזכר במשמעות המושג טוניות. טוניות היא מדד לריכוז מומסים אפקטיביים בתמיסה, כלומר מומסים שאינם חוצים את הממברנה. זהו מונח השוואתי בין שתי תמיסות שונות. תמיסות איזוטוניות הן תמיסות עם אותה כמות מומסים אפקטיביים, תמיסה היפרטונית היא תמיסה עם יותר מומסים אפקטיביים ביחס לתמיסה אחרת ותמיסה היפוטונית היא תמיסה עם פחות מומסים אפקטיביים ביחס לתמיסה אחרת. מונח נוסף שחשוב להבינו בהקשר לשאלה הוא אוסמולליות. אומולליות היא מדד לריכוז המומסים בתמיסה, כלומר מספר המומסים (אוסמול) בק”ג אחד של ממס.
בשאלה הוכנסה לפלסמה תמיסה היפרטונית, כלומר תמיסה שמכילה יותר מומסים אפקטיביים ביחס לערכים נורמליים בתא. כיון שהפלסמה והנוזל הבין רקמתי מופרדים ע”י קרום חדיר, ניתן לייחס לכל הנוזל החוץ תאי אוסמולליות זהה כמו לפלסמה, כלומר גבוהה יותר מפנים התא. בשלב הבא, כיון שחוץ התא היפרטוני ביחס לתוך התא מים ינועו מתוך התא החוצה בכדי להגיע לשיווי משקל. תנועה זו של המים תוריד את ערכי האוסמולליות במדור החוץ תאי ותעלה את ערכי האוסמולליות במדור התוך תאי. חשוב לציין שהתנועה מתבצעת ע”י מים ולא ע”י המומס כיון שמדובר במומסים אפקטיביים שלא יכולים לחצות את הממברנה. כמו כן מעבר המים מתוך התא החוצה, יגרום לתא לאבד מנפחו. לפיכך יציאת המים מובילה לשתי תוצאות: הקטנת נפח הפלסמה והגדל האוסמולליות.
שלילת מסיחים:
ב. בשאלה מוצג מצב בו לפלסמה מוזרקת תמיסה היפרטונית, קרי בעלת ריכוז מומסים אפקטיביים גבוה יותר ביחס לתוך התא. מצב כזה מחייב את התא להוציא מים והוצאה זו תגרום להקטנת נפחו. בכדי שנפח המדור התוך תאי יגדל, יש להכניס לפזמה תמיסה היפוטונית, קרי תמיסה בעלת ריכוז מומסים אפקטיביים נמוך ביחס לתוך התא. במצב זה מים יכנסו לתוך התא וזאת בכדי להפוך את התמיסות לתמיסות איזוטוניות.
ג. האוסמולליות התוך תאית תקטן במידה ותוכנס תמיסה היפוטונית לפלסמה, כלומר תמיסה בעלת ריכוז נמוך יותר של מומסים אפקטיביים. במצב זה, מים יכנסו לתא בכדי להפוך את התמיסות לאיזוטוניות. הכניסה של המים לתוך התא תגרום לתוך התא להקטין את האוסמולליות שלו, אולם זה לא המצב המתואר בשאלה.
ד. כפי מתואר בתשובה לסעיף א’, האוסמולליות תגדל וזאת באמצעות הוצאה של מים מהתא. יחד עם זאת, הוצאת המים מהתא תגרום לתא לאבד מנפחו, כלומר ההפך ממה שכתוב במסיח זה.
להרחבה – Bern & Levy, מהדורה 8 עמודים 12-16 (אוסמוזה); 19-22 (מדורי המים בגוף).
פיזיולוגיה 1 שאלה 11
מה נכון לגבי אוסמולריות (Osmolarity) ואוסמולליות (Osmolality)?
במה השאלה עוסקת: אוסמוזה, אוסמולריות, אוסמולליות ולחץ אוסמוטי
תשובה א. כדי לענות על שאלה זו נתחיל בלהכיר מונח בסיסי יותר והוא אוסמול (osmol). אוסמול הוא יחידת מידה למספר המומסים בתמיסה. כך למשל, אם יש מול אחד של מלח (NaCl), יש שני אוסמול חלקיקים כיון שכל מולקולה של NaCl מתפרקת ל-Na ו-Cl בתמיסה מימית. אוסמולליות היא מדד לריכוז המומסים בתמיסה, כלומר מספר המומסים (אוסמול) בק”ג אחד של ממס. אוסמולריות היא מספר המומסים (אוסמול) בליטר אחד של ממס. אוסמולליות היא מדד יותר מדויק כיון שנפח משתנה בהתאם לטמפרטורה בעוד מסה אינה משתנה. למשל בטמפרטורה גבוהה, אוסמולריות התמיסה עלולה לרדת (מכיוון שנפח התמיסה גדל) אך האוסמולליות תישאר אותו דבר (מכיוון שמסת התמיסה לא השתנה) .
אוסמוזה היא מעבר מים ממקום בו הלחץ האוסמוטי נמוך למקום בו הלחץ האוסמוטי גבוה. חשוב להבדיל בין לחץ אוסמוטי ובין אוסמולריות ואוסמולליות. תחילה כיון שהם מודדים דברים שונים, לחץ אוסמוטי מודד את מידת הלחץ שמופעל על הממברנה על ידי המומסים הבלתי חדירים. אוסמולריות ואוסמולליות הם מדדים לריכוז המומסים בתמיסה. סיבה נוספת להבחנה בין המונחים היא שלחץ אוסמוטי נוצר על ידי מומסים שאינם חודרים את הממברנה (מומסים אפקטיביים), בעוד אוסמולריות ואוסמולליות מודדים את כלל המומסים, ללא הבחנה אם הם חודרים או שאינם חודירם את ממברנת התא.
שלילת מסיחים:
ב. אוסמולריות אומדת את ריכוז החלקיקים ב-1 ליטר של ממס.
ג. אוסמולליות אומדת את ריכוז החלקיקים ב-1 ק”ג של ממס.
ד. כאמור קיים הבדל בין שני המונחים כפי המתואר בתשובה לסעיף א’.
פיזיולוגיה 1 שאלה 20
מה לא ניתן לבדוק על ידי בדיקת דם פשוטה?
במה השאלה עוסקת: מדורי המים בגוף
תשובה ב. חשוב לזכור כי קיים מעבר מים חופשי בין מדורי הגוף השונים, האוסמולליות של כל המדורים תהייה זהה. מכאן, ניתן יהיה להעריך את אוסמולליות הנוזל התוך תאי על ידי בדיקת האוסמולליות של הפלזמה. מכיוון שמעבר המים הוא חופשי, ניתן לומר שהתמיסות בכל המדורים הן איזוטוניות אחת ביחס לשנייה. עם זאת, הרכב המומסים בפלזמה הוא שונה מזה שבתוך התא וזאת כתוצאה מכך שהממברנה של התא היא בררנית ולא מאפשרת מעבר של ישיר של חומרים דרכה.
שלילת מסיחים:
א. מכיוון שמדורי הגוף איזוטונים אחד ביחס לשני, אוסמולליות הנוזל התוך תאי זהה לאוסמולליות הפלזמה.
ג. ריכוז המומסים שאינם חדירים (האפקטיביים) שווה בכל אחד מהמדורים. מכאן שריכוז החלבונים שאינם חדרירים בתוך התאים יהיה שווה לריכוזים בפלזמה. אחרת, יהיה מעבר של מים אל עבר המדור בעל הלחץ האוסמוטי הגדול יותר עד שהמצב יגיע לשיווי משקל וריכוזם יתאזנו.
ד. מכיוון שמדורי הגוף איזוטונים אחד ביחס לשני, אוסמולליות הנוזל התוך תאי זהה לאוסמולליות המדור הבין תאי.
להרחבה – Bern & Levy, מהדורה 8 עמודים 18-22 (מדורי המים בגוף).
פיזיולוגיה 1 שאלה 23
מטופל הגיע למיון עקב אירוע מוחי. הרופאים במיון חששו כי בעקבות האירוע יצטברו נוזלים בחלל המוח ותיווצר בצקת מסכנת חיים. איזה עירוי על הרופאים לתת למטופל על מנת למנוע ככל הניתן את מצב זה?
במה השאלה עוסקת: תמיסות בשימוש קליני
תשובה א. שבץ מוחי פעמים רבות מלווה בהצטברות נוזלים בחלל המוח והתנפחות של נוירונים. בצקת מוחית יכולה לגרום ללחץ תוך גולגולתי, לפגוע בתפקוד הנוירונים ולגרום אף למוות או קומה. על מנת למנוע מצב זה משתמשים בתמיסת Manitol. מניטול אינו חודר את ה-BBB, כך שהוא מהווה אוסמוליט אפקטיבי, והוא יעלה את הלחץ האוסמוטי בגוף ויגרום למעבר של מים באוסמוזה מתוך חלל המוח.
שלילת מסיחים:
ב. Dextran היא מולקולה בעלת משקל מולקולרי גבוהה, והיא אינה חוצה את תאי האנדותל ונשארת בפלזמה. ניתן להשתמש בתמיסה זו כאשר רוצים להעלות, למשל את האוסמולריות של הפלזמה.
ג. Dexterose הינו סוכר המתפרק במים לפחמן דו חמצני ולמים ועל כן אינו מייצר לחץ אוסמוטי כלל. תמיסת דקסטרוז בכל האחוזים המשקליים תהייה תמיסה היפוטונית ותגרור כניסת מים לתאים.
ד. תמיסת סליין היא תמיסה איזוטונית של נתרן כלוריד שאינה משנה את מאזן האוסמולריות במדורי הגוף ולא גוררת תנועה של מים נטו לאף כיוון.
להרחבה – Bern & Levy, מהדורה 8 עמודים 19-22 (משק המים בגוף); 22 (In The Clinic).
פיזיולוגיה 4 שאלה 26
חייל התייבש במהלך אימון. בכדי להתאושש על החובש להגדיל את נפח הפלמסה של החייל. לשם כך החליט החובש לתת עירוי של תמיסה היפוטונית. מה סביר שיקרה?
במה השאלה עוסקת: התייבשות ומדורי המים בגוף
תשובה ג. כדי לענות על שאלה זו נזכר בכמה רעיונות ומושגים. מדורי המים בגוף מחולקים לשניים, תוך התא וחוץ התא. המדור החוץ תאי מחולק גם הוא לשני תת מדורים, הפלסמה (plasma) והנוזל הבין רקמתי (interstitial fluid). תתי המדורים במדור החוץ תאי מופרדים על ידי קירות מערכת הדם שחדירות ליונים ומולקולות קטנות ואינן חדירות לחלבונים. כעת, כדי לענות על השאלה נזכר במשמעות המושג טוניות. טוניות היא מדד לריכוז מומסים אפקטיביים בתמיסה, כלומר מומסים שאינם חוצים את הממברנה. זהו מונח השוואתי בין שתי תמיסות שונות. תמיסות איזוטוניות הן תמיסות עם אותה כמות מומסים אפקטיביים, תמיסה היפרטונית היא תמיסה עם יותר מומסים אפקטיביים ביחס לתמיסה אחרת ותמיסה היפוטונית היא תמיסה עם פחות מומסים אפקטיביים ביחס לתמיסה אחרת.
כעת ננסה לתאר מה יקרה כאשר החובש נתן עירוי של תמיסה היפוטונית לחייל. תמיסה היפוטונית היא תמיסה עם פחות מומסים אפקטיביים ביחס לפלסמה ולכן כאשר החייל יקבל אותה, הטוניות של הפלסמה שלו תפחת. עקב החדירות הגדולה יחסית של כלי הדם למים ומולקולות קטנות הנוזל הבין רקמתי יהפוך גם הוא היפוטוני ביחס לתוך התא. כלומר, כרגע כלל חוץ התא הוא היפוטוני לתוך התא ודבר זה יגרום לתנועה של מים לתוך התאים וזאת כדי להגיע למצב ששני האזורים הם איזוטונים אחד לשני. כזכור מים עוברים מתמיסה עם אוסמולליות נמוכה לתמיסה עם אוסמולליות גבוהה ולכן הם יעברו מחוץ התא פנימה.
כעת ננסה להבין מדוע החובש יעלה למשפט. כדי לטפל בהתייבשות החובש היה צריך להעלות את נפח הדם, אולם כאשר הוא נתן תמיסה היפוטונית הוא העלה את נפח הדם לזמן קצר בלבד כיון שהמים עזבו את הדם ונכנסו לתאים. לכן, במקרה זה היה עדיף לתת תמיסה איזוטונית ובכך לספק למטופל את הנוזלים שהוא איבד ולהעלות את נפח הדם.
שלילת מסיחים:
א. העירוי לא יפצה על אובדן הנוזלים כיון שהם יעזבו את הפלסמה ויכנסו לתאים כפי שמתואר בתשובה לסעיף ג’.
ב. מים נעים מתמיסה היפוטונית לתמיסה היפרטונית או במילים אחרות, מתמיסה עם ריכוז מומסים אפקטיביים קטן יותר אל עבר תמיסה עם ריכוז מומסים אפקטיביים גדול יותר. כיון שהפכנו את חוץ התא להיפוטוני ביחס לתוך התא, מים יכנסו לתוך התאים ולא יצאו מהם.
ד. אוסמולריות היא מדד לריכוז המומסים בתמיסה, כלומר מספר המומסים (אוסמול) בליטר אחד של ממס. כיון שמים יכנסו לתאים, האוסמולריות התוך תאית דווקא תרד וזאת כיון שהגדלנו את כמות הממס (מים) ולא שינינו את כמות המומסים.
להרחבה – Bern & Levy, מהדורה 8 עמודים 12-16 (אוסמוזה); 18-22 (מדורי המים בגוף).
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: אוסמוזה, אוסמולליות, אוסמולריות וטוניות. בנוסף – מדורי המים בגוף
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1, 2
פיזיולוגיה 1 שאלה 22
איזה תהליך יפגע כתוצאה ישירה מהמוטציה הנקודתית בעמדה 508 של החלבון במחלת ה-Cystic Fibrosis?
במה השאלה עוסקת: מחלת ה-Cystic Fibrosis
תשובה ג’. במחלת הציסטיק פיברוזיס קיימת מוטצית מחיקה של חומצת האמינו פניל-אלנין בעמדה 508, בגן המקודד ל-CFTR (Cystic fibrosis transmembrane conductance regulator). החלבון הואABC טרנספורטר המתפקד כתעלת כלור ואחראי על בקרה על טרנספורטרים נוספים. בשל קיפול שגוי נמנעת ההגעה שלו לממברנה. כל הולכת היונים בתא נפגעת- לא מייצרים מוקוזה בריאות, בעיית ספיגה ממערכת העיכול, עקרות, זיהומי ריאות חוזרים, זיעה מלוחה (הכלור לא נספג).
להרחבה – Bern & Levy, מהדורה 8 עמוד 8 (ציסטיק פיברוזיס).
פיזיולוגיה 4 שאלה 23
נתון תא אפיתל בטובול הפרוקסימלי של הכליה, כמתואר באיור למטה. בצד האפיקלי יש סימפורטר נתרן-ביקרבונט. בצד הבאזולטרלי יש משאבת נתרן-אשלגן ותעלת ביקרבונט. בעקבות מעבר המומסים מהצד האפיקלי לצד הבאזולטרלי, מים וכלור עוברים גם כן אל הצד הבאזולטרלי. מה מבין הבאים נכון?
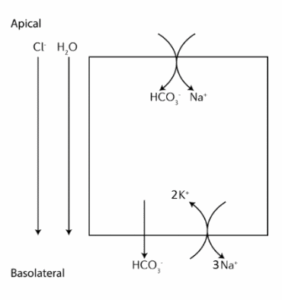
במה השאלה עוסקת: העברה אפיתליאלית
תשובה ג. מומסים יכולים לחצות את תא האפיתל באופן טרנסצלולרי או פאראצלולרי. מעבר טרסצלולרי דורש ביטוי של נשאים על גבי הממברנות של תאי האפיתל ובאופן זה מומסים נכנסים לתא ויוצאים ממנו בצידו השני. לדוגמה בכליה, נתרן צריך להיספג חזרה לתוך מחזור הדם, לאחר שהוא עבר סינון. הנתרן נכנס באופן פסיבי מהצד של הממברנה האפיקלית וזאת עקב הריכוז הנמוך שלו בתא שגורם למפל ריכוזים. לעומת זאת, המעבר חזרה למחזור הדם בצד הבאזולטרלי של תא האפיתל דורש אנרגיה עקב הריכוז הגבוה של נתרן בדם. תהליך זה כולו מוגדר כתהליך אקטיבי וזאת על אף שרק בצד אחד של תא האפיתל הגוף השתמש באנרגיה. מעבר פאראצלולרי הינו מעבר פסיבי של מומסים דרך ה-tight junctions של תאי האפיתל שבחלק מהמקרים חדירים למומסים מסוימים. חשוב לציין שבסוג העברה זה אין ביטוי של נשאים לצורך מעבר המומסים.
בשאלה זו נתרן וביקרבונט עוברים באופן טרנסצלולארי ומעבר זה גורר אחריו מעבר של מים. כעת, כיון שמים עברו מהצד האפיקלי לבאזולטרלי, ריכוז כלור גדל כי כמות הממס, דהיינו מים, פחתה. נוצר הפרש ריכוזים של כלור בין הממברנה האפיקלית לבזולטרלית שגורם לכלור לעבור לצד הבזולטרלי כדי להפחית את ריכוזו בצד האפיקלי ולאזן את הבדלי הריכוזים.
שלילת מסיחים:
א. נתרן וביקרבונט אכן עוברים באופן טרנסצלולרי, אך כלור עובר באופן פאראצלולרי ולכן מסיח זה נפסל.
ב. משאבת נתרן אשלגן אכן יוצרת מפל חשמלי בכך שהיא מכניסה 2 יוני אשלגן ומוציאה 3 יוני נתרן ובכך הופכת את תוך התא לשלילי יותר. אולם במקרה זה ניתן לראות שביקרבונט הטעון שלילית מפצה על המפל החשמלי בכך שהוא יוצא מהתא.
ד. המונח solvent drag (גרירת מומס) מתואר במסיח זה באופן הפוך ממשמעותו. גרירת מומס מתייחסת למעבר של מומס בעקבות תנועת מים באופן שהמומס בעצם נסחף עם המים. במסיח מוצג כי המים עוברים בעקבות כלור, כלומר הפוך ממשמעות המונח גרירת מומס.
להרחבה – Bern & Levy, מהדורה 8 עמודים 27-33 (טרנספורט דרך תאי אפיתל).
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: העברה אפיתליאלית
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 2
פיזיולוגיה 1 שאלה 24
הקטנה של איזה מהערכים הבאים תקטין את השטף של CO2 החוצה מן התא?
במה השאלה עוסקת: דיפוזיה דרך ממברנה
תשובה ה. נתונה משוואת הדיפוזיה: 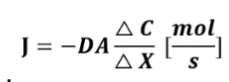
ככלל, הקטנת ערך שנמצא במונה או הגדלת ערך שנמצא במכנה במשוואה, תגרום להקטנת שטף הדיפוזיה הכולל. אותה נקודה נכונה גם למשוואת מקדם הדיפוזיה: 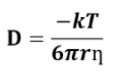
שהינה חלק ממשואת הדיפוזיה. בחלק שלילת המסיחים נבין מדוע כל מסיח אינו נכון.
שלילת מסיחים:
א. פחמן דו חמצני הינה מולקולה סימטרית וללא מטען חשמלי כלל. מסיבה זו פחמן דו חמצני חוצה את ממברנת התא בדיפוזיה פשוטה בקלות יתרה. ככלל, ככל שהמולקולה פחות טעונה היא דווקא תחצה את הממברנה בקלות יותר ושטף הדיפוזיה דרך הממברנה יגדל.
ב. הקטנת ריכוז הפחמן הדו חמצני מחוץ לתא, תגדיל את הכוח המניע של המולקולה לצאת החוצה מהתא וזאת על מנת להשוות את מפל הריכוזים. כלומר, יצירת C△ – מפל ריכוזים שיגרור שטף גדול יותר של פחמן דו חמצני לחוץ התא.
ג. הקטנת עובי הממברנה תקטין את ה-X△ במשוואת שטף הדיפוזיה. כלומר, יקטן המרחק אותו המולקולה צריכה לעבור ובעקבות כך יגדל השטף של הפחמן הדו חמצני לחוץ התא.
ד. הצמיגות (אתא) נמצאת במכנה במשוואת שטף הדיפוזיה (בתוך מקדם הדיפוזיה). הקטנת הצמיגות תקל על המולקולות לנוע במדיום ותגדיל את שטף הדיפוזיה.
להרחבה – Bern & Levy, מהדורה 8 עמודים 10-12 (דיפוזיה).
פיזיולוגיה 1 שאלה 19
מה הלחץ האוסמוטי של תמיסה בעלת M5 גז מתאן ו- M2 קלציום כלוריד בהינתן כי מכפלת קבוע הגזים בטמפרטורה שווה ל-25?
במה השאלה עוסקת: משוואת הלחץ האוסמוטי
תשובה ג’. נשתמש במשוואת הלחץ האוסמוטי: כאשר:
n – מספר החלקיקים המסיסים במולקולה (למשל עבור CaCl מדבור בשלושה). נקרא גם המקדם הסטויכיומטרי
C – ריכוז המולקולה [mol / L].
R – קבוע הגזים [L * atm / (K * mol] 8.205*102. לא צריך לזכור את הערך הממשי.
T – טמפרטורה בקלווין [T(K)].
נתמקד בפתרון רק בכלציום כלוריד ולא במתאן כיון שגזים חודרים את הממברנה ולכן אינם יוצרים לחץ אוסמוטי. כלציום כלוריד היא מולקולה המתפרקת בתמיסה לשלושה חלקיקים (2 יוני כלור ויון סידן) ולכן המקדם הסטויכומטרי הוא 3. נכפיל את מקדם הסטויכומטרי בריכוז הנתון ובמכפלת קבוע הגזים בטמפרטורה לפי הנוסחה: π=3x2x25=150.
להרחבה – Bern & Levy, מהדורה 8 עמודים 12-16 (אוסמוזה).
פיזיולוגיה 1 שאלה 1
תמיסת סליין 0.9% NaCl מכילה 150 mmol/Kg של NaCl. מה האוסמולליות של התמיסה בהינתן ש-NaCl אינו עובר פירוק מלא בתמיסה (n = 1.5)?
תשובה ג. אוסמול (osmol) היא יחידת מידה למספר המומסים בתמיסה. כך למשל, אם יש מול אחד של מלח (NaCl), יש שני אוסמול חלקיקים כיון שכל מולקולה של NaCl מתפרקת ל-Na ו-Cl. אוסמולליות היא מדד לריכוז המומסים בתמיסה, כלומר מספר המומסים (אוסמול) בק”ג אחד של ממס. לצורך התזכורת, אוסמולריות היא מספר המומסים (אוסמול) בליטר אחד של ממס. אוסמולליות היא מדד יותר מדויק כיון שנפח משתנה בהתאם לטמפרטורה בעוד מסה אינה משתנה. בהמשך הפתרון נתמקד רק באוסמולליות כיון שעליה נשאלתם. במידה ומולקולה אינה מתפרקת בתמיסה לשתי מולקולות (או יותר), מידת האוסמולליות שלה פרופורציונאלית לריכוזה בק”ג אחד של ממס. כאשר מולקולה מתפרקת באופן חלקי ניתן לכפול את מידת הפירוק שלה (במקרה שלנו 1.5) בריכוז שלה, כדי לקבל את מידת האוסמולליות. בשאלה זו החישוב נעשה כך:
כלומר, מידת האוסמולליות של התמיסה בשאלה זו היא 225mOsmol/Kg. חשוב לציין בהקשר לשאלה זו שאוסמולריות ואוסמולליות מתייחסות לכלל המומסים בתמיסה, בעוד שכאשר אנו מדברים על לחץ אוסמוטי, אנו מתייחסים למומסים שאינם חדירים את הממברנה. מומסים כאלו אפקטיביים ביצירת לחץ אוסמוטי ולכן שמם הוא מומסים אפקטיביים.
להרחבה – Bern & Levy, מהדורה 8 עמודים 12-16 (אוסמוזה).
פיזיולוגיה 4 שאלה 37
בתאים יש חלבונים אשר לא חוצים ממברנה ויונים המשפיעים על תנועת המים לתוך התא והחוצה (אפקט גיבס-דונאן). איך תאים מתמודדים עם הבעיה הזאת?
במה השאלה עוסקת: אפקט דונאן כפול
תשובה א’. מערכת גיבס-דונן מטרתה להסביר כיצד נוצר הפרש מתחים מצידי הממברנה. במערכת גיבס-דונן ישנם שני תאים המופרדים בממברנה, כאשר תא אחד מכיל מומס טעון שאינו חדיר דרך הממברנה. חוסר חדירות המומס גוררת תנועת מומסים נוספים כך שבסוף נוצר הפרש מטענים על גבי הממברנה.
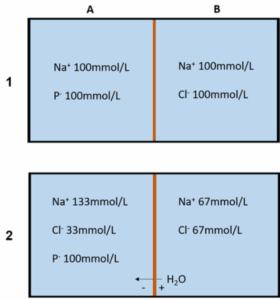
בתמונה מתואר המצב ההתחלתי בו שתי תמיסות מופרדות ע”י ממברנה החדירה לנתרן, כלור ומים, אך אינה חדירה לחלבון (P-). אוסמולריות תמיסה A זהה לזו של תמיסה B. לאחר שנמתין זמן מה, יתרחשו התנועות הבאות: כלור יעבור בדיפוזיה מתמיסה B לתמיסה A במורד מפל הריכוזים שלו ← דיפוזיה זו גורמת לתמיסה A להיות טעונה שלילית ביחס לתמיסה B (ראה מתח ממברנה בעמוד 31) ← הכלור יוצר הפרש מתחים הגורם לנתרן לעבור בדיפוזיה מתמיסה B לתמיסה A ← עובר אותו מספר מולקולות נתרן כמו מולקולות הכלור שעברו, שכן מטרת הנתרן היא לסתור את המטענים השליליים של הכלור ← הגענו ל-“שיווי משקל גיבס-דונן”. נשים לב כי בשיווי משקל זה ישנו הפרש אוסמולריות בין התמיסות. הפרש האוסמולריות בין המדורים יוצר לחץ אוסמוטי המושך מים מתמיסה B ל-A, אך במערכת המתוארת תנועת המים לא מתאפשרת כיוון שהמיכלים כבר מלאים. מה קורה במערכת ביולוגית בה אחד המיכלים הוא הנוזל התוך תאי? במקרה כזה כן מתאפשרת כניסת מים כיוון שדפנות התא גמישות. עקב כניסת המים לתמיסה A (תוך התא) ריכוז הכלור יורד, כלור כבר אינו בשיווי משקל ולכן כלור נוסף עובר מתמיסה B. בעקבות הכלור הנוסף שעבר יעברו שוב נתרן ומים וחוזר חלילה. תהליך זה גורם להצטברות מומסים ומים בצורה לא שוויונית, דבר שיכול לסכן את התאים. הפתרון לבעיה זו טמון בחוסר החדירות של נתרן, במה שנקרא “אפקט דונן כפול” (double Donnan). כל מעגל תנועת המומסים והמים התחיל כי במדור A יש אניון בלתי חדיר. אפקט דונן כפול מתבסס על העובדה כי יוני נתרן כמעט ואינם חודרים את ממברנת התא וגם המעט שכן מצליח להיכנס לתא מיד מוצא החוצה על ידי משאבת הנתרן-אשלגן. כלומר בפועל הנתרן הוא קטיון בלתי חדיר. אם כן, כיצד יראה האפקט כאשר הממברנה אינה חדירה לנתרן: כלור עבר בדיפוזיה מתמיסה B לתמיסה A במורד מפל הריכוזים שלו ← דיפוזיה זו גורמת לתמיסה A להיות טעונה שלילית ביחס לתמיסה B ← הכלור יוצר הפרש מתחים, פנים התא שלילי יותר מהחוץ ← נתרן רוצה להיכנס אבל הוא הוא לא יכול. התהליך נעצר והתוצאה היא מתח ממברנה ששווה לפוטנציאל שיווי משקל של כלור (ראו בהמשך).
להרחבה- Bern & Levy מהדורה 8 עמוד 25
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: מערכת גיבס דונאן
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 2
פיזיולוגיה 1 שאלה 13
נתון תא אפיתל מסוים שעל גביו משאבות נתרן-אשלגן ותעלות אשלגן בצד הבאזולטרלי, ותעלות נתרן בצד האפיקלי. נתרן נכנס לתוך התא בהתאם למפל האלקטרוכימי שלו. אין תעלות נוספות על גבי הממברנה מעבר לאלו המצויינות. בתא זה כלור עובר מהצד האפיקלי לצד הבאזולטרלי במנגנון פארא-צלולארי (paracellular). מה עשוי להיות נכון אודות מערכת זו?
במה השאלה עוסקת: העברה טרנסצלולארית ופאראצלולארית
תשובה א. בתאי אפיתל יש טרנספורטרים שונים בכל צד וטרנספורטרים אלו קובעים את הפרשי המתח בין הממברנה האפיקלית והבאזולטרלית. הסיבה לכך היא שהם מכניסים או חוסמים את כניסתם של יונים מסוימים שהם היוצרים של מטען חשמלי בממברנה. בשאלה מוצג מצב סטנדרטי בתא אפיתל בו בצד האפיקלי יש תעלות נתרן ובצד הבאזולטרלי יש משאבות נתרן-אשלגן ותעלות אשלגן. תעלות נתרן בצד האפיקלי מלמדות על כך שקיים גרדיאנט של נתרן לתוך התא. הגרדיאנט הוא לתוך התא כיון שריכוז הנתרן בתא נשמר נמוך מאוד. תאי אפיתל שמבטאים תעלות נתרן בצד האפיקלי קיימים למשל בכליה ובמעי ומטרתם לספוג מחדש נתרן בכדי שלא יופרש. לאחד כניסתו של נתרן לתא, משאבת נתרן אשלגן מוציאה אותו לצד הבאזולטרלי בעזרת אנרגיה מ-ATP. סוג כזה של מעבר, שחוצה את הממברנה האפיקלית ואת הממברנה הבאזולטרלית, מכונה מעבר טרנסצלולארי (trnascellular).
כאשר נתרן עובר לצד הבאזולטרלי נוצר הפרש מתחים בין הממברנות והסיבה לכך היא שמטען חיובי עזב את הממברנה האפיקלית ועבר לממברנה הבאזולטרלית. כלומר, הממברנה האפיקלית היא כעת שלילית יותר ביחס לממברנה הבאזולטרלית. חשוב לציין שהפרש מתחים נמדד בדרך כלל בין שני צדי הממברנה, אולם במקרה זה בו מודדים שתי ממברנות, משווים בין חוץ התא של כל ממברנה. הפרש המתחים גורם לכלור לעבור גם הוא את שתי הממברנות וזאת כדי לאזן את הפרש המטענים שנוצר. האופן שבו כלור עובר הוא פאראצלולארי (paracellular). במעבר מסוג זה חומרים אינם עוברים דרך ממברנות התא, אלא דרך חלבונים שנמצאים במרווחים שבתאי האפיתל ומכונים tight junctions. מעבר פאראצלולארי הוא תמיד מעבר פסיבי, כלומר עם המפל האלקטרוכימי של החומר.
שלילת מסיחים:
ב. בשאלה, כלור עובר בעקבות נתרן והסיבה לכך היא שנתרן גורם להפרש מטענים משני צדי הממברנה. הפרש המטענים יוצר עבור כלור כוח מניע חשמלי שמושך אותו לעבור באופן פאראצלולארי.
ג. הממברנה האפיקלית שלילית יותר מהממברנה הבאזולטרלית וזאת עקב מעבר נתרן לצדו השני של תא האפיתל. כאשר מטען חיובי עוזב את הממברנה האפיקלית הוא למעשה הופך אותה לשלילית יותר וכמו כן כאשר הוא עובר לממברנה הבאזולטרלית הוא הופך אותה לחיובית יותר.
ד. רקמת אפיתל מפרישה היא רקמה שמוציאה חומר מהתא דרך הממברנה האפיקלית. לדוגמה, במקרה של מערכת הכלייה, הNaCl- שיצא מהתא יופרש בשתן. תהליך זה הוא אינו מה שמוצג בשאלה כיון שבשאלה מוצג תרחיש בו יש כניסה של נתרן לתוך התא (מהצד האפיקלי). תהליך זה מכונה ספיגה כיון שהוא מונע הפרשה של נתרן ומחזיר אותו לתוך הגוף. דוגמה למכניזם בו מתרחשת הפרשה היא העברה של כלור מהצד הבאזולטרלי אל עבר הצד האפיקלי באופן טרנסצלולארי. לאחר המעבר נתרן עוקב אחרי כלור, אך הפעם הוא זה שעובר באופן פאראצלולארי ו-NaCl מופרש מהגוף.
פיזיולוגיה 4 שאלה 36
הגדלת כל הפרמטרים הבאים תשפיע על שטף הדיפוזיה (J) דרך ממברנה באותו האופן. מיהו היוצא דופן?
במה השאלה עוסקת: דיפוזיה
תשובה ב. שאלה זו למעשה בוחנת כיצד הגדלת פרמטרים שונים במערכת משפיעה על הדיפוזיה וכדי לענות עליה נחזור למשוואות הרלוונטיות. קצב דיפוזיה (שטף) של מולקולה בתמיסה מתואר בחוק הראשון של פיק, והוא קובע כי קצב הדיפוזיה פרופורציונאלי להפרש הריכוזים. ניתן לראות זאת במשוואה עצמה:
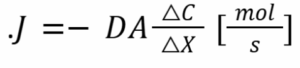
בנוסחה D הוא מקדם הדיפוזיה, C△ הוא הפרש ריכוזים ו-X△ מרחק הדיפוזיה (במקרה שלנו, עובי הממברנה). משוואה זו מתחשבת בשטח הפנים (A) וחשוב לשים לב שהדבר משפיע גם על היחידות של השטף שהן [mol/s] ביחס למשוואה ללא שטח פנים בה היחידות הן [mol/m^2s]. ניתן לראות על פי המשוואה שהגדלת שטח הפנים תגרום להגדלת הדיפוזיה. אפשר להבין נקודה זו גם באופן אינטואיטיבי, ככל שהשטח דרכו חומר עובר גדול יותר, יותר חומר יכול לעבור בכל נקודת זמן. בחלק שלילת מסיחים נראה מדוע כל שאר המסיחים גורמים להקטנת השטף.
שלילת המסיחים
הגדלת המרחק על פניו מתבצעת הדיפוזיה תקטין את השטף וניתן לראות זאת בבירור במשוואת הדיפוזיה: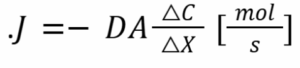 המרחק ממוקם במכנה ככה שככל שהמרחק גדל (לצורך עניינו מדובר בעובי הממברנה) השטף קטן.
המרחק ממוקם במכנה ככה שככל שהמרחק גדל (לצורך עניינו מדובר בעובי הממברנה) השטף קטן.
ג. צמיגות המדיום תקטין גם היא את השטף וניתן להבין זאת גם אינטואיטיבית – יותר קשה לחומר לעבור בג’ל מאשר מטווח מימי. בנוסחה זו מבוטא במקדם הדיפוזיה, D, שעל פי נוסחאת Stokes-Einstein איבר זה מחושב באופן הבא: D=-kT/6πrƞ כאשרk הוא קבוע בולצמן, T מייצג טמפרטורה בקלווין, r רדיוס המולקולה ו- ƞ צמיגיות המדיום. גם במקרה זה הצמיגות ממוקמת במכנה ולכן ככל שהיא תגדל כך השטף יקטן.
ד. ככל שחומר מסיס יותר במים הדבר יפגע ביכולת שלו לעבור דרך ממברנה שהיא תווך שומני ולפיכך יוריד גם כן את השטף.
להרחבה – Bern & Levy, מהדורה 8 עמודים 10-11(דיפוזיה).
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: דיפוזיה
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1
פיזיולוגיה 4 שאלה 28
מהו יחס הריכוזים שצריך להיות על מנת לשמור על מתח הממברנה בדוגמא, בהינתן שהממברנה חדירה ליוני אשלגן בלבד? נתונה משוואת נרנסט:
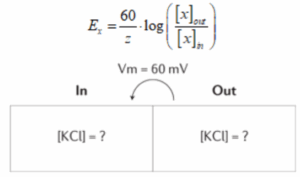
במה השאלה עוסקת: מתח הממברנה
תשובה ב. מתח הממברנה תלוי רק ביונים שחודרים את הממברנה. אפשר לראות זאת גם במשוואת ה-chord conductance שמחשבת את מתח הממברנה:
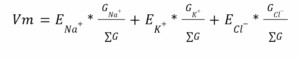
משוואה זו מוצגת כפי שאתם מכירים אותה והיא מציגה את היונים העיקריים בתא. אולם, בשאלה זו נתונה מערכת עם אשלגן וכלור בלבד ולכן נוריד את נתרן מהמשוואה. כמו כן כיון שהחדירות של כלור הינה 0, נציב זאת באיבר המתאים ונראה שלמעשה מתח הממברנה נקבע רק על פי אשלגן בשאלה זו.
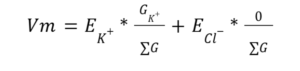
כלומר המשוואה נראית בצורה הבאה:
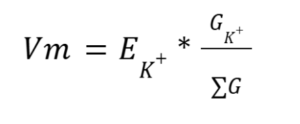
חשוב לציין שבמידה והייתה חדירות חלקית לכלור היינו מתחשבים בכלור במשוואה, אך הוא אינו חודר את הממברנה כלל. כמו כן המשוואה נועדה לעזור לכם להבין את החומר, אך ניתן לפתור שאלה זו גם ללא המשואה באמצעות ההבנה שרק היונים שחודרים את הממברנה (חדירות מלאה או חלקית) משפיעים על מתח הממברנה.
כעת נתון לנו כי מתח הממברנה הוא 60 והשאלה היא מהם ריכוזי האשלגן הנחוצים כדי להגיע לתוצאה זו. כדי לענות על כך הפעם נצטרך להשתמש במשואת נרנסט הנתונה בשאלה:
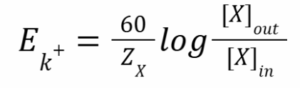
כאמור ידוע לנו שרק אשלגן קובע את מתח הממברנה, ולכן נחפש את ריכוזי אשלגן שיובילו לכך שמתח הממברנה יהיה שווה 60mv. נעשה זאת באותה משוואה איתה עצרנו מספר שורות למעלה:
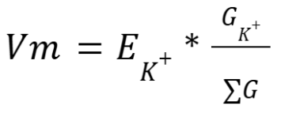
במקרה זה המוליכות אינה רלוונטית כיון שהאשלגן הוא היון היחידי החדיר במערכת והמוליכות שלו היא 1. נשלב כעת את משוואת נרנסט ומשוואת מתח הממברנה ונקבל:
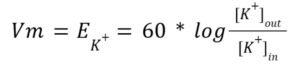
ניתן לראות שבכדי שמתח הממברנה יהיה 60mv, כל איבר ה-log צריך להיות שווה ל-1. מצב זה מתרחש כאשר ריכוז אשלגן בחוץ גבוה פי 10 מאשר ריכוזו בפנים. כלומר נקבל:
![]()
המהלך האחרון בפתרון זה הוא להבין שריכוז הכלור יהיה זהה לריכוז האשלגן. למעשה נקודה זו מסתמך על עקרון האלקטרוניטרליות שלפיו המטענים יהיו מאוזנים בשני המדורים. לפיכך, התשובה הנכונה היא שריכוז כלור מחוץ התא יהיה גדול פי 10 מריכוזו בתוך התא.
שלילת מסיחים:
א. נציב ערך זה במשוואה שקובעת את מתח הממברנה ונראה כיצד זה ישפיע על מתח הממברנה.
![]()
ניתן לראות שמסיח זה לא עונה על השאלה, כיון שאנו מחפשים שמתח הממברנה ישאר ב-60mv.
ג. נציב ערך זה במשוואה שקובעת את מתח הממברנה ונראה כיצד זה ישפיע על מתח הממברנה.
![]()
ניתן לראות שמסיח זה לא עונה על השאלה, כיון שאנו מחפשים שמתח הממברנה ישאר ב-60mv.
ד. נציב ערך זה במשוואה שקובעת את מתח הממברנה ונראה כיצד זה ישפיע על מתח הממברנה.
![]()
ניתן לראות שמסיח זה לא עונה על השאלה, כיון שאנו מחפשים שמתח הממברנה ישאר ב-60mv.
להרחבה – Berne & Levy, מהדורה 8, עמודים 11-12 (גרדיאנט אלקטרוכימי);22-27 (פוטנציאל הממברנה).
נושא: פיזיולוגיה תת נושא: הומאוסטזיס, נוירוביולוגיה תת-תת נושא: פוטנציאל אלקטרוכימי, מתח הממברנה במנוחה ועקומת זרם מתח
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1, 2
פיזיולוגיה 4 שאלה 41
תא דם אדום הועבר מתמיסה איזוטונית (תמיסה א’) לתמיסה היפרטונית (תמיסה ב’) ובחזרה לתמיסה א’. מה צפוי שיקרה?
במה השאלה עוסקת: טוניות
תשובה ג. כדי לענות על השאלה תחילה ניזכר במושג טוניות. טוניות היא מדד לריכוז מומסים אפקטיביים בתמיסה, כלומר מומסים שאינם חוצים את הממברנה. זהו מונח השוואתי בין שתי תמיסות שונות. תמיסות איזוטוניות הן תמיסות עם אותה כמות מומסים אפקטיביים, תמיסה היפרטונית היא תמיסה עם יותר מומסים אפקטיביים ביחס לתמיסה אחרת ותמיסה היפוטונית היא תמיסה עם פחות מומסים אפקטיביים ביחס לתמיסה אחרת. בשאלה זו התא היה בתמיסה איזוטונית, כלומר עם אותה כמות מומסים אפקטיביים ולכן נפח התא לא השתנה. התא מועבר לתמיסה היפרטונית, וכיוון שהמומסים הינם מומסים אפקטיביים, הם אינם חוצים את הממברנה, ומים חוצים את הממברנה בכדי להשוות ערכי אוסמולריות ולהפוך את התמיסה לאיזוטונית. כיוון המים הוא החוצה מהתא כיון שמחוץ לתא יש יותר מומסים (תמיסה היפרטונית) והמים “מוהלים” את אותם מומסים ולמעשה מורידים את האוסמולריות של התמיסה החיצונית. לאחר יציאת מים, התא והתמיסה החיצונית איזוטוניים והאוסמולריות של התא גדלה ונפחו קטן. בשלב הבא התא מוחזר לתמיסה א’, שהייתה איזוטונית בתחילת הניסוי אך כעת היא היפוטונית לתא. הסיבה לכך היא שתמיסה א’ הייתה איזוטונית לתא באוסמולריות מסוימת, אך לאחר החשיפה לתמיסה היפרטונית, אוסמולריות התא עלתה עקב יציאת מים. כעת, כדי שהתא ותמיסה א’ יהיו איזוטוניים, מים נכנסים לתא ומשווים את ערכי האוסמולריות שלו ושל הסביבה החיצונית. כניסת המים מעלה את נפחו של התא והוא חוזר לערך האוסמולרי המקורי מתחילת הניסוי.
שלילת מסיחים:
א. התא אכן יתכווץ לאחר המעבר לתמיסה ב’, אך בחזרה לתמיסה א’ הוא יתנפח כיון שהאוסמולריות שלו השתנתה בזמן שהיה בתמיסה ב’. אמנם התמיסה הייתה איזוטונית לתא בתחילת הניסוי אך הוא עבר מניפולציה שגרמה לו לעליה באוסמולריות.
ב. לאחר המעבר לתמיסה ב’ התא יתכווץ ולא יתנפח. תמיסה ב’ היא היפרטונית לתא ולכן התא יוציא מים בכדי להשוות ערכי אוסמולריות והוצאת המים תגרום לכווצו.
ד. התא אכן יתכווץ לאחר המעבר לתמיסה ב’, אך בחזרה לתמיסה א’ הוא יתנפח ולא יתכווץ יותר. תמיסה א’ היא היפוטונית ביחס לתמיסה ב’ לפי ההגדרה, ולכן לא ייתכן שהחזרה לתמיסה א’ תהווה עבור התא סביבה אף יותר היפרטונית מתמיסה ב’ ועל כן מסיח זה נפסל.
להרחבה – Bern & Levy, מהדורה 8 עמודים 12-16 (אוסמוזה).
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא:אוסמוזה, אוסמולליות, אוסמולריות וטוניות
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1
פיזיולוגיה 4 שאלה 25
בטמפרטורה של 37ºC ניתן לפשט את משוואת נרנסט כמתואר למטה. נתון תא ובו שני יונים, אחד חיובי ואחד שלילי. ממברנת התא חדירה לשני היונים בצורה שווה והמתח שלה בזמן מנוחה הוא-61.5mV . הניחו כי מתח השיווי משקל של הקטיון הוא חיובי. מה מבין הבאים נכון?
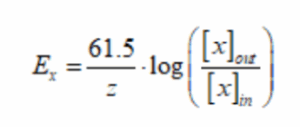
במה השאלה עוסקת: פוטנציאל שיווי משקל
תשובה ד. בתא זה ישנם שני יונים, קטיון ואניון, שחוצים את הממברנה וחדירותם שווה. מתח הממברנה מושפע מפוטנציאל שיווי המשקל של היונים החדירים בלבד וכן ממידת החדירות שלהם. נתון לנו שפוטנציאל שיווי המשקל של הקטיון הינו חיובי ולכן על פי משוואת נרנסט אפשר לטעון שריכוזו של הקטיון גבוה מחוץ לתא מאשר תוך התא. הסיבה לכך היא שבמידה וריכוז הקטיון היה גבוה יותר בתוך התא היינו מקבלים ערך שלילי של איבר ה-log ומכך גם פוטנציאל שיווי משקל שלילי. כדי לענות על שאלה זו חשוב לזכור את תוצאות החישוב של log. כאשר מנת הריכוזים במשוואת נרנסט היא מעל 1, תוצאת ה-Log תהיה חיובית, כאשר המנה שווה ל-1, התוצאה תהיה 0 וכאשר היא קטנה מ-1, התוצאה תהיה שלילית. מצורפת משוואת נרנסט:
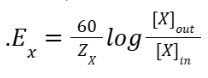
כעת נעבור לבחון מדוע גם ריכוזו של האניון גבוה יותר מחוץ לתא. ידוע לנו שמתח הממברנה הוא שלילי, כ–61.5mv. כמו כן, טענו בתחילת הפתרון שמתח הממברנה נקבע ע”י שני היונים החדירים. לפיכך, אנחנו יכולים להניח שפוטנציאל שיווי המשקל של האניון הוא בהכרח שלילי כיון שהוא צריך למשוך את מתח הממברנה לערך שבו היא נמצאת, כלומר -61.5mv.
שלילת מסיחים:
א. במידה וריכוז האניון מחוץ לתא היה נמוך מריכוזו בתוך התא, היינו מקבלים תוצאה שלילית בחישוב הלוגריתם. תוצאה זו שמוכפלת במטען השלילי של האניון (ZX במשוואת נרנסט הכתובה מעלה) תוביל לפוטנציאל שיווי משקל חיובי. פוטנציאל שיווי משקל חיובי של האניון אינו אפשרי כיון שאחד היונים צריך למשוך את מתח הממברנה לערך שלילי. כיון שנתון שפוטנציאל שיווי המשקל של הקטיון הוא חיובי, האפשרות היחידה היא שהפוטנציאל שיווי המשקל של האניון יהיה שלילי.
ב. כפי שראינו בתשובה לסעיף ד’ נתון לנו שפוטנציאל שיווי המשקל של הקטיון הינו חיובי. לכן על פי משוואת נרנסט בהכרח ריכוזו של הקטיון גבוה מחוץ לתא ביחס לתוך התא.
ג. במידה וריכוז האניון היה שווה בין חוץ התא ותוך התא, מנת הריכוזים שלהם הייתה 1 והחישוב הבא יתקבל:
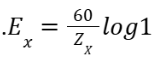
תוצאה של חישוב זה היא 0 ותוצאה זו אינה אפשרית כיון שהאניון צריך למשוך את מתח הממברנה לערך השלילי שבו היא נמצאת.
להרחבה – Berne & Levy, מהדורה 8, עמודים 11-12 (גרדיאנט אלקטרוכימי); 23-27 (פוטנציאל הממברנה).
נושא: פיזיולוגיה תת נושא: הומאוסטזיס, נוירוביולוגיה תת-תת נושא: פוטנציאל אלקטרוכימי, מתח הממברנה במנוחה ועקומת זרם מתח
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1, 2
פיזיולוגיה 4 שאלה 1
מה נכון בנוגע לכוחות הפועלים על מים בכלי הדם?
במה השאלה עוסקת: מעבר מים בין מדורי הגוף
תשובה ב. מים יכולים לעבור בחופשיות בין מדורי הגוף השונים, כאשר שני כוחות מניעים אותם: לחץ אוסמוטי/אונקוטי ולחץ הידרוסטטי. לחץ הידרוסטטי, בהקשר למערכת הקרדיווסקולרית, מתייחס לכוח שמפעילה הפלזמה על קירות כלי הדם. לחץ הידרוסטטי זה מונח מאד חשוב “לחיים האמיתיים” כאשר מדברים על מעבר מים אל ומתוך הנימים, אך פחות למבחן ידע היות ובמצב התקין אין הבדל בלחץ ההידרוסטטי בין שני צדי ממברנת התא. בהתאם, הגורם העיקרי למעבר מים בין תוך התא לחוץ התא זה הלחץ האוסמוטי. יחד עם זאת בשאלה זו נשאלתם על מעבר מים דרך נימים ולא דרך תא בודד וניתן לענות עליה על פי העקרונות שאנו מכירים. נתאר כעת את הכוחות העיקריים הפועלים על המים בנימים ובכך נבין מדוע סעיף זה נכון. הלחץ ההידרוסטטי בתוך הנימים בהתחלה חזק מאוד ומתגבר על הלחץ האוסמוטי בכלי הדם ולכן מים עוזבים את התא. ככל שמים יוצאים מהתא הלחץ ההידרוסטטי בכלי הדם קטן והלחץ האוסמוטי שבכלי הדם גובר עליו וגורם למים להיכנס לקפילרה. לפיכך בצד הורידי של הנימים, הלחץ האוסמוטי הגבוה מתגבר על הלחץ ההידרוסטטי וגורם לכניסת מים לתוך הנימים.
שלילת מסיחים:
א. תחילה כדאי לזכור שהתווך הבין רקמתי מפריד את נוזל הפלסמה מתוך התא. כעת נבין את השוני בין לחץ הידרוסטטי לבין לחץ אוסמוטי בהקשר של תנועת המים. לחץ אוסמוטי גבוה במדור מסוים גורם לכניסה של מים לאותו מדור, בעוד לחץ הידרוסטטי גבוה במדור מסוים גורם ליציאה של מים ממדור זה. לפיכך, לחץ הידרוסטטי גבוה בתווך הבין רקמתי יוביל לדחיפה של מים לנימים ולא למשיכה של מים לתווך הבין רקמתי.
ג. כפי שהוסבר במסיח א’, לחץ הידרוסטטי גבוה גורם ליציאה של מים מאותו מדור. לכן, לחץ הידרוסטטי גבוה בנימים יוביל ליציאה של מים מהנימים ולא לכניסתם.
ד. לחץ אוסמוטי גבוה בתווך הבין רקמתי יגרום למים להיכנס לתווך זה בעקבות הפרשי לחצים, ולא לצאת ממנו.
להרחבה – Bern & Levy, מהדורה 8 פרק 2 (מדורי המים בגוף).
פיזיולוגיה 4 שאלה 3
מה יכול להסביר את העובדה שחומר עובר דיפוזיה איטית בנוזל הפסלמה, אך דיפוזיה מהירה דרך ממברנת התא?
במה השאלה עוסקת: דיפוזיה
תשובה א’. ניזכר במשוואת הדיפוזיה המלאה-
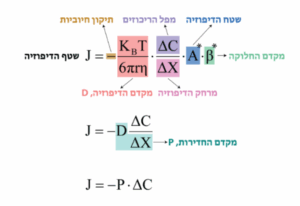
ניתן לראות כי דיפוזיה דרך ממברנה מתרחשת מהר יותר (וביחס לינארי) במקרים הבאים:
ככל ששטח הפנים דרכו מתבצעת הדיפוזיה גדול יותר (במקרה של דיפוזיה דרך ממברנה).
ככל שמפל הריכוזים משני צדי הממברנה חד יותר.
ככל שהטמפרטורה גבוהה יותר.
ככל שמקדם החלוקה של המולקולה גדול יותר (במקרה שך דיפוזיה דרך ממברנה. מקדם החלוקה = מסיסות החומר בשמן לעומת מסיסות החומר במים).
ככל שמרחק הדיפוזיה קטן יותר (במקרה של דיפוזיה דרך מממברנה- ככך שעובי הממברנה קטן יותר).
ככל שהמדיום פחות צמיגי.
ככל שהמולקולה יותר קטנה.
אנו מוסיפים את הפרטמטרים A ו-B למשוואת שטף הדיפוזיה רק כאשר אנחנו מודדים דיפוזיה דרך ממברנה. בהחלט ייתכן כי חומר יעבור דיפוזיה איטית יותר שלא דרך ממברנה, אך מכיוון שהוא יתמוסס טוב בשמן (בעל מקם חלוקה גבוה), הוא יחצה את הממברנה בקלות ומהירות הדיפוזיה שלו דרך ממברנה תהייה מהירה יותר.
שלילת מסיחים:
ב. טמפרטורה גבוהה משפרת את מהירות הדיפוזיה ולכן התוצאה תהייה הפוכה במקרה זה- מהירות הדיפוזיה אמורה להיות מהירה יותר בפלסמה.
ג. צמיגות נמוכה משפרת את מהירות הדיפוזיה ולכן התוצאה תהייה הפוכה במקרה זה- מהירות הדיפוזיה אמורה להיות מהירה יותר בפלסמה.
ד. שטח הדיפוזיה (A) הוא פרמטר המתאר את שטח הפנים של הממברנה ולא נכון להוסיף אותו בדיפוזיה פשוטה.
להרחבה- , Bern & Levy מהדורה 8 עמוד 10 (דיפוזיה).
פיזיולוגיה 4 שאלה 35
נתונים שני מדורים בעלי דפנות קשיחות כמתואר למטה. בין שני המדורים ממברנה שאינה חדירה לחלבונים .(P-) כיצד תראה המערכת לאחר הגעה לשיווי משקל?
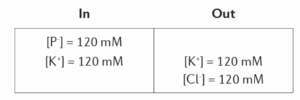
במה השאלה עוסקת: גיבס דונן
תשובה ד. שאלה זו עוסקת במערכת גיבס דונן אך עם אשלגן במקום נתרן. במערכת גיבס דונן ישנם שני מכלים: מיכל המייצג את הציטופלסמה שבו ישנם חלבונים בעלי מטען שלילי שאינם חודרים את הממברנה וכן קטיון. במיכל הנוסף שמייצג את חוץ התא יש את אותו קטיון ובנוסף אניון. כיון שריכוזי כל החומרים זהים אין הפרש מטענים בין המכלים, אולם כן ישנו הפרש ריכוזים עבור חלק מן החומרים. החלבונים בתא אינם נמצאים מחוצה לו וכלור אינו נמצא בתוך התא. יחד עם זאת, החלבונים אינם יכולים לחדור את הממברנה וכלור כן יכול ולכן הוא נע לתוך התא בהתאם למפל הריכוזים שלו. אשלגן, בעקבות ההפרש החשמלי שנוצר לאחר מעבר כלור, נע גם הוא באותו כיוון והתוצאה היא שיש כמות גודלה יותר של מומסים בתוך התא ולכן האוסמולריות שלו עולה. כיון שבמערכת זו הדפנות הקשיחות לא מאפשרות מעבר מים, תוך התא ישאר בערכים אוסמולריים גבוהים יותר ביחס לחוץ התא.
כעת נחרוג מן הדוגמה הספציפית בשאלה זו ונעבור לדבר על מצבים פיסיולוגיים. האסטרטגיה של דפנות קשיחות אופיינית לצמחים, אולם בני אדם משתמשים באסטרטגיה שונה למניעת כניסת מים לתא. אצל בני אדם יש אפקט המכונה “אפקט דונאן כפול” ולפיו נתרן אף הוא אינו חודר את הממברנה. במצב מנוחה, הממברנה חדירה לנתרן במידה מסוימת. לכן, כמות הנתרן שמצליחה לחדור את הממברנה, מסולקת באמצעות משאבת Na+/K+ ובכך הופכת את נתרן למעשה ליון בלתי חדיר. כיון שנתרן אינו חודר את הממברנה, מים לא עוקבים אחריו לתוך מיכל א’ ולכן גם בדונן כפול אין מעבר מים.
שלילת מסיחים:
א. האוסמולריות בשני המדורים אינה שווה כיון שקיים מפל ריכוזים לכלור שגורר אחרי את אשלגן ומעלה את האוסמולריות בתוך התא.
ב. הקטיון יכנס ולא יצא מן התא (כפי שנרמז ממסיח זה) וזאת כאמור בעקבות מפל הריכוזים של כלור.
ג. בשיווי משקל גיבס דונן אין מעבר מים כפי שמפורט בתשובה לסעיף ד’ שבשאלה זו.
להרחבה – מומלץ לקרוא על מערכת גיבס דונן בספר הקורס שנמצא באתר ולקריאה נוספת ניתן לקרוא מהמקורות המצוינים שנמצאים בספריה שלאוניברסיטת תל אביב. Bern & Levy אינם המקור המועדף בנושא זה.
Aidley, David J. ThePhysiology of Excitable Cells. Cambridge University Press, 1998. pp. 26-28
Sperelakis, Nicholas. CellPhysiology Sourcebook: A Molecular Approach. Gulf Professional Publishing,2001. pp. 243-246.
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: מערכת גיבס דונאן
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 2
פיזיולוגיה 1 שאלה 25
נתונות ארבעת תמיסות שונות של 10% אחוז משקלי: תמיסת אוראה (g\mol Mw=60), תמיסת NaCl (g\mol Mw=58), תמיסת סוכרוז (Mw = 342 g\mol) ותמיסת גלוקוז (g\mol Mw = 180). מי מבין התמיסות היא בעלת האוסמולריות הגדולה ביותר?
במה השאלה עוסקת: אוסמולריות
תשובה ב. אוסמולריות מוגדרת כמספר החלקיקים לליטר ממס, והיא מחושבת על ידי מכפלה של ריכוז החומר במספר החלקיקים שהמולקולה מתפרקת אליהם בתמיסה. בשאלה לא נתון הריכוז, אלא האחוז המשקלי. אנחנו צריכים להסיק מהאחוז המשקלי מידע בנוגע לריכוז. כאשר אנו נשאלים על תמיסות בעלי אותו אחוז משקלי, יש שני כללי אצבע שחשוב לזכור:
1. כאשר משווים בין מולקולות המתפרקות לאותה כמות חלקיקים – תמיסה המכילה חלקיקים בעלי משקל מולקולרי נמוך יותר, בהכרח תהייה בעלת אוסמולריות גבוהה יותר. הסיבה לכך היא שכדי שחלקיקים בעלי מסה קטנה יותר יגיעו לאותו אחוז משקלי כמו תמיסה המכילה חלקיקים בעלי מסה גדולה יותר, דרושים יותר חלקיקים.
2. כאשר משווים בין תמיסות בעלות משקל מולקולרי דומה – תמיסה המכילה מולקולות המתפרקות ליותר חלקיקים, בהכרח תהייה בעלת אוסמולריות גבוהה יותר.
תמיסת הגלוקוז והסוכרוז אינן מתפרקות לחלקיקים נוספים בתמיסה והמשקלים המולקולריים של הגלוקוז והסוכרוז הם הגדולים ביותר בהשוואה ליתר התמיסות. לכן, אפילו ללא חישוב אנו יכולים להסיק כי אלו הן שתי התמיסות בעלות האוסמולריות הנמוכה ביותר. אוראה היא בעלת משקל מולקולרי גדול יותר מ-NaCl ובנוסף אינה מתפרקת בתמיסה ולכן האוסמולריות שלה נמוכה יותר מתמיסת NaCl בעלת אותו אחוז משקלי. כלומר, NaCl הינה התמיסה בעלת המשקל המולקולרי הנמוך ביותר וכן מתפרקת להכי הרבה חלקיקים, ולכן היא התמיסה בעלת האוסמולריות הגבוהה ביותר ביחס לשאר התמיסות.
להרחבה – Bern & Levy, מהדורה 8 עמודים 12-16 (אוסמוזה).
פיזיולוגיה 4 שאלה 22
מה משותף למצב בו הממבנרה נמצאת בשיווי משקל ולמצב בו היא נמצאת במצב יציב(steady state)?
במה השאלה עוסקת: שיווי משקל או מול מצב עמיד
תשובה א .
בכל מצב בו אין שינוי במתח הממברנה- סכום השטפים דרך הממברנה בהכרח שווה לאפס. גם במצב יציב וגם בשיווי משקל סכום השטפים דרך הממברנה שווה לאפס. כלומר, מתח הממברנה לא השתנה.
דיברנו על שני מצבים כאלו:
1. שיווי משקל גיבס דונאן. אמרנו שמה שמאפיין שיווי משקל גיבס דונאן-
יש בהכרח הפרש אוסמולריות- המדור בעל היון הבלתי חדיר (למשל חלבון) יהיה בעל האוסמולריות הגדולה יותר.
קיים שיווי משקל אלקטוריכמי – כל אחד מהיונים נמצא בשיווי משקל (כך הגענו לנוסחא) ולכן הדלתא G של המערכת הוא 0 (אין השקעת אנרגיה= שיווי משקל).
2. משוואת Chord Conductance Equation משוואת מתח הממברנה.
על אף ששטפי היונים אשלגן, נתרן וכלור קובעים את מתח הממברנה במנוחה (Vm), הוא אינו שווה לפוטנציאל שיווי המשקל של אף אחד מיונים אלו (EK, ENa, Ecl) אלא הינו מעין ממוצע משוקלל שלהם. ככלל מפתח, כאשר Vm נקבע ע”י שני יונים או יותר, התרומה של כל יון לערכו של Vm תלויה בחדירות היחסית שלו.
משוואה זו מראה כי ככל שחדירות הממברנה של יון גדולים יותר, כך תרומתו לפוטנציאל הממברנה המשוקלל עולה. כאשר החדירות ליון מסוים גבוהה באופן חריג, משוואת מתח הממברנה שווה למעשה (בקירוב) למשוואת נרנסט של אותו היון.
מילה על ההבדל בין שיווי משקל למצב יציב:
מה ההבדל בין שיווי משקל ומצב יציב? הרי בשניהם אין שינוי בריכוזים. ההבדל טמון בדרישות האנרגטיות.
בשיווי משקל הריכוזים אינם משתנים מכיוון שאף אחד לא רוצה שהם ישתנו – כולם מאושרים. למשל, בפונטציאל שיווי משקל (נרנסט) של יון כלשהו, הריכוזים של אותו יון אינם משתנים מכיוון שהכוח הכימי שווה לכוח החשמלי – טוב לו, ליון.
מתח הממברנה לעומת זאת, אינו מוגדר כשיווי משקל אלא כמצב יציב. הריכוזים נותרים קבועים וזאת למרות (ולא בזכות) רצונות היונים (שהרי כולם “לא מרוצים”). כדי לשמור על ריכוז (ובהתאם מתח מנוחה) קבוע, התא צריך להשקיע הרבה מאד אנרגיה בפעילות המשאבה Na-K-ATPase
שמירה על הומיאוסטזיס
הומאוסטזיס – תהליך שמירת נפח, תכולה וטמפרטורות מדורי המים בגוף קבועים. הומאוסטזיס נשמר באמצעות השקעת אנרגיה, כלומר מדובר במצב יציב (steady state).
כדי לשמור על steady state למערכת צריכה להיות set point, אותו ערך אליו היא שואפת לתקן את המצב במקרה של חריגה. כלומר, אם ישנה כניסה מוגברת של יוני אשלגן, המערכת צריכה לזהות חריגה מהריכוז התקין (הוא ה-set pint) ולהפעיל את המנגנונים המתאימים (נקראים effectors). כדי לזהות חריגה מה-set point למערכת צריכים להיות חיישנים וכלי מדידה מתאימים.
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: שמירה על הומאוסטזיס
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1
להרחבה – Berne and Levy, Physiology , מהדורה 8, עמודים 17-19.
פיזיולוגיה 1 שאלה 21
זרקו כדורית דם לתוך מיכל עם תמיסה, נפח הכדורית גדל ואז התייצב בשיווי משקל. אילו מן התמיסות הבאות יכולה לגרום לכך?
במה השאלה עוסקת: תמיסות בשימוש קליני
תשובה ה. על מנת שנפח הכדוריות יגדל, התמיסה אליה מוכנס תא הדם האדום צריכה להיות תמיסה היפוטונית (תמיסה בה ריכוז החלקיקים האפקטיביים נמוך מריכוזים בתוך התא). תמיסה היפוטונית מדללת את הסביבה החוץ תאית כך שהלחץ האוסמוטי בתוך התא עולה. בעקבות כך מים ינועו לתוך התא על מנת להשוות את הלחץ האוסמוטי שנוצר. כתוצאה מכך נפח התא יעלה והאוסמולריות של הנוזל בתוכו תרד.
שלילת מסיחים:
א. תמיסת אוריאה איזואוסמוטית הינה תמיסה שאינה מייצרת לחץ אוסמוטי כלל, כיוון שאוריאה חוצה את ממברנת התא האדום בחופשיות. כלומר, המצב מקביל להכנסת האריתרוציט לתמיסת מים מזוקקים. אוריאה תכנס לתוך התא על מנת להשוות את מפל הריכוזים. מים ייכנסו לתוך התא, אל עבר המקום בו ריכוז החלקיקים האפקטיביים והלחץ האוסמוטי הוא גבוהה יותר. מכיוון שהתמיסה דומה לתמיסת מים מזוקקים ואין בה כלל לחץ אומסוטי, ייכנסו מים לתוך התא עד כדי פיצוץ שלו והמערכת לא תספיק להגיע לשיווי משקל.
ב. תמיסת סליין היא תמיסה איזוטונית ביחס לנוזל התוך תאי. מכאן, שהיא אינה מייצרת לחץ אוסמוטי יחסי כלשהו באף אחד מהמדורים. בעקבות הכנסת הכדורית לתמיסה, לא תהייה תנועה נטו של מים לאף כיוון ולא יהיה שינוי בנפח התא.
ג. תמיסת גלוקוז 10% היא תמיסה היפר-טונית ביחס לפנים התא. כלומר, התמיסה תייצר לחץ אוסמוטי יחסי מחוץ לתא שיגרור יציאה של מים מתוך התא אל עבר המקום שבו ריכוז המומסים האפקטיביים הוא גובהה יותר. כתוצאה מכך נפח התא יקטן.
ד. גזים חוצים את ממברנת התא בדיפוזיה פשוטה ולכן חדירים לחלוטין את הממברנה. מכאן, שהתמיסה לא מייצרת לחץ אוסמוטי כלל והתגובה שתתרחש עקב הכנסת תא הדם האדום לתמיסת מתאן תהייה זהה לזו של הכנסת התא לתמיסת אוריאה (מסיח א’).
להרחבה – Bern & Levy, מהדורה 8 עמודים 12-16 (אוסמוזה); עמודים 18-22 (מדורי המים בגוף).
פיזיולוגיה 4 שאלה 20
מה מהבאים נכון?
במה השאלה עוסקת: אינטגרציה- דיפוזיה וכוח אלקטרוכימי
תשובה ה .
שטף של חלקיק הוא ביחס ישר לריכוז ולקבוע הדיפוזיה (מכיל את תכונות הממס והמומס) וביחס הפוך למרחק. אין קשר למוביוליות.
יון הכלוריד נע כנגד מפל האנרגיה החשמלית שלו (תוך התא שלילי יותר). בנוסף, ריכוז הכלור בתוך התא קטן יותר ולכן כניסה של כלור לתוך התא תהייה עם מפל הריכוזים שלו.
אנרגיה פוטנציאלית (פוטנציאלה אלקטרוכימי) מורכבת מהכוח החשמלי והכוח הכימי אשלגן כלוריד מתפרק בתמיסה לאשלגן וכלור והם בהחלט בעלי מטען.
מכיוון שלגלוקוז אין מפל חשמלי, אלא רק כימי- המפל האלקטרוכימי שלו שווה למפל הכימי וניתן להזניח את הרכיב החשמלי מהמשוואה.
קבוע החדירות (P) מורכב ממקדם הדיפוזיה D וממרחק הדיפוזה. גם הצמיגות וגם הרדיוס נמצאים במכנה בקבוע הדיפוזיה- כלומר, ככל שהם יותר גדולים, השטף יהיה קטן יותר ולהפך. מכאן- יש יחס הפוך בינם לבין קבוע החדירות P.
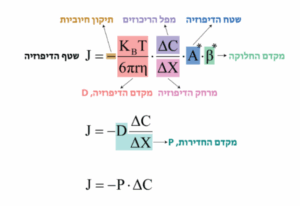
להרחבה – Berne and Levy, Physiology , מהדורה 8, עמודים 10-11.
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: דיפוזיה, פוטנציאל אלקטרוכימי
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1
פיזיולוגיה 4 שאלה 6
נתונות שתי תמיסות המופרדות על ידי ממברנה החדירה ליוני כלור, נתרן ולמים, אך לא חדירה לחלבון (P-). מה מהבאים נכון בתנאים של שיווי משקל של המערכת?
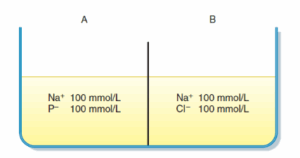
במה השאלה עוסקת: מערכת גיבס דונאן
תשובה א’. בתמונה מתואר המצב ההתחלתי בו שתי תמיסות מופרדות ע”י ממברנה החדירה לנתרן, כלור ומים, אך אינה חדירה לחלבון (P-). אוסמולריות תמיסה A זהה לזו של תמיסה B.
לאחר שנמתין זמן מה, יתרחשו התנועות הבאות:
כלור יעבור בדיפוזיה מתמיסה B לתמיסה A במורד מפל הריכוזים שלו ← דיפוזיה זו גורמת לתמיסה A להיות טעונה שלילית ביחס לתמיסה B← הכלור יוצר הפרש מתחים הגורם לנתרן לעבור בדיפוזיה מתמיסה B לתמיסה A ← עובר אותו מספר מולקולות נתרן כמו מולקולות הכלור שעברו, שכן מטרת הנתרן היא לסתור את המטענים השליליים של הכלור ← כעת יש מפל אוסמוטי כאשר תמיסה A בעלת אוסמולריות גבוהה יותר ולכן יעברו מתא B לתא A, נשים לב כי מעבר המים יוריד את הריכוז של כלל היונים בצד A (כולל החלבון), מה שיצור כוח מניע לכלור לעבור מתא B לתא A וחוזר חלילה. ברגע שתנועת המים תעצר (למשל- אם הכלים סגורים ומלאים) הגענו ל-“שיווי משקל גיבס-דונן”. נשים לב כי בשיווי משקל זה ישנו הפרש אוסמולריות בין התמיסות (תמיסה A בעלת אוסמולריות גבוהה יותר).
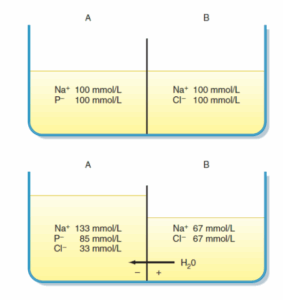
להרחבה – מומלץ לקרוא על מערכת גיבס דונן בספר הקורס שנמצא באתר ולקריאה נוספת ניתן לקרוא מהמקורות המצוינים שנמצאים בספריה של אוניברסיטת תל אביב. Bern & Levy אינם המקור המועדף בנושא זה.
Aidley, David J. ThePhysiology of Excitable Cells. Cambridge University Press, 1998. pp. 26-28
Sperelakis, Nicholas. CellPhysiology Sourcebook: A Molecular Approach. Gulf Professional Publishing,2001. pp. 243-246.
פיזיולוגיה 1 שאלה 16
המערכת הבאה מתארת מערכת דונן הנמצאת בש”מ בטמפרטורת החדר (27oC). יוני הנתרן והכלור חדירים דרך הממברנה, ואילו החלבון (P2-) אינו חדיר. מה ריכוז Pr2- בתא A?
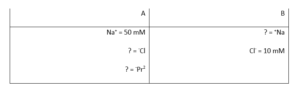
במה השאלה עוסקת: שיווי משקל גיבס דונן
תשובה ג. במערכת גיבס דונן שמתוארת בשאלה ישנם שני מיכלים: מיכל A המכיל חלבונים שאינם חודרים את הממברנה, נתרן וכלור, ומיכל B המכיל נתרן וכלור. נתון לנו שהמערכת נמצאת בשיווי ולכן חשוב לציין שבמקרה זה קיים הפרש אוסמולריות בין התאים, אך לא קיים הפרש מטענים וזאת כיון שכל תא הוא אלקטרוניטרלי (כלומר מכיל את אותה כמות של מטענים חיוביים ושליליים). כלומר, כל תא בנפרד מאוזן מבחינת המטענים, אולם כן יש הבדלי ריכוזים של היונים שבמערכת בין התאים. על פי עקרון האלקטרוניטרליות ניתן להסיק שריכוזו של נתרן במיכל B הוא 10mM. כשמערכת גיבס דונן נמצאת בשיווי משקל, מכפלת שני היונים במיכל A שווה למכפלת שני היונים במיכלB . כלומר ניתן לנסח את המשוואה באופן הבא: 50mMNa+*XmMcl-=10mMNa+*10mMcl-, ומכאן ניתן להסיק כי ריכוז כלור הוא כ- 2mM בתא A. ניתן לחשב את ריכוז החלבון על סמך ריכוז הכלור והנתרן שבתא. חשוב לשים לב כי החלבון בעל ערכיות של -2 ולכן בחישוב המטענים על פי עקרון האלקטרוניטראליות, יש לחלק את מספר המטענים הדרושים לאיזון החשמלי פי 2, כדי למצוא את ריכוז החלבון. על פי עקרון האלקטרונטרליות חסרים עוד 48 מטענים שליליים בכדי לאזן את תא A חשמלית, כלומר ריכוז של 24mM חלבון. כעת נרצה להבין את הדינמיקה בין היונים במערכת שלב אחר שלב. תחילה כלור, שנמצא במכיל B ולא נמצא במיכל A, רוצה לעבור למיכלA בגלל הבדלי ריכוזים. נתרן, בעקבות ההפרש החשמלי שנוצר לאחר מעבר כלור, נע גם הוא ממיכל B למיכל A. אולם, על נתרן פועלים שני כוחות, האחד חשמלי שמושך אותו להיכנס למיכל A והשני נובע מהנתרן שכבר נמצא במיכל A ומקשה על נתרן נוסף להיכנס. בסופו של דבר המערכת מגיעה לשיווי משקל וריכוז זהה של נתרן וכלור עוברים ממיכל B למיכל A.
שלילת מסיחים:
א. במסיח זה, סך המטענים השליליים שהחלבון תורם הם 30- ולכן כאשר מחשבים יחד עם התרומה של נתרן אנו רואים כי חסרים עדיין מטענים שליליים בשביל לאזן חשמלית את מיכל A. כמות המטענים שחסרים היא מתאימה לריכוז של 20mM כלור, אולם אנו יודעים כי ריכוז כלור הינו רק 2mM ולכן מסיח זה נפסל.
ב. סך המטענים השליליים שהחלבון תורם הם 40- ולכן כאשר מחשבים יחד עם התרומה של נתרן אנו רואים כי חסרים עדיין מטענים שליליים בשביל לאזן חשמלית את מיכל A. כמות המטענים שחסרים מתאימה לריכוז של 10mM כלור. כיון שאנו יודעים כי ריכוז כלור הוא 2mM מסיח זה נפסל גם הוא.
ד. סך המטענים השליליים שהחלבון תורם הם 50- ולכן כאשר מחשבים יחד עם התרומה של נתרן אנו רואים כי לא חסרים מטענים שליליים בשביל לאזן חשמלית את מיכל A. כאמור, כיון שידוע לנו כי קיים כלור בתא A בריכוז של 2mM מסיח זה גם הוא נפסל.
ה. סך המטענים השליליים שהחלבון תורם הם 80- ולכן כאשר מחשבים יחד עם התרומה של נתרן אנו רואים כי חסרים מטענים חיוביים בשביל לאזן חשמלית את התא. מצב זה גם הוא אינו אפשרי במערכת גיבס דונן כיון שעקרון האלקטרוניטראליות נפגם.
להרחבה – מומלץ לקרוא על מערכת גיבס דונן בספר הקורס שנמצא באתר ולקריאה נוספת ניתן לקרוא מהמקורות המצוינים שנמצאים בספריה של אוניברסיטת תל אביב. Bern & Levy אינם המקור המועדף בנושא זה.
Aidley, David J. The Physiology of Excitable Cells. Cambridge University Press, 1998. pp. 26-28
Sperelakis, Nicholas. Cell Physiology Sourcebook: A Molecular Approach. Gulf Professional Publishing, 2001. pp. 243-246.
פיזיולוגיה 1 שאלה 14
אילו מהמשפטים הבאים נכון בנוגע לתעלות יוניות?
במה השאלה עוסקת: טרנספורטרים – תעלות ונשאים
תשובה ב. קצב הטרנספורט דרך תעלה הוא מהיר יותר כיון שתעלה לא נדרשת לבצע שינוי קונפורמציה, בעוד שנשא, לאחר קישור הסובסטרט, חייב לשנות קונפורמציה ולשחרר את החומר בצדה השני של הממברנה. תעלה היא למעשה חור סלקטיבי בממברנה ולכן חומרים עוברים דרכה באופן מהיר יותר. הבדל נוסף בין שני הטרנספורטרים הוא האופן שבו כל אחד מגיב לריכוזי סובסטרט עולים. עבור חומר שעובר בדיפוזיה דרך תעלות, קצב הדיפוזיה יגדל באופן ליניארי כתלות בריכוזי סובסטרט עולים. לעומת זאת, דיפוזיה דרך נשא מתנהגת באופן דומה לקינטיקת מיכאליס מנטן. במודל מיכאליס מנטן, בריכוזי סובסטרט גבוהים האנזים (או הנשא) מגיע לרוויה כאשר הוספה של סובסטרט נוסף לא תגדיל את המהירות. למעשה המהירות בנקודה זו היא המהירות המקסימלית.
שלילת מסיחים:
א. חוק פיק מודד דיפוזיה פשוטה ולא דיפוזיה דרך תעלות או נשאים. דיפוזיה פשוטה היא דיפוזיה שלא נעזרת באף חלבון לצורך המעבר ומתרחשת עם מפל הריכוזים. ניתן לחשב קצב מעבר דרך תעלה אבל הדבר נובע מהתכונות של התעלה, מטען חשמלי וכדומה, חישובים שאינם רלוונטים עבורכם. כן חשוב להבין שעבור חומר שחודר את הממברנה בקלות בדיפוזיה פשוטה, קצב הדיפוזיה יתנהג באופן דומה לדיפוזיה דרך תעלות. ככלל, קצב הדיפוזיה יגדל באופן ליניארי כתלות בריכוזי סובסטרט עולים. יחד עם זאת יש הבדלים בין דיפוזיה פשוטה ודיפוזיה דרך תעלה כמו למשל שתעלה יכולה להיסגר, וכן כפי שציינתי תכונות נוספות שיש לתעלות.
ג. ישנם מצבים בהם חומרים נעים כנגד מפל הריכוזים שלהם כמו למשל במקרה של יונים שהן מולקולות טעונות. עבור יונים ישנם שני כוחות שקובעים את כוון תנועתם, הכוח החשמלי והפרשי הריכוזים. כאשר הכוח החשמלי למשל גדול יותר מהכוח הנובע ממפל הריכוזים, היון ינוע כנגד מפל הריכוזים שלו עד אשר שני הכוחות יתאזנו. פוטנציאל אלקטרוכימי הוא ערך שמשלב את שני הכוחות הללו וניתן להסתכל עליו ככמות האנרגיה הפוטנציאלית שתשתחרר בעת העברת המולקולה בין צדדי הממברנה (מחושב ב-Juole). ניתן לחשב פוטנציאל אלטקרוכימי של חומר באמצעות הנוסחה הבאה: μx= RTlnXiXo+ZxFVm, כאשר R הוא קבוע הגזים, T טמפרטורה, Xi ריכוז בתוך התא, Xo ריכוז מחוץ לתא, Zx ערכיות היון,F קבוע פאראדיי ו- Vm מתח הממברנה. כאשר שני הכוחות משתווים היון מגיע לשיווי המשקל שלו והפוטנציאל האלקטרוכימי משתווה ל-0.
ד. ישנם נשאים שמעבירים חומרים עם מפל הריכוזים וכנגד מפל הריכוזים. נשאים שמעבירים חומר כנגד מפל הריכוזים צורכים לשם כך אנרגיה וטרנספורט מסוג זה מכונה טרנספורט אקטיבי. נשאים שדורשים אנרגיה לצורך ההעברה והאנרגיה שלהם אינה מגיעה מ-ATP, פועלים במנגנון המכונה טרנספורט אקטיבי שניוני. בטרנספורט אקטיבי שניוני יש שימוש במפל ריכוזים של חומר X (אשר הושג באמצעות הידרוליזת ATP), לצורך העברת חומר Y לצידה השני של הממברנה כנגד המפל האלקטרוכימי שלו. מנגנון העברה זה יכול להיות סימפורטר (co-transporter/symporter) או אנטיפורטר (antiporter). תעלות בהכרח מעבירות חומרים באופן פסיבי, כלומר עם המפל האלקטרוכימי של המולקולה ולכן לא צורכות אנרגיה לשם כך.
ה. תעלות ונשאים הם טרנספורטרים בררניים ולכן אינם יכולים להעביר דרכם מספר סוגים של יונים. בתעלות למשל יש סלקציה לפי גודל היון וצפיפות המטען החשמלי שלו ולכן הן סלקטיביות ליון מסוים. חשוב לסייג אמירה זו בכך שישנן תעלות שפחות בררניות ויכולות להעביר יונים בעלי מכנה משותף כמו למשל יונים חיוביים- נתרן ואשלגן.
פיזיולוגיה 4 שאלה 29
במערכת המתוארת להלן שני תאים מלאים במצב שיווי משקל. בתוך התא יש חלבון 3 P-(בעל שלושה מטענים שליליים) בריכוז של 25mM וכן אשלגן K+ בריכוז 100mM. הממברנה שבין התאים חדירה לאשלגן ולכלור Cl- אבל לא לחלבון. מהו ריכוז האשלגן מחוץ לתא?

במה השאלה עוסקת: שיווי משקל גיבס דונן
תשובה ג. בשאלה זו חסרים הריכוזים של היונים החוץ תאיים וכדי למצוא אותם חשוב להגיע למספר הנחות ראשוניות. תחילה נתון לנו שהמערכת נמצאת בשיווי משקל ונקודה זו חשובה כי ללא נתון זה לא ניתן להניח שיווי משקל. כמו כן לא כתוב באופן ברור שמדובר בשיווי משקל גיבס דונן, אולם קיימים המאפיינים של גיבס דונן ולכן ניתן להניח זאת. יחד עם זאת, הגון מצד הבוחנים לרשום שמדובר בשיווי משקל גיבס דונן אך כדאי להתכונן גם לתרחיש בו זה לא יהיה רשום במפורש. המאפיין המרכזי של גיבס דונן הוא שקיים חלבון שהוא בלתי חדיר לממברנה המייצג את הציטופלסמה התאית. בגיבס דונן כפול יהיה גם יון טעון חיובית שאינו חודר את הממברנה, והוא ממוקם במיכל השני המייצג את חוץ התא. המטרה של שיווי משקל גיבס דונן הוא להציג כיצד החלבון הבלתי חדיר יכול ליצור הפרש אוסמולריות ובגיבס דונן כפול, גם הפרש מתחים (למעשה גיבס דונן כפול מסביר כיצד נוצר מתח ממברנה). כמו כן דפנות קשיחות מרמזות לנו על שאלת גיבס דונן. כעת לאחר שהגענו למסקנה שמדובר בשאלת גיבס דונן ונתון לנו שאנו בשיווי משקל, ניתן להכיל את הכללים שאתם מכירים בנוגע למערכת גיבס דונן. למדנו שמכפלת ריכוזי היונים החדירים בצד אחד שווה למכפלה שלהם בצד השני. כעת לפני שנבצע את המכפלה נרצה לחלץ את ריכוז הכלור התוך תאי. כיון שהערכיות של החלבון הינה -3 הוא גם תורם למטען החשמלי פי 3 מהריכוז שלו ולכן החישוב הוא באופן הבא:

שלילת מסיחים:
א. ניתן לראות לפי החישובים שבסעיף ג’ שריכוז אשלגן הוא 50mM.
ב. ניתן לראות לפי החישובים שבסעיף ג’ שריכוז אשלגן הוא 50mM.
ד. לכאורה זה נראה שחסרים נתונים בשאלה זו, אבל כאשר עוברים שלב אחר שלב ניתן לראות שיש למעשה מספיק נתונים כדי לענות עליה. תחילה חשוב להבין שמדובר בשאלת גיבס דונן בה רק החלבון אינו חודר את הממברנה וכן שהמערכת כבר נמצאת בשיווי משקל. לאחר מכן ניתן לחלץ את ריכוז הכלור התוך תאי ובסוף באמצעות מכפלת הריכוזים אפשר לחלץ את מכפלת ריכוז אשלגן וכלור החוץ תאיים וממנה את ריכוז האשלגן לבדו.
להרחבה – מומלץ לקרוא על מערכת גיבס דונן בספר הקורס שנמצא באתר ולקריאה נוספת ניתן לקרוא מהמקורות המצוינים שנמצאים בספריה של אוניברסיטת תל אביב. Bern & Levy אינם המקור המועדף בנושא זה.
Aidley, David J. The Physiology of Excitable Cells. Cambridge University Press, 1998. pp. 26-28
Sperelakis, Nicholas. Cell Physiology Sourcebook: A Molecular Approach. Gulf Professional Publishing, 2001. pp. 243-246.
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: מערכת גיבס דונאן
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 2
פיזיולוגיה 1 שאלה 3
כיצד יושפע הנוזל התוך תאי והנוזל החוץ תאי מהוספה של מים מזוקקים לפלסמה? הנח כי האוסמלליות המקורית של הפלסמה הינה 300 mOsm / L.
במה השאלה עוסקת: טוניות ומדורי המים בגוף
תשובה ג. מים מזוקקים הם מים ללא מומסים כלל ולכן ערך האוסמולליות שלהם הוא אפס. תמיסה של מים מזוקקים היא היפוטונית לפלסמה. טוניות היא מדד לריכוז מומסים אפקטיביים בתמיסה, כלומר מומסים שאינם חוצים את הממברנה. זהו מונח השוואתי בין שתי תמיסות שונות. תמיסות איזוטוניות הן תמיסות עם אותה כמות מומסים אפקטיביים, תמיסה היפרטונית היא תמיסה עם יותר מומסים אפקטיביים ביחס לתמיסה אחרת ותמיסה היפוטונית היא תמיסה עם פחות מומסים אפקטיביים ביחס לתמיסה אחרת. הכנסה של תמיסה היפוטונית תוריד את ערך האוסמולליות בפלסמה (plasma) ובכל המדור החוץ תאי. לצורך תזכורת המדור החוץ תאי מחולק לשני מדורים, הפלסמה והנוזל הבין רקמתי (interstitial fluid). תתי מדורים אלו מופרדים על ידי קירות מערכת הדם שחדירות ליונים ומולקולות קטנות ואינן חדירות לחלבונים. כלומר, ההשפעה על המדור החוץ תאי היא הורדת האוסמולליות ונוסף לכך הגדלת הנפח. הנפח החוץ תאי יגדל כיון שהוספנו תמיסה ודבר זה לבדו גורר עלייה בנפח.
כעת ננסה להבין את ההשפעה על המדור התוך תאי. המדור התוך תאי מופרד על ידי ממברנה בררנית, אולם מים עוברים בממברנה זו באמצעות תעלות המכונות אקוופורינים (aquaporins). מיד לאחר הוספת התמיסה האוסמולליות בחוץ התא קטנה והתמיסה החוץ תאית נהייתה היפוטונית ביחס לתמיסה התוך תאית. לפיכך, הכוח המניע של המים הוא להיכנס לתא וזאת כדי להפוך את התמיסות לאיזוטוניות. כניסה של מים לתוך התא מעלה את כמות הממס (מים) בתוך התא בעוד כמות המומס נשארת זהה. מים נכנסים לתא עד שחוץ התא ופנים התא מגיעים לשיווי משקל חדש בו שני המדורים הם איזוטונים אחד לשני. כפי שקרה לחוץ התא, הכניסה של מים לתוך התא גרמה לנפח התוך תאי לגדול ולאוסמולליות התוך תאית לקטון.
שלילת מסיחים:
א. מסיח זה נכון בחלקו, אמנם הנפח החוץ תאי יגדל עקב הוספת התמיסה, האוסמולליות דווקא תקטן. הסיבה לכך היא שהוספנו תמיסה היפוטונית כלומר בעלת מספר מומסים קטן יותר (ובשאלה זו ללא מומסים כלל). פעולה זו מגדילה את כמות הממס ולא משנה את כמות המומס. אוסמולליות היא מספר מומסים, אוסמול, לקילו ממס. כיון שהגדלנו את כמות הממס, מספר המומסים לקילו ממס ירד. כמו כן הנפח התוך תאי יגדל ולא יקטן עקב כניסה של מים לתא כפי שמתואר בתשובה לסעיף ג’.
ב. כיון שהאוסמולליות בחוץ התא קטנה בעקבות הוספת התמיסה, מים יכנסו לתוך התא כדי להשוות את ערכי האוסמולליות בין המדורים. הדבר יוביל לכך שנפח התא יגדל והאוסמולליות בו תרד וזאת בניגוד למתואר במסיח זה.
ד. מסיח זה מתאר נכונה שהאוסמולליות בחוץ ובתוך תאית תקטן, אולם נפחם של מדורים אלו יגדל. נפחם יגדל בעקבות הוספת התמיסה לחוץ התא וכן כניסה של מים לתוך התא.
פיזיולוגיה 4 שאלה 27
מה שטף הדיפוזיה של טריפטופן בהינתן שמקדם החדירות שלו P = 10^-7 [cm / sec], הריכוז התוך תאי הוא 3-^10 [mol / cm3] והריכוז החוץ תאי 4-^10 [mol / cm3] ?
במה השאלה עוסקת: חישוב שטף
תשובה ד. כדי לענות על שאלה זו נציב את המספרים בנוסחת השטף המכילה את מקדם החדירות (P) כיון שהן הריכוזים והן P נתונים לנו בשאלה: J=P*(Cin-Cout). לאחר הצבת הנתונים מתקבל J=10-7*10-3-10-4. בנקודה זו לי נוח להוסיף שלב נוסף בו המשוואה נכתבת באופן הבא: J=10-7*0.01-0.001, כעת נחסר ונקבל J=10-7*0.009 כאשר ניתן לכתוב את זה גם באופן הבא: J=10-7*(9*10-4).
לאחר ההכפלה אנו מקבלים את התשובה:
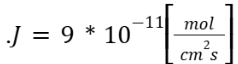
כעת נתייחס קצת ליחידות השטף. שטף נמדד ביחידות 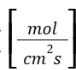 (כאשר לא מתייחסים לשטח הפנים). יחידות אלו מתקבלות כשכופלים לפי המשוואה את היחידות של מקדם החדירות P בהפרש הריכוזים. היחידות של P הן
(כאשר לא מתייחסים לשטח הפנים). יחידות אלו מתקבלות כשכופלים לפי המשוואה את היחידות של מקדם החדירות P בהפרש הריכוזים. היחידות של P הן ![]() ושל ריכוז
ושל ריכוז 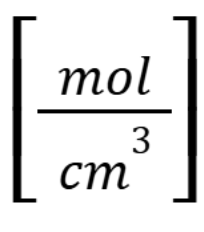 ולפיכך כשכופלים את היחידות של ערכים אלה אחד בשני מקבלים
ולפיכך כשכופלים את היחידות של ערכים אלה אחד בשני מקבלים 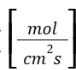
להרחבה – Bern & Levy, מהדורה 8 עמודים 10-11 (דיפוזיה).
נושא: פיזיולוגיה תת נושא: הומאוסטזיס תת-תת נושא: דיפוזיה
שם ספר: berne&levy, מהדורה 8 מס’ פרק: 1
פיזיולוגיה 1 שאלה 18
מטופל הגיע למיון כאשר הוא נחשף לרעלן שפוגע בתהליך שרשרת מעבר האלקטרונים. מי מהתהליכים הבאים לא ייפגע עקב כך?
במה השאלה עוסקת: טרנספורט ממברנלי
תשובה ג. פגיעה בתהליך שרשרת העברת אלקטרונים תגרום לפגיעה בייצור ה-ATP ובמאגרי האנרגיה בתא. עקב כך, יפגעו כל התהליכים בתא הזקוקים לאנרגיה. טרנספורט ממברנלי נחלק למספר סוגים מבחינת הצריכה האנרגתית- טרנספורנט ממברנלי פסיבי (כלומר, שלא צורך אנרגיה), טרנספורט ממברנלי אקטיבי ראשוני (המשתמש ישירות ב-ATP) וטרנספורט ממברנלי אקטיבי שניוני (המשתמש באנרגיה של העברת חומר אחד כנגד מפל הריכוזים על מנת להעביר חומר אחר עם מפל הריכוזים. יצירת מפל ריכוזים של חומר מסוים תמיד דורשת אנרגיה). טרנספורט GLUT2 הוא נשא יוניפורט המעביר גלוקוז לתוך התאים עם מפל הריכוזים שלו, כך שהוא נשא פסיבי שאינו דורש ATP.
שלילת מסיחים:
א. משאבת נתרן אשלגן הינה משאבה המשתמשת באופן ישיר בהידרוליזה של ATP על מנת להעביר 2 יוני נתרן מחוץ לתא ולהכניס 3 יוני אשלגן לתוך התא ולכן נחשבת טרנספורט אקטיבי ראשוני
ב. הסינפורט המעביר גלוקוז ונתרן בכליה משתמש באנרגיה של הכנסת נתרן לתא עם מפל הריכוזים על מנת להכניס גלוקוז לתוך התא כנגד מפל הריכוזים. כלומר, מדובר על טרספורט אקטיבי שניוני. שימו לב כי מספיק לדעת את משמעות המושג סימפורט על מנת לענות על השאלה, גם אם לא זכרתם את הנשא הספציפי.
ד. אנטיפורט NHE-1 נמצא על ממברנת כל תאי הגוף ומשמש תפקיד חשוב ברגולצית ה-PH בתוך התא וכן משמש את התא במהלך מנגנון ה- RVI. הטרנספורט מכניס יון נתרן במקביל להוצאת פרוטון החוצה מהתא. האנרגיה לפעילותו מגיעה ממפל הריכוזים של התנרן שנוצר בעזרת משאבת נתרן אשלגן הדורשת ATP. כלומר, מדובר בטרנספורט אקטיבי שניוני. שימו לב כי מספיק לדעת את משמעות המושג אנטיפורט על מנת לענות על השאלה, גם אם לא זכרתם את הנשא הספציפי.
ה. אנטיפורט סידן- נתרן נמצא גם כך על ממברנת כל תאי הגוף ומשחק תפקיד חשוב בשמירה על ריכוזים נמוכים של סידן בתוך התא. הטרנספורט מכניס שלושה יוני נתרן לתוך תא ומוציא יון סידן מחוץ לתא. האנרגיה לפעולתו מגיעה ממפל הריכוזים של הנתרן שנוצר בעזרת משאבת נתרן אשלגן הדורשת ATP, כלומר מדובר בטרנספורט אקטיבי שניוני.
להרחבה – Bern & Levy, מהדורה 8 עמודים 6-8 (טרנספורט ממברנלי).
פיזיולוגיה 2 שאלה 16
למה תגרום פתיחת תעלות כלור בנוירון שפוטנציאל הממברנה במנוחה= -80 mv ונתונים פוטנציאלי שיווי המשקל הבאים: mV Ena= +50, Ek= -100 mv, Ecl= -70 vm ?
במה השאלה עוסקת: פוטנציאל אלקטרוכימי
תשובה א. אם פוטנציאל שיווי המשקל של יון הכלור הוא -70mV אז כאשר מתח הממברנה נמוך מפוטנציאל שיווי המשקל, כלור יזרום החוצה (כיון שכלור הוא שלילי ומטרתו להפוך את מתח הממברנה לחיובי יותר). בעקבות יציאת הכלור מתח הממברנה יעלה כך שתיוצר דה-פולריזציה בממברנה.
שלילת מסיחים:
ב. מכיוון שכלור הוא יון שלילי, שטף של כלור החוצה יעלה את מתח הממברנה ויצור דה-פולריזציה.
ג. כאשר מתח הממברנה יהיה מעל פוטנציאל שיווי המשקל, הכלור יזרום פנימה.
ד. מכיוון שכלור הוא יון שלילי, שטף של כלור פנימה יוריד את מתח הממברנה ויצור היפר-פולריזציה.
להרחבה – Bern& Levy, מהדורה 8 עמודים 22-27 (שמירה על הומאוסטזיס).
פיזיולוגיה 4 שאלה 7
נתונה שכבת אפיתל. ממברנת הצד האפיקלי של התאים מכילה תעלות החדירות ליוני נתרן בלבד, בעוד שממברנת הצד הבזו- לטרלי מכילה תעלות חדירות ליוני אשלגן בלבד ומשאבות .Na/K ATPase פרט לכך הממברנות אינן חדירות ליונים אחרים. לתמיסות שמשני צידי האפיתל יש אותו הרכב: 13mM KCl + 150mM NaCl ואילו בתוך תאי האפיתל ריכוז יון האשלגן הוא 130mM וריכוז יון הנתרן הוא 15mM . איזה מתח חשמלי נמדד משני צידי האפיתל(=VmA מתח על גבי הצד האפיקלי,= VmB מתח על גבי הצד הבאזולטרלי(?
מה השאלה עוסקת: מתח הממברנה
תשובה א. בשאלה זו נתון תא אפיתל כאשר בצד האפיקלי הוא חדיר רק לנתרן ואילו בצד הבאזולטרלי התא חדיר רק לאשלגן. מתח הממברנה נקבע לפי המשוואה הבאה:
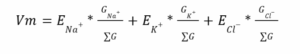
מתח הממברנה נקבע לפי היונים החדירים בלבד, לכן עבור הממברנה האפיקלית נחשב מתח ממברנה השווה לפוטנציאל שיווי המשקל (נרנסט) של נתרן ואילו בצד הבאזולטרלי נחשב פוטנציאל שיווי משקל של אשלגן בלבד. חשוב לציין שאמנם משאבת נתרן/אשלגן היא משאבה אלקטרוגנית, אבל התרומה שלה למתח הממברנה היא קטנה יחסית ולכן לא נתחשב בה בחישוב מתח הממברנה. כלומר החישוב עבור הצד האפיקלי יהיה באופן הבא:
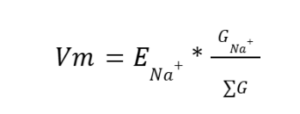
ואילו עבור הצד הבאזולטרלי מתח הממברנה יחושב באופן הבא:
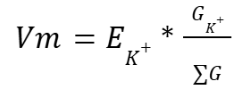
חשוב לציין שבשני המקרים המוליכות של כל אחד מהיונים הינה 1 כיון שבכל צד הם היון היחידי החודר את הממברנה (כאמור הזנחנו את ההשפעה של משאבת נתרן/אשלגן).
לפיכך נחשב את פוטנציאל נרנסט של נתרן שהוא למעשה מתח הממברנה בצד האפיקלי:
![]()
וכעת נחשב את פוטנציאל נרנסט של אשלגן שהוא למעשה מתח הממברנה בצד הבאזולטרלי:
![]()
שלילת מסיחים:
ב. מתח הממברנה בצד האפיקלי נקבע על פי נתרן כיון שהוא היון היחידי שהחודר את הממברנה בצד זה. על פי הפרשי הריכוזים של נתרן בין חוץ התא ותוך התא בצד האפיקלי פוטנציאל שיווי המשקל שלו הוא חיובי (+60).
ג. מתח הממברנה בצד האפיקלי נקבע על פי נתרן כיון שהוא היון החודר את הממברנה בצד זה. על פי הפרשי הריכוזים של נתרן בין חוץ התא ותוך התא בצד האפיקלי, פוטנציאל שיווי המשקל שלו הוא חיובי (+60). במסיח זה אפשר לטעון דבר דומה בנוגע לצד הבאזולטרלי בו מתח הממברנה נקבע על פי אשלגן כיון שהוא היון החודר את הממברנה בצד זה. על פי הפרשי הריכוזים של אשלגן בין חוץ התא ותוך התא בצד הבאזולטרלי, פוטנציאל שיווי המשקל שלו הוא שלילי (-60mv).
ד. במסיח זה הסימנים (פלוס ומינוס) נכונים בשני הצדדים אך גודל הפוטנציאל בצד הבאזולטרלי אינו נכון. הסיבה האפשרית לבחירה במסיח זה היא ניסיון להתחשב בפעילות משאבת נתרן אשלגן, אך כפי שכבר טענו בתשובה לסעיף א’, מזניחים את ההשפעה שלה בקביעת מתח הממברנה. משאבת נתרן/אשלגן עוזרת בלשמור על ריכוז יונים קבוע משני צדי הממברנה וזו ההשפעה שלה על מתח הממברנה.
להרחבה – Berne & Levy,מהדורה 8, עמודים 11-12 (גרדיאנט אלקטרוכימי);23-24 (פוטנציאל הממברנה).
פיזיולוגיה 4 שאלה 10
לאן יזרום כלור בהינתן שמתח השיווי משקל שלו -80mV ומתח הממברנה ?-70mV
במה השאלה עוסקת: ECF (ElectroChemical Force)
תשובה א. בשאלה זו קיימים שני נתונים, האחד הוא פוטנציאל שיווי המשקל של היון והשני הוא מתח הממברנה. שני נתונים אלו צריכים להדליק אצלכם נורה שאולי מדובר במשוואת הכוח המניע (ECF). משוואה זו מתייחסת לכיוון התנועה של יון בודד דרך הממברנה. להלן המשוואה:
ECF = Vm-Eion. במקרה של שאלה זו: ECF = -70 – (-80) = 10. כלומר שהכוח המניע של כלור הוא חיובי. בנקודה זו חשוב להזכיר את ההבדל בין זרם חיובי לזרם שלילי. זרם חיובי מאופיין בכך שהוא הופך את חוץ התא לחיובי יותר, ולכן כולל בתוכו יציאה של קטיון טעון חיובית החוצה מהתא או כניסה של אניון טעון שלילית לתוך התא. זרם שלילי גם הוא מתייחס לחוץ התא והוא מאופיין ביציאה של אניון מהתא או כניסה של קטיון לתוך התא.
כעת כאשר מדובר באניונים כמו כלור, כאשר ה-ECF חיובי, הזרם של האניון יהיה לתוך התא, כלומר זרם חיובי. מקרה זה מסכם את התשובה לשאלה אך נמשיך לתאר את כל שאר האפשרויות. כאשר ה-ECF הינו שלילי, כיוון התנועה של אניון היא כלפי חוץ, כלומר זרם שלילי. כעת נעבור בקצרה מה קורה כאשר מדובר בקטיונים. כאשר ה-ECF חיובי, הקטיון יצא מהתא, כלומר זרם חיובי. כאשר ה-ECF שלילי, הקטיון יכנס לתא, כלומר זרם שלילי.
שלילת מסיחים:
ב. כלור טעון שלילית ולכן ב-ECF חיובי הוא יצור זרם חיובי, כלומר יכנס לתוך התא. כמו כן יש במסיח זה הגדרה שגויה של זרם חיובי, כיון שיציאה של כלור מחוץ לתא תגרום לחוץ התא להיות שלילי יותר – כלומר זרם שלילי.
ג. כלור אכן יכנס לתוך התא אך זה יגרום לזרם חיובי (על פי ההגדרה) ולא לזרם שלילי.
ד. יציאה של כלור מחוץ לתא היא אכן זרם שלילי, אך כיון שה-ECF שלנו יצא חיובי, כיוון הזרם של כלור יהיה חיובי, כלומר לתוך התא.
להרחבה – Bern & Levy, מהדורה 8 עמודים 22-26 (שמירה על הומאוסטזיס).
פיתרון מלא/הסבר:
חשוב לזכור
מקור
רפרנס
התפלגות תשובות
יצירת קשר
דוא"ל
תפריט מהיר
תקנון ומדיניות
- תקנון מוצרים
- תקנון מנויים
- מדיניות פרטיות
- מדיניות ביטולים
- תקנון האתר
לא ניתן להעתיק
