שאלון מערכת: שיעורי בית ביוכימיה 2
ביוכימיה 2 שאלה 1
מה מן הבאים נכון אודות אנרגיית הקישור (binding energy) המתקבלת מאינטראקציה בין אנזים לסובסטרט שלו?
במה השאלה עוסקת: קינטיקה אנזימתית.
תשובה ב’: אנרגיית הקישור (binding energy) מלווה ביצירה של הרבה קשרים חלשים בין הסובסטרט/ים שבאתר הפעיל להאנזים. אנזים המזרז ריאקציה בה מעורבים מספר סובסטרטים משתמש באנרגיית הקישור להחזקה אופטימלית שלהם זה ביחס לזה כך שהקטליזה תתבצע כמה שיותר מהר. תפיסת כל אחד מהסובסטרטים באתר הפעיל של האנזים איננה שרירותית. באנזים יש קבוצות פונקציונאליות שמיקומן שמור ותפקידן להחזיק כל אחד מהסובסטרטים בפוזיציה האידיאלית להתרחשות הקטליזה.
שלילת מסיחים:
א. האנזים יוצר באתר הפעיל שלו הרבה מאוד קשרים חלשים עם הסובסטרט, כל קשר כזה מלווה בשחרור של אנרגיה חופשית המנוצלת להורדת אנרגיית האקטיבציה. אנרגיית הקישור (Binding energy) המתקבלת מסך הקשרים שנוצרים מסבירה את העלייה החדה בקצב הריאקציה.
אנרגיית האקטיבציה היא האנרגיה הנדרשת על מנת להתגבר על המחסום האנרגטי והמאפשרת הגעה אל מצב המעבר.
חשוב לציין כי אנרגיית הקישור הגדולה שמתקבלת לא רק אחראית לעלייה החדה בקצב הריאקציה בנוכחות אנזים אלא גם לספציפיות שלו (יכולת האנזים להבחין בין הסובסטרט שלו למולקולה מתחרה). באתר הפעיל של האנזים יש קבוצות פונקציונאליות רבות במיקומים מסוימים אשר באמצעותן הוא יוצר קשרים חלשים עם הסובסטרט שלו, כל מולקולה אחרת שתהיה חסרת המאפיינים הנדרשים לא תתיישב באופן טוב באתר הפעיל.
ג. אנרגיית הקישור מתקבלת כתוצאה מיצירה של קשרים לא קוולנטיים בין האנזים לסובסטרט (אינטראקציות יוניות, הידרופוביות וקשרי מימן). שכן, יצירה של קשרים קוולנטיים ביניהם הייתה (מאוד) מייצבת את הסובסטרט ומקשה על שחרורו מהאתר הפעיל של האנזים (שבירת קומפלקס ES) והפיכתו לתוצר.
ד. מסיח זה חוזר בסגנון שלו בשאלות רבות ורצוי להיזהר ממנו – אנזימים לא משנים את קבוע שיווי המשקל של הריאקציה או את התרמודינאמיקה שלה (לאיזה כיוון תלך) אלא משנים את קצב ההגעה לשיווי המשקל.
קבוע שיווי המשקל הינו היחס בין מכפלת ריכוזי התוצרים למגיבים. שיווי משקל כימי מתאר מצב בו קצב יצירת התוצר שווה לקצב יצירת המגיב ובמצב זה האנרגיה החופשית שווה לאפס. חשוב לציין כי קבוע שיווי המשקל אינו מלמד על מהירות התגובה אלא רק על הרכב המערכת בשיווי משקל.
להרחבה –Lehninger , מהדורה שישית, עמודים 198-201
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה –Lehninger , מהדורה שמינית, פרק 6, עמודים 754-757.
ביוכימיה 2 שאלה 2
תפקיד האנזים בזירוז ריאקציות כימיות הינו:
במה השאלה עוסקת: אנזימים
תשובה ג. אנזימים הם חלבונים המזרזים ריאקציות כימיות ותפקודם הכרחי לקיומם של חיים. למעשה אנזימים מאיצים ריאקציות שמתרחשות בתא באופן ספונטני ע”י הורדת אנרגית האקטיבציה. אנרגיית האקטיבציה מסומנת כ- ‡G והיא מייצגת את המחסום האנרגטי במעבר מחומר מסוים, הסובסטרט, לחומר אחר, התוצר.
אנזימים מאיצים ריאקציות על ידי התאמת האתר הפעיל למצב המעבר של החומר ולא לסובסטרט או לתוצר. התאמה זו למצב המעבר מאפשרת להוריד את אנרגיית האקטיבציה וכך לזרז את הריאקציה. חשוב לציין שהורדת אנרגית האקטיבציה אינה משפיעה על קבוע שיווי המשקל, אשר מושפע רק מהבדלי ריכוזים בין החומרים. קבוע שיווי משקל, כשמו, מייצג מצב בו המערכת נמצאת בשיווי משקל, כלומר בנקודה יציבה שבה ריכוז החומרים נשאר קבוע. במידה והמערכת אינה נמצאת בשיווי משקל היא תשאף להגיע אליו.
קבוע שיווי המשקל מובע בנוסחא הבאה:
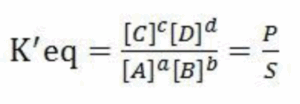
כאשר K’eq מתייחס לריאקציה בתנאים סטנדרטיים, בשונה מ-Keq שמתייחס לשיווי משקל בתנאים לא סטנדרטיים.
שלילת מסיחים
א. אנזימים אכן נקשרים בצורה הטובה ביותר לתוצר הביניים, אך הם לא מונעים ממנו לחזור חזרה לסובסטרט. אנזימים אך ורק מאיצים תהליכים וכיוון הריאקציה מושפע מההבדל בין ריכוז התוצרים למגיבים ומכמות האנרגיה במערכת. מדד שמאפשר לדעת את כיווניות הריאקציה מכונה האנרגיה החפשית של גיבס והוא לוקח בחשבון שני אלמנטים אלה.
מדד זה מובע בנוסחה הבאה:
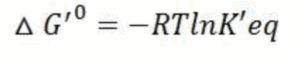
נוסחא זו מתארת מצב של תנאים סטנדרטים כאשר R הוא קבוע ו-T היא טמפרטורה קבועה. ניתן לראות כי קיים יחס הפוך בין האנרגיה החפשית ובין קבוע שיווי המשקל, כלומר K’eq חיובי מתבטא ב- 0’G△שלילי ולהפך. לפיכך, ככל שמדד האנרגיה החפשית של גיבס (0’G△) שלילי יותר, כך יש למערכת יותר נטייה להפוך את הסובטרט לתוצר (K’eq חיובי יותר, ולכן יותר תוצרים ביחס למגיבים).
ב. אנזימים אינם משפיעים על יציבות התוצר הסופי או הסובסטרט, תפקידם הוא לזרז ריאקציה שלרוב מתרחשת בתא באופן ספונטני ובקצב נמוך מהרצוי. יציבות מולקולה תלויה בתכונות הכימיות שלה ולא בפעילות האנזים. ריאקציות בהן התוצר פחות יציב מהסובסטרט, תתרחשנה בהתאם לקבוע שיווי המשקל של הריאקציה. בכדי לבצע ריאקציה זו לאחר הגעת המערכת לשיווי משקל, יש צורך באנרגיה כאשר מטבע האנרגיה הנפוץ ביותר בתא הוא Adenosine triphpspate) ATP).
ד. מסיח זה עלול לבלבל כיון שאנזימים משפיעים על אנרגית האקטיבציה, ‡G, אך לא על G .△G△ מכונה האנרגיה החפשית של גיבס אך בתנאים לא סטנדרטיים, והוא מדד לספונטניות הריאקציה בתא (בהתאם לתנאים שם). G△ נמדד על פי הנוסחה הבאה:
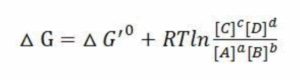
כאשר הרכיבים דומים לנוסחא של 0’G△ אך יש לשים לב שבנסוחה זו מציבים את הריכוזים בפועל, ולא את הריכוזים בשיווי משקל.
האנרגיה החפשית היא למעשה הפער בין שתי נקודות יציבות אנרגטית (סובסטרט ותוצר), בעוד שאנרגיית האקטיבציה היא המחסום האנרגטי שצריך לעבור בכדי להגיע לנקודה היציבה.
אנזימים לא משפיעים על G△ אך הם כן מורידים את אנרגית האקטיבציה.
להרחבה – Lehninger, מהדורה 6, עמודים 189-197 (אנזימטיקה).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה –Lehninger , מהדורה שמינית, פרק 6, עמודים 726-756 (אינזימטיקה).
ביוכימיה 2 שאלה 3
מי מבין ההיגדים הבאים נכון אודות קטליזה אנזימטית?
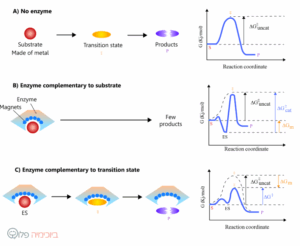
תשובה ד. אנזימים מאיצים ריאקציות שמתרחשות בתא באופן טבעי ע”י הורדת אנרגית האקטיבציה. אנרגיית האקטיבציה מסומנת כ- ‡G, והיא מייצגת את המחסום האנרגטי במעבר מחומר מסוים, הסובסטרט, לחומר אחר, התוצר. אנזימים מאיצים ריאקציות על ידי התאמת האתר הפעיל למצב המעבר של החומר ולא לסובסטרט או לתוצר. את האופן שבו אנזימים מזרזים ריאקציות ניתן לראות במנגנוני הקטליזה השונים, כמו למשל בקטליזה מסוג חומצה-בסיס. בקטליזה מסוג זה יש מעבר מימנים בין חומצות אמינו שונות באנזים, לבין הסובטרט או התוצר. חומצות אמינו בהיותן חומצות חלשות ומתפקדות כבופר בערכי PH שונים, מתאימות במיוחד לסוג כזה של קטליזה. כאשר האנזים שבאתר הפעיל שלו ישנן חומצות אמינו שמשתתפות בקטליזה ומאפשרות העברה מהירה של פרוטונים, יווצר קומפלקס עם הסובסטרט, הדבר יכול להגביר את קצב הריאקציה בכמה סדרי גודל.
שלילת מסיחים:
א. הקטליזה האנזימטית אכן תלוית pH ורואים זאת באופן הברור ביותר בקטליזה אנזימטית מסוג חומצה-בסיס. כיון שבקטליזה מסוג זה יש שימוש בהעברת פרוטונים, ערכי ה-pH צריכים להיות מתאימים בכדי לאפשר את הריאקציה. חומצות אמינו שונות מתפקדות כתורמות או מקבלות פרוטונים וזאת בהתאם לרקמה ול-pH שקיים בסביבת הפעולה של האנזים.
חשוב להכיר מנגנונים נוספים של קטליזה אנזימטית: קטליזה קוולנטית, קטליזת יון מתכת וקטליזה אלקטרוסטטית. בקטליזה קוולנטית האנזים יוצר קשר קוולנטי זמני עם הסובסטרט. בקטליזת יון מתכת ישנו שימוש ביוני מתכת הקשורים לאנזים או נמצאים בתמיסה ובקטליזה אלקטרוסטטית יש ייצוב של מצב הביניים באמצעות קשרים יוניים.
ב. אנזימים הינם סטריאוספציפיים (stereospecific), כלומר הם מגיבים רק עם איזומר (isomer) אחד מתוך השניים. החשיבות של הספציפיות של אנזימים נובעת מכך שבכדי שהם יורידו את אנרגית האקטיבציה באופן משמעותי, הם צריכים להיקשר בחוזקה למצב המעבר. קשירה זו למצב המעבר מחייבת את האנזימים להיות ספציפיים מאוד, אפילו כלפי איזומרים שונים של מולקולה. מושג המוכנה אנרגית הקשר, GB△, מתאר את ההפרש בין אנרגית האקטיבציה ללא אנזים (G‡uncat△) לאנרגיית האקטיבציה עם אנזים (G‡cat△). כאמור אנרגית הקשר היא תוצאה של ספציפיות האנזים והיא נוצרת לרוב מהרבה אינטרקציות חלשות בין האנזים לסובסטרט שמייצבות את הקומפלקס.
ג. אנזימים אינם משפיעים על קבוע שיווי המשקל אלא על קצב הריאקציה בלבד. שיווי משקל תלוי בריכוזם של התוצר והסובסטרט והוא מובע בנוסחא הבאה:
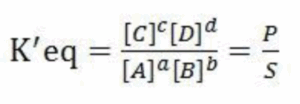
כאשר K’eq מתייחס לריאקציה בתנאים סטנדרטיים, בשונה מ-Keq שמתייחס לשיווי משקל בתנאים לא סטנדרטיים. לכל חומר יש K’eq קבוע ואילו Keq (כלומר שיווי משקל בתנאים לא סטנדרטיים) תלוי בריכוזי החומרים הספציפי.
להרחבה – Lehninger, מהדורה 6, עמודים (189-200).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה –Lehninger , מהדורה שמינית, פרק 6, עמודים 736-738, 762-769 (מנגנונים נוספים של קטליזה אינזימטית).
ביוכימיה 2 שאלה 4
מי מבין ההיגדים הבאים אודות ריאקציות אנזימטיות שגוי?
במה השאלה עוסקת: קינטיקה אנזימטית
תשובה ג. מהירות ריאקציה תלוי באנרגיית השפעול של התגובה. אנרגיית השפעול מהווה מחסום אנרגטי שיש להתגבר עליו – ככל שהמחסום יהיה גבוה יותר, כך יהיה קשה להתגבר עליו ולכן קצב הריאקציה יהיה איטי יותר. אנזימים מורידים את אנרגיית השפעול של ריאקציות ובכך מאיצים את קצב הריאקציה. קבוע שיווי המשקל מתייחס ליחס שבין התוצרים למגיבים בשיווי משקל וערך זה איננו מושפע מקצב הריאקציה. אנזימים מזרזים את הזמן הדרוש להגיע לשיווי משקל אך אינו משנים את שיווי המשקל עצמו. כדאי לדעת שקבוע שיווי המשקל משתנה כאשר הטמפרטורה משתנה.
שלילת מסיחים:
א. כאשר ריכוז הסובסטרט מספיק גבוה, ריכוז האנזים הופך לגורם המגביל את קצב הריאקציה. לכן, במצב זה קצב הריאקציה יהיה תלוי בריכוז האנזים ובקבוע הקצב:
([kcat (Vmax = kcat*[Et.
ב. מעכב תחרותי נקשר לאתר הפעיל של האנזים ולכן מפריע לסובסטרט להיקשר למקומו. ככל שריכוז הסובסטרט יהיה גבוה יותר מריכוז המעכב כך עולה הסבירות שהאנזים יקשור סובסטרט ויהפוך אותו לתוצר. לכן, כאשר ריכוז הסובסטרט מספיק גבוה מריכוז המעכב, האנזימים יכולים להגיע למהירות המקסימלית.
ג. ערך Km מורכב מקבועי הקצב המפרקים קומפלקס ES (במונה), ויוצרים קומפלקס ES (במכנה). ערך Km נמדד ביחידות ריכוז (כמו הסובסטרט), ולמעשה מהווה את הריכוז בו חצי מהאנזימים קושרים סובסטרט – הנקודה בה מגיעים לחצי מהמהירות המקסימלית. ניתן לראות זאת גם לפי משוואת מיכאליס מנטן: (]Vo=(Vmax*[S])/(Km+[S כאשר S]=Km], ניתן להציב את [S] במקום Km ונקבל: Vo=(Vmax*[S])/2[S]=Vmax/2.
להרחבה – Lehninger, מהדורה שישית, עמוד 192-194 (Enzymes Affect Reactions Rates, Not Equilibria).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמוד 737-744 (Enzymes Affect Reactions Rates, Not Equilibria).
ביוכימיה 2 שאלה 5
מודל מיכאליס-מנטן נבנה עבור הריאקציה הכוללת כמתואר למטה. על פי משוואה זו, ניתן לתאר את קצב פירוק קומפלקס האנזים-סובסטרט ע”י מי מבין הביטויים הבאים?
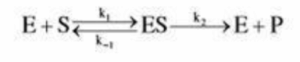
במה השאלה עוסקת: מודל מיכאליס מנטן
תשובה ד. מודל מיכאליס מנטן מתאר קינטיקת אנזימים בהתאם לריכוזי סובסטרט שונים. לפי המודל, ריכוז האנזים נשאר קבוע והמהירות ההתחלתית היא פונקציה של ריכוז סובסטרט משתנה. אנזימים יכולים להיות כקומפלקס יחד עם הסובסטרט (ES) או חפשיים. כדי לתאר את קצב פירוק הקומפלקס ES אנחנו צריכים להתייחס הן לפירוק הקומפלקס לאנזים ותוצר (E+P) והן לחזרתו לאנזים וסובסטרט (E+S). הפירוק לאנזים ותוצר מתואר על ידי מכפלת הקומפלקס ES בקבוע הקצב k2 והפירוק לאנזים וסובסטרט מתואר על ידי מכפלת ES בקבוע הקצב k-1. קבוע הקצב הנוסף הוא k1 והוא מתאר את היווצרות הקומפלקס ES ולכן אינו רלוונטי לשאלה זו. קבוע הקצב k-2 שמתאר את החזרה מאנזים ותוצר לקומפלקס ES לא נלקח בחשבון במודל מיכאליס מנטן, תחת ההנחה שההשפעה שלו זניחה.
שלילת מסיחים:
א. ביטוי זה מתאר את קצב היווצרות ES כיון שהוא כופל את קבוע הקצב k1 בכלל האנזים החופשי. כלל האנזים החופשי מחושב על ידי חיסור כמות האנזימים שמחוברים לסובסטרט מכלל האנזימים במערכת (Etotal-ES). כיון שאנו מחפשים את קצב פירוק הקומפלקס ולא את קצב הרכבתו, מסיח זה נפסל.
ב. מסיח זה גם מתייחס לאנזים חופשי ולכן אינו מתאר נכונה את פירוק הקומפלקס. בנוסף הוא מתאר רק את הפירוק חזרה לכיוון אנזים וסובסטרט וחסר גם הביטוי שמתאר את הפירוק לכיוון התוצרים.
ג. מסיח זה מתאר נכונה רכיב מסוים של פירוק הקומפלקס, אך הוא מזניח את הפירוק חזרה לכיוון הסובסטרט ולכן שגוי.
להרחבה – Lehninger, מהדורה 6, עמודים 200-203 (קינטיקה של אנזימים).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמודים 776-778 (משוואת מיכאליס מנטן).
ביוכימיה 2 שאלה 6
מי מבין ההיגדים הבאים אודות הגרף המקשר בין המהירות ההתחלתית (V0) לריכוז הסובסטרט [S] עבור אנזים הפועל על פי עקומת מיכאליס-מנטן, הינו שגוי?
במה השאלה עוסקת: קינטיקה אנזימטית
תשובה ב. בעקומת מיכאליס מנטן מתקבלת עקומה היפרבולית, כאשר ציר x מתאר את ריכוז הסובסטרט וציר y את מהירות הריאקציה. בהתחלה, ככל שמעלים את ריכוז הסובסטרט כך קצב הריאקציה עולה, עד נקודה מסוימת בא כל האנזימים מגיעים לרוויה ומקבלים עקומה לינארית. בעקומת מיכאליס מנטן אין נקודת חיתוך עם ציר ה-y. בנוסף, Km נמצא על ציר ה-x ומהווה את ריכוז הסובסטרט בו חצי מהאנזימים תפוסים בסובסטרט (הריכוז בו קצב הריאקציה הוא חצי מהמהירות המקסימלית).
שלילת מסיחים:
א. בעקומת מיכאליס מנטן ככל שמעלים את ריכוז הסובסטרט כך המהירות ההתחלתית עולה, עד נקודה מסוימת בה כל האנזימים רוויים ואז מהירות הריאקציה אינה משתנה כתלות בריכוז הסובסטרט. מסיח זה אמנם אינו מפרט עד הסוף, אך ישנו מסיח אחר אשר שגוי באופן מוחלט, ולכן מסיח זה נפסל (כלומר – מסיח זה נכון).
ג. ערך Km מורכב מקבועי הקצב המפרקים קומפלקס ES (במונה), ויוצרים קומפלקס ES (במכנה). ערך Km נמדד ביחידות ריכוז (כמו הסובסטרט), ולמעשה מהווה את הריכוז בו חצי מהאנזימים קושרים סובסטרט – הנקודה בה מגיעים לחצי מהמהירות המקסימלית. ניתן לראות זאת גם לפי משוואת מיכאליס מנטן: ([Vo=(Vmax*[S])/(Km+[S כאשר S]=Km], ניתן להציב את [S] במקום Km ונקבל: Vo=(Vmax*[S])/2[S]=Vmax/2.
ד. בעקומת מיכאליס מנטן, ציר ה-y הינו מהירות הריאקציה. מהירות הריאקציה נמדדת ביחידות של ריכוז/זמן. M זהו ריכוז במולאר, ו-min מתייחס לדקות.
להרחבה – Lehninger, מהדורה שישית, עמוד 201 (Figure 6-11).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמוד 773 (Figure 6-12).
ביוכימיה 2 שאלה 7
בריאקציות אנזימטיות בהן שלב מגביל המהירות הינו ES–>P, יהיה Km שווה בקירוב ל:
במה השאלה עוסקת: קינטיקה אנזימתית
תשובה ג. נוסחא שיש להכיר בעל פה לבחינה הינה הנוסחא שמתארת את Km:
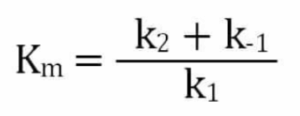
במידה ונתון כי השלב מגביל מהירות (השלב האיטי) הוא שלב פירוק הקומפלקס ES לאנזים ולתוצר אנחנו יכולים להזניח את ערך K2 מהביטוי של Km בטענה ש- K-1>>K2 ואז Km שווה בקירוב ל- K-1/K1. הביטוי המקורב הוא למעשה קבוע הדיסוציאציה ונקרא Kd (או Ks). היות ואנחנו יכולים לומר ש- Km שווה בקירוב לביטוי זה אז הוא יכול להוות מעין אומדן לאפיניות שבין האנזים לסובסטרט.
הערת מחבר – Kd הינו קבוע הדיסוציאציה של הקומפלקס ES. הקבוע מתאר את הפרדת הקומפלקס אנזים סובסטרט לאנזים ולסובסטרט לחוד. המונה מתאר את פירוק קומפלקס ES והמכנה את בנייתו. לכן, ככל ש- Kd קטן יותר כך האפיניות גבוהה יותר (מכנה גדול יותר ולכן קצב פירוק קטן יותר) ולהיפך – Kd גדול אומר כי המונה גדול יותר ולכן קצב פירוק גדול יותר.
שלילת מסיחים :
א. כאשר נתון כי שלב מסוים הוא מגביל מהירות ניתן להניח כי קבוע הקצב המאפיין אותו הוא נמוך וניתן להזניחו במקרים רבים. מסיח א’ מזניח את K-1 שהרבה יותר גדול מ- K2 ולכן לא אפשרי.
ב. בנקודה בה המהירות היא מקסימלית הסובסטרט ברוויה וריכוזו לא משפיע על מהירות האנזים, זוהי ריאקציה מסדר 0. באופן כללי, ערך Km לא תלוי כלל בריכוז האנזים או בריכוז הסובסטרט.
ד. מספר מולקולות הסובסטרט ההופכות על ידי האנזים לתוצר ביחידות זמן הוא הקבוע הקטליטי K2 (השלב האיטי של הריאקציה/ מגביל המהירות הוא השלב הקובע קצב), כדי למצוא אותו יש לחלק את המהירות המקסימלית בכמות האנזים – נקבל כמה תוצרים נוצרו על ידי אנזים אחד בשניה אחת (כמה מולקולות סובסטרט הפכו לתוצר בשניה אחת על ידי אנזים אחד).
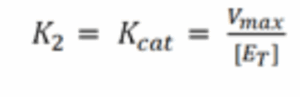
להרחבה – Lehninger, מהדורה שישית, עמודים 204-207.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמודים 785-786 .
ביוכימיה 2 שאלה 8
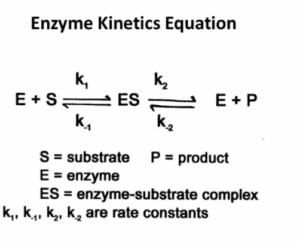
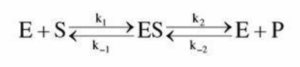
על פי הסכמה הנתונה להלן, הנוגעת לריאקציה אנזימטית כללית, מה נכון עבור המצב בו הקומפלקס אנזים- סובסטרט (ES) נמצא במצב עמיד (steady state)?
במה השאלה עוסקת: קינטיקה אנזימטית
תשובה ג. במצב עמיד ריכוז קומפלקס אנזים-סובסטרט (ES) נשאר קבוע עקב כך שקצב הרכבת קומפלקס ES שווה לקצב פירוק קומפלקס ES (מצב עמיד שונה משיווי משקל בכך שבש”מ מדובר בריאקציה שהולכת קדימה ואחורה בו זמנית). הרכבת קומפלקס ES תלויה בריכוז המגיבים וקבוע הקצב k1: Vo= k1*[E][S]. פירוק קומפלקס ES תלוי בשתי ריאקציות: פירוק קומפלקס ES חזרה למגיבים (Vo=k-1[ES]) ופירוק קומפלקס ES לתוצר (Vo=k2*[ES]). מכיוון שקצב הרכבת הקומפלקס שווה לקצב הפירוק נקבל: k1[E][S]=k-1[ES]+k2[ES]
שלילת מסיחים:
א. מצב עמיד מתייחס לריכוז קומפלקס ES ולא רק לקבועי הקצב. ובנוסף, מלבד k1 היוצר את קומפלקס ES ו-k2 המפרק את קומפלקס ES, גם k-1 מעורב בפירוק קומפלקס ES. מלבד זאת, k1 הוא בהרבה יותר מהיר מ-k2. קבוע הקצב k2 הוא בהרבה מקרים שלב קובע מהירות של ריאקציות אנזימטיות.
ב. מצב עמיד מתייחס לריכוז קומפלקס ES ולא רק לקבועי הקצב. ובנוסף, מלבד k1 היוצר את קומפלקס ES ו-k-1 המפרק את קומפלקס ES, גם k2 מעורב בפירוק קומפלקס ES.
ד. מצב עמיד מתייחס לסך הגורמים המובילים להרכבה ופירוק של קומפלקס ES. במשוואה במסיח זה אין התייחסות ל-k2[ES], שזהו שלב נוסף המוביל לפירוק קומפלקס ES ולכן מסיח זה נפסל.
להרחבה – Lehninger, מהדורה שישית, עמוד 202-203 (The Relation Between Substrate Concentration and Reaction Rate)
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמודים 776-781 (The Relation Between Substrate Concentration and Reaction Rate).
ביוכימיה 2 שאלה 9
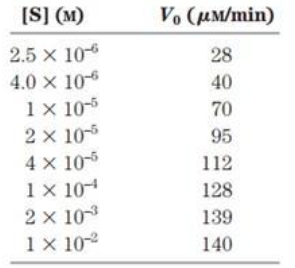
חוקר בדק את הקינטיקה של אנזים מסוים ואסף את התוצאות שלפניך. מה הוא ערך Km המוערך של האנזים?
במה השאלה עוסקת: קינטיקה אנזימתית
תשובה ג. Km נמדד ביחידות של ריכוז מולר (molar) ומתאר את ריכוז הסובסטרט הדרוש כדי להגיע לחצי מהמהירות המקסימאלית, כלומר ריכוז הסובסטרט בנקודה בה V0=1/2Vmax. מנתוני השאלה ניתן לראות שהמהירות המקסימלית שנמדדה היא 140μM/min ולכן חצי מהמהירות המקסימלית היא באזור 70μM/min, ריכוז הסובסטרט בנקודה זו הוא 1×10^-5 וזה גם ערך ה- Km.
הרחבה – באופן כללי, יש תלות בין המהירות ההתחלתית של הריאקציה לריכוז הסובסטרט –
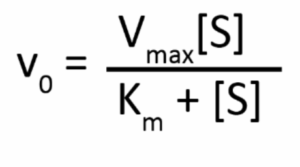
וישנם שלושה מצבים :
א. כאשר [Km>>[S (בריכוז סובסטרט נמוך מאוד) יש תלות לינארית בין ריכוז הסובסטרט למהירות ההתחלתית של הריאקציה, V0=Vmax[S]/Km.
ב. כאשר S]=Km] יש חצי אוכלוסייה רוויה בסובסטרט, במצב זה מהירות הריאקציה שווה למחצית מהמהירות המקסימאלית, V0=1/2Vmax.
ג. כאשר [Km<<[S (בריכוז סובסטרט גבוה מאוד) האנזים יעבוד תמיד במהירות המקסימאלית שלו ללא תלות בריכוז הסובסטרט (סובסטרט ברוויה לא משפיע על מהירות האנזים), V0=Vmax.
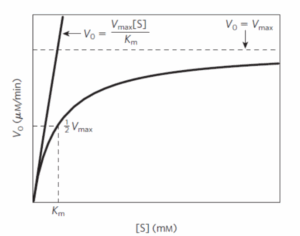
(מקור התמונה – figure 6-12, page 203) / (מקור התמונה – מהדורה 8 figure 6-13, page 780)
להרחבה – Lehninger, מהדורה שישית, עמודים 202-203.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמודים 780-781.
ביוכימיה 2 שאלה 10
עבור אנזים מסוים קומפלקס ES מתפרק לתוצר משמעותית מהר יותר מאשר פירוק קומפלקס ES חזרה למגיב. מה ניתן להסיק לגבי Km?
במה השאלה עוסקת: קינטיקה אנזימטית
תשובה ד. ערך Km מורכב מקבועי הקצב העיקריים בריאקציה האנזימטית, כאשר המונה מורכב מקבועי הקצב אשר מפרקים את קומפלקס ES (k-1 + k2) והמכנה מורכב מקבוע הקצב היוצר את קומפלקס ES (k1). כאשר אחד מקבועי הקצב במונה גדול משמעותית מקבוע הקצב השני, ניתן להזניח את קבוע הקצב הקטן. לכן, כאשר נתון שפירוק קומפלקס ES לתוצר מתרחש משמעותית מהר יותר מאשר פירוק קומפלקס ES חזרה למגיבים ניתן להסיק כי k2>>k-1. במצב זה נזניח את k-1 ממשוואת Km ונקבל Km = k2/k1.
שלילת מסיחים:
א. קבוע הדיסוציאציה בהגדרה מתקבל מהיחס בין קבוע קצב הריאקציה אחורה לבין קבוע הקצב של הריאקציה קדימה (k-1/k1). כאשר k-1>>k2 ערך Km יהיה שווה ל-Km = k-1/k1. מצב זה מסמל את קבוע הדיסוציאציה. בשאלה נתון כי k2>>k-1 ולכן מסיח זה נפסל.
ב. זהו קבוע הדיסוציאציה והוא מתקבל כאשר k-1>>k2. בשאלה נתון כי k2>>k-1 ולכן מסיח זה נפסל.
ג. ערך Km מהווה מדד לאפיניות כאשר Km שווה לקבוע הדיסוציאציה. לכן, מסיח זה נפסל.
להרחבה – Lehninger, מהדורה שישית, עמודים 203-204(Kinetic Parameters)
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמודים 785-786.
ביוכימיה 2 שאלה 11
איזה מבין ההיגדים הבאים מתאר נכונה את ההשפעה של ריכוז האנזים על Km ו-Vmax של הריאקציה אותה הוא מזרז?
במה השאלה עוסקת: קינטיקה אנזימתית, מודל מיכאליס-מנטן.
תשובה ד’. ריכוז האנזים (Et) משפיע ביחס ישר על המהירות המקסימלית, Vmax, של ריאקציה אנזימתית שמצייתת למודל מיכאליס-מנטן, כפי שמתבטא במשוואה:
Vmax=Kcat*Et
ערך Kcat הוא קבוע הקטליזה ומבטא את השלב קובע המהירות במודל מיכאליס-מנטן שהוא המעבר בין הקומפלקס ES ל-E+P. ערך Kcat הינו קבוע אשר אופייני לכל אנזים.
נזכר גם כי בריכוזי סובסטרט גבוהים מאוד ([S]>>Km) הגורם המגביל את הריאקציה האנזימטית הוא ריכוז האנזים. לכן, ככל שריכוז האנזים יהיה יותר גבוה כך יהיו יותר אנזימים שיוכלו להפוך סובסטרט לאנזים, ומכאן שנגדיל את המהירות המקסימלית.
ערך Km,קבוע מיכאליס מנטן, אינו קשור לריכוז האנזים הכולל. זהו גודל אינטרינזי לריאקציה האנזימתית המווה את ריכוז הסובסטרט בו מהירות הריאקציה תהיה חצי מקסימלית. כאשר k2<<k-1 ערך Km שווה לאפיניות בין הסובסטרט לאנזים מכיוון שהוא שווה לקבוע הקצב עבור הריאקציה של פירוק קומפלקס ES (k-1) חלקי קבוע הקצב עבור הריאקציה של הרכבת קומפלקס (k1) ES.היחס בין קבועי קצב אלו הוא קבוע הדיסוציאציה (Kd).
שלילת מסיחים:
א.ריכוז האנזים אמנם לא משפיע על ערך Km אך הוא משפיע על ערך Vmax כפי שהוסבר.
ב. ריכוז האנזים אמנם משפיע על Vmax אך הוא אינו משפיע על ערך Km.
ג. כאמור ריכוז האנזים לא משפיע על Km ומשפיע ביחס ישר על Vmax.
להרחבה: Lehninger 6th edition ע”מ 204-205
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה – Lehninger, מהדורה שמינית, פרק 6, עמודים 785-789.
ביוכימיה 2 שאלה 12
חוקרים בדקו את הפעילות של אנזים מסויים. בניסוי ראשון הם הפעילו את האנזים בנוכחות ריכוז סובסטרט השווה ל-Km של האנזים. בניסוי השני הפעילו החוקרים את האנזים בנוכחות ריכוז סובסטרט גדול פי 100 מערך ה-Km של האנזים. איזה מהבאים מתאר נכונה את ההבדל במהירות התגובה Vo בין הניסוי הראשון לשני?
במה השאלה עוסקת: קינטיקה אנזימתית, מודל מיכאליס-מנטן.
תשובה ב’. לפי מודל מיכאליס-מנטן Km שווה לריכוז הסובסטרט שבו מהירות הריאקציה האנזימתית שווה לחצי Vmax. כלומר, ברגע שריכוז הסובסטרט גבוה מערך Km, ולא משנה בכמה, מהירות הריאקציה יכולה לגדול לכל היותר פי 2 עד ההגעה ל-Vmax.
שלילת מסיחים:
א. מהירות הריאקציה, Vo,תמשיך לעלות לאחר שריכוז הסובסטרט עבר את Km עד הגעה ל – Vmax ואז המהירות תישאר קבועה למרות העלאת ריכוז הסובסטרט. ברגע שריכוז הסובסטרט מספיק גבוה האנזים הופך להיות הגורם המגביל עבור אותה ריאקציה אנזימטית. ניתן לראות זאת במשוואת מיכאליס מנטן כאשר [S]>>Km.במצב זה, המהירות ההתחלתית שווה למהירות המקסימלית.
ג. כאמור, מהירות הריאקציה יכולה לגדול לכל היותר פי 2 כאשר ריכוז הסובסטרט עובר את ריכוז Km.
ד. כאשר ריכוז הסובסטרט שווה לערך Km זו הנקודה בה המהירות שווה לחצי המהירות המקסימלית. כאשר נעלה מספיק את ריכוז הסובסטרט ניתן להגיע למהירות של פי 1.5 וניתן גם לעבור מהירות זו עד פי 2 מהמהירות החצי המקסימלית, כפי שהוסבר.
להרחבה: Lehninger 6th edition עמודים202-203 (The Relation Between Substrate Concentrationand Reaction Rate)
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger, מהדורה שמינית, פרק 6, עמודים 780-781.
ביוכימיה 2 שאלה 13
נתונים שני אנזימים: אנזים A הוא בעל קבוע הקטליזה, Kcat, של:
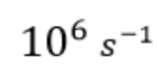
לעומת זאת קבוע הקטליזה של אנזים B הוא:
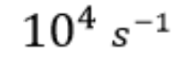
על סמך נתונים אלה, איזה מבין ההיגדים הבאים נכון?
במה השאלה עוסקת: קינטיקה אזימתית, מודל מיכאליס-מנטן.
תשובה ב’. על מנת לענות על השאלה עלינו להכיר את ההגדרה של Kcat (קבוע הקטליזה). Kcat למעשה מתאר את השלב קובע המהירות במודל מיכאליס-מנטן של מעבר מקומפלקס ES לאנזים חופשי ותוצר (E+P). ככל ש-Kcat גדול יותר, כך האנזים יבצע שלב זה במהירות גדולה יותר, ומכיוון שזה השלב קבוע המהירות, ה-Vmax שלו יהיה גדול יותר, כלומר Vmax תלוי ביחס ישר ב-Kcat. ההגדרה של Kcat אם כן היא:
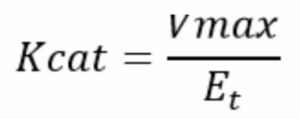
כאשר Et הוא ריכוז האנזים הכולל. מהגדרה זו אנו למדים ש-Kcat יהיה גדול יותר ככל שהאנזים יכול להגיע ל-Vmax גדול יותר בריכוז אנזים קטן יותר.
חזרה לשאלה – נותנים לנו שני אנזימים כאשר ההבדל בין ה-Kcat שלהם הוא בסדר גודל של פי 100. לפי הגדרת Kcat אנו יודעים שהאנזים שה-Kcat שלו קטן פי 100 ידרש לפי 100 יותר אנזים על מנת להגיע לאותו Vmax כמו האנזים שה-Kcat שלו גדול פי 100.
שלילת מסיחים:
א. כפי שראינו ההפך הוא הנכון. לאנזים A ה-Kcat הגדול יותר ולכן הוא נדרש לפחות אנזים כדי להגיע ל-Vmax כלשהו.
ג. אין קשר בין ריכוז הסובסטרט ל-Kcat. זהו גודל אינטרינזי של האנזים.
ד. כאמור לא נכון. ע”י הגדלת ריכוז האנזים ניתן להעלות את ה-Vmax ביחס ישר.
להרחבה: Lehninger 6th edition, ע”מ 204-205
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמודים 787-789.
ביוכימיה 2 שאלה 14
מה נכון לגבי אנרגיית השפעול?
תשובה: ב’ (אנרגיית השפעול נמוכה יותר בכיוון האקסרגוני של התגובה). אנזימים יכולים לזרז ריאקציות בשני הכיוונים (מהמגיבים לתוצרים, ומהתוצרים למגיבים). בריאקציה אקסרגונית (משחררת אנרגיה) אנרגיית הסובסטרט גבוהה מאנרגיית התוצר, ולכן ההפרש בין הסובסטרט לאנרגית השפעול נמוך יותר מאשר אנרגיית התוצר לאנרגיית השפעול.
שלילת מסיחים:
א. אנרגיית השפעול מהווה מחסום אנרגטי שיש להתגבר עליו על מנת שהריאקציה תתרחש, לכן, ככל שאנרגיית השפעול תהיה נמוכה יותר כך התגובה תהיה מהירה יותר.
ג. אנרגיית השפעול משפיעה על קצב התגובה ואיננה מעידה על העדפה האנרגטית של הריאקציה. תתכן ריאקציה אקסרגונית עם אנרגיית שפעול גבוהה – כגון תגובות שריפה (חומר אורגני + חמצן = CO2 + מים) או פירוק הקשר הפפטידי.
ד. האנזים נקשר לסובסטרט בקשרים חלשים והאנרגייה המשתחררת מקישור הסובסטרט היא זו שמאפשרת להוריד את אנרגיית השפעול. ייתכן והאנזים ייקשר קוולנטית לסובסטרט אך זה אינו נחוץ בכל האנזימים.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמוד 739 (Figure 6-2).
ביוכימיה 2 שאלה 15
עבור ריאקציה אנזימטית מסוימת k2>>k-1. מה ניתן לומר על Km במקרה זה?
תשובה: ד’ (שלב ES E + S זניח בריאקציה זו). ערך Km מורכב מקבועי הקצב אשר מתארים את פירוק קומפלקס ES (k-1 ו-k2) וקבוע הקצב שמתאר את הרכבת קומפלקס ES (k1). המשוואה: Km = (k-1 + k2)/k1. כאשר אחד מקבועי הקצב במונה גדול משמעותית מקבוע הקצב השני (במקרה שלנו k2>>k-1), ניתן להזניח את קבוע הקצב הקטן (במקרה זה- k-1). לפי כך ניתן להבין שהשלב אותו k-1 מתאר (ES E + S) הינו זניח בריאקציה האנזימטית המדוברת.
שלילת מסיחים:
א. Km שווה לקבוע הדיסאוציאציה קשר k-1>>k2 ובמצב זה יתקבל Km = k-1/k1 (שזהו גם התיאור של קבוע הדיסאוציאציה)
ב. במקרה המדובר בשאלה ניתן להזניח את k-1 ולכן ערך Km יהיה שווה ל- k2/k1
ג. Km מעיד על זיקה בין אנזים לסובסטרט כאשר k-1>>k2 ובמצב זה יתקבל Km=k-1/k1 (שזהו גם התיאור של קבוע הדיסאוציאציה)
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמודים 785-786.
ביוכימיה 2 שאלה 16
Kcat/Km:
תשובה: ג’ (גודלו מוגבל ביכולת הדיפוזיה של האנזים והסובסטרט). Kcat/Km מתאר את מידת יעילות האנזים: שני הגורמים המשפיעים על היעילות היא יכולת קישור הסובסטרט (Km) ויכולת הפיכת הסובסטרט לתוצר (Kcat – הזירוז האנזימטי). ככל ש-Km קטן יותר וככל שKcat גבוה יותר כך האנזים יהיה יותר אפקטיבי. עם זאת, יעילות האנזים מוגבלת ע”י קצב הדיפוזיה של האנזים והסובסרט יחד בתמיסה. אנזימים בעלי יעילות הקרובה לקבוע הדיפוזיה (108-109 M-1S-1) נחשבים כאנזימים שהגיעו לשלמות קטליטית. דוגמה לכך הם האנזימים פומראז (Fummarase), קטאלאז (Catalase), וקרבוניק אנהידראז (Carbonic Anhydrase).
שלילת מסיחים:
א. המדד לזיקה בין האנזים לסובסטרט הוא Km כאשר k-1>>k2
ב. ערכים גבוהים מעידים על יעילות גבוהה של האנזים – גם בקישור הסובסטרט וגם בזירוז הריאקציה האנזימטית
ד. Km אינו משפיע על מהירות הקטליזה אלא על קישור הסובסטרט לאנזים.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמודים 788-789.
ביוכימיה 2 שאלה 17
כחלק מחקר קינטיקה אנזימטית, העמידו מספר מערכות ריאקציה שבכל מבחנה נמצא אנזים X בריכוז אחר. מה צפוי להיות ההבדל בין הריאקציות?
תשובה: ג’ (חצי המהירות המקסימלית תהיה שונה בכל מבחנה). לפי משוואת מיכאליס מנטן, המהירות המקסימלית מתקבלת במצב בו [S]>>Km בה המשוואה היא Vo=Vmax=k2*[E]. לכן, ככל שריכוז האנזים יעלה כך ערך Vmax יעלה גם כן. כתוצאה מכך – גם ערך חצי המהירות המקסימלית יעלה. ככל שיש יותר אנזים חופשי במבחנה כך הסבירות שיפגוש סובסטרט גבוה יותר, ובנוסף יש יותר אנזימים שיכולים לזרז את הריאקציה כך שהמערכת תגיע לרוויה בשלב מאוחר יותר.
שלילת מסיחים:
א. שינוי ריכוז האנזים מוביל לשינוי במהירות הריאקציה, אך אינו משפיע על ערך Km.
ב. שינוי בריכוז האנזים מוביל לשינוי במהירות הריאקציה
ד. שינוי בריכוז האנזים אינו מוביל לשינוי בערך Km, אך העלאת ריכוז האנזים תוביל לעלייה במהירות המקסימלית.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמודים 772-773.
ביוכימיה 2 שאלה 18
מדוע ניתן להניח את הנחת המצב היציב?
תשובה:ב.
הסבר על מנת לחשב את הקינטיקה האנזימתית, אנו צריכים להניח מספרהנחות. הנחת המצב היציב אומרת שהקצב בו נוצר קומפלקס אנזים סובסטרט (ES) זהה לקצב הפירוק שלו ואנו יכולים להניח זאת בגלל שבתחילת הריאקציה, כמות הסובסטרט גדולה בהרבה מכמות האנזים, כלומר כל האנזים תפוס ע”י הסובסטרט וכמות האנזים החופשי זניחה.
שלילת מסיחים:
א– זאת הסיבה לכך שאנחנו צריכים את הנחת המצב היציב, אך לא מסביר מדוע ניתן להניח אותה.
ג– יש קשר – ככל שיש לי יותר סובסטרט כך נוצר פחות אנזים חופשי. מכאן, הנחה נוספת בקינטיקה אנזימתית, לא קיים אנזים חופשי בתחילת הריאקציה וכמות קומפלקסים ES זהה לכמות האנזים הכללית.
ד– זהו המצב ההפוך.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמודים 777-778.
ביוכימיה 2 שאלה 19
מה תהיה ההשפעה של הורדת כמות האנזים על קינטיקת מיכאליס מנטן?
תשובה: ד
על מנת לחשב Vmax, אנו משתמשים בנוסחא Vmax=k2*E. אם מורידים את כמות האנזים, אנו נצפה בירידה ב-Vmax.
אנו יכולים גם לדמיין את המצב – המהירות המקסימלית נמדדת ע”י כמות התוצאים הנוצרים. אם יש פחות אנזים על אותה כמות סובסטרט, נצפה בפחות תוצרים חדשים, כלומר המהירות תרד.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמודים 779-780.
ביוכימיה 2 שאלה 20
למטה מתוארת ריאקציה כלשהי. האנזים המזרז ריאקציה זו יכול להיות מוגדר כ:
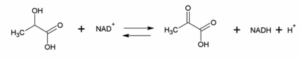
במה עוסקת השאלה: אנזימים, טרמינולוגיה.
תשובה ב’. מתוארת ריאקציה של הפיכת לקטאט לפירובאט ולהפך. זו ריאקצית חמצון חיזור שבה NADH משמש כמחזר ופירובאט כמחמצן.
נעבור על המסיחים:
א. לא נכון. טרספרז הוא אנזים שמעביר קבוצה פונקציונאלית מסוימת בין מולקולות, מה שלא קיים בריאקציה הזאת.
ב. נכון. אוקסידורדוטאז הוא אנזים שמשתתף בריאקציות חמצון-חיזור בהן יש מעבר אלקטרונים, כמו בריאקציה המתוארת. אנזימים שנקראים דהידרוגנאזות או רדוקטאזות או אוקסידזות שייכים לקבוצה זו.
ג. לא נכון. הידרולאזות אלו אנזימים שמפרקים קשרים באמצעות החדרת מולוקולת מים. לדוגמא : פפטידזות או גלוקוזידזות.
ד. לא נכון. איזומרזות אלו אנזימים שהופכים את הסובסטרט לאיזומר שלו. לא קיים בתגובה המתוארת.
להרחבה: lehninger 6th edition, ע”מ 190-191
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמוד 734 (Table 6-3).
ביוכימיה 2 שאלה 21
איזו חומצה אמינית נצפה למצוא בחלק הפנימי של חלבון גלובולרי?
תשובה ד. חלבונים מסיסים במים, שהינם חומר פולארי. מסיבה זו, שיירים פולארים בחלבון יפנו לחלק החיצוני של החלבון, שם יבואו במגע עם מולקולות מים, בעוד שיירים הידרופובים יפנו לחלק הפנימי של החלבון – ובצורה זו ימנעו ממגע עם מים. מבין המסיחים הקיימים, ואלין היא החומצה האמינית ההידרופובית היחידה, ולכן השייר של ח”א זו יפנה לחלק הפנימי של החלבון.
שלילת מסיחים:
א. ארגינין זו חומצה אמינית טעונה חיובית. חומר טעון הוא בהכרח פולארי, ולכן השייר של ארגינין יכול לבוא במגע עם מים. מסיבה זו, ארגינין תפנה לחלק החיצוני של החלבון.
ב. אספרטט זו חומצה אמינית טעונה שלילית. חומר טעון הוא בהכרח פולארי, ולכן השייר של אספרטט יכול לבוא במגע עם מים. מסיבה זו, אספרטט תפנה לחלק החיצוני של החלבון.
ג. גלוטמאט זו חומצה אמינית טעונה שלילית. חומר טעון הוא בהכרח פולארי, ולכן השייר של גלוטמאט יכול לבוא במגע עם מים. מסיבה זו, גלוטמאט תפנה לחלק החיצוני של החלבון.
להרחבה – Lehninger, מהדורה שישית, עמוד 577-579 (The Non Oxidative Phase Recycles Pentose Phosphates to Glucose-6-Phosphate).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: המבנה של חלבונים.
להרחבה – Lehninger, מהדורה שמינית, פרק 4, עמוד 482.
ביוכימיה 2 שאלה 22
מה נכון לגבי קשר פפטידי?
במה השאלה עוסקת: קשר פפטידי
תשובה א. בקשר הפפטידי ישנם שני מרכזים עשירים באלקטרונים: הקשר הכפול בין הפחמן לחמצן האמידי, וזוג האלקטרונים הלא קושר של החנקן האמידי. כאשר יש סמיכות בין מרכזים עשירים באלקטרונים מתקיים בהם רזוננס – האלקטרונים “קופצים” בין האטומים היוצרים את אותו מרכז עשיר אלקטרונים. בפועל, מתקבל מצב היברידי בו האלקטרונים מתחלקים בין אותם אטומים, והקשר הפפטידי שנראה כקשר בודד הוא למעשה קשר קוולנטי וחצי (1.5). מכיוון שהקשר הפפטידי הוא יותר מקשר קוולנטי בודד, הוא מקבל תכונות של קשר כפול והינו קשיח. מסיבה זו, אטומי הקשר אינם יכולים להסתובב בקשר הפפטידי.
שלילת מסיחים:
ב. מיונן פירושו במצב יוני (בעל מטען). בעת היווצרות הקשר הפפטידי ב-pH ניטרלי (פיזיולוגי) הקבוצה האמינית של חומצה אמינית אחת מוסרת שני פרוטונים (ובכך מאבדת את המטען החיובי שלה) והחמצן הקרבוקסילי המיונן יוצא (ובכך מאבד את המטען השלילי) ומתקבל קשר שאינו טעון חשמלית. סה”כ ביצירת הקשר הפפטידי מתקבלת מולקולת מים (H2O). ניתן לעצור פה, אך נעמיק את ההסבר: בקשר הפפטידי ישנו רזוננס שאחת הצורות שלו היא מטען חיובי על גבי החנקן, ומטען שלילי על גבי החמצן. בפועל רזוננס זה אינו מעבר בין צורות, אלא מדובר היבריד של כל הצורות האפשריות, ולכן לא מדובר במטען מוחלט אלא בδ- על גבי החמצן וδ+ פלוס על גבי החנקן. מכיוון שלא מדובר במטענים מוחלטים זהו לא מצב מיונן.
ג. תיוליזה זהו פירוק של קשר המכיל גופרית. הקשר הפפטידי הינו קשר הנוצר בין הפחמן הקרבוקסילי לבין החנקן האמיני. מכיוון שאין גופרית בקשר הפפטידי, פירוק הקשר אינו נקרא תיאוליזה. פירוק קשר פפטידי נקרא פרוטאוליזה.
ד. הקונפיגורציה של קשרים פפטידים היא לרוב טראנס (trans). בקונפיגורצית טראנס המתמירים העיקריים של הקשר הפפטידי נמצאים בכיוונים מנוגדים אחד לשני. בצורה זו, הדחייה החשמלית בין המתמירים היא מינימלית ולכן זוהי הצורה המועדפת מבחינה תרמודינאמית. בקונפיגורציה ציס (cis) המתמירים של הקשר הפפטידי פונים לאותו כיוון וקרובים אחד לשני, ולכן במצב זה הדחייה החשמלית מקסימלית (אפקט סטרי).
להרחבה – Lehninger, מהדורה שישית, עמוד 117-118(The Peptide Bond).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: המבנה של חלבונים.
להרחבה – Lehninger, מהדורה שמינית, פרק 4, עמוד 486-487 (The Peptide Bond).
ביוכימיה 2 שאלה 23
איזה סוג של אינטראקציה חלשה משחק תפקיד חשוב בהחזקת גדילי ביטא (beta strands) יחד במבנה של משטחי ביטא (beta sheets)?
במה השאלה עוסקת: מבנה שניוני של חלבונים
תשובה ג. משטח בטא זהו סוג של מבנה שניוני. מבנים שניוניים מיוצבים בעיקר ע”י קשרי מימן. קשרי המימן במשטח בטא (וגם בסליל אלפא) נוצרים בין קבוצה קרבוקסילית של ח”א אחת לבין קבוצה אמינית של ח”א אחרת.
שלילת מסיחים:
א. אינטרקציות יוניות מתייחסות להפרדת מטענים מוחלטת ומשיכה בין חומר טעון חיובית לבין חומר טעון שלילית. משטח בטא אינו מיוצב ע”י אינטרקציות אלו.
ב. קשר קוולנטי זהו הקשר המייצב את המבנה הראשוני של חלבון. ברצף הראשוני מתייחסים לסדר החומצות האמיניות בחלבון כפי שהן מופיעות אחת אחרי השנייה. חומצות אמיניות מתחברות אחת לשנייה בריאקצית דחיסה (קונדנסציה) היוצרת את הקשר הפפטידי (שזהו קשר קוולנטי).
ד. אינטרקציות ואן דר ואלס אילו האינטרקציות הבין מולקולריות החלשות ביותר. אינטרקציות אלו אינן האינטרקציות המאפשרות יצירה של משטח בטא.
להרחבה – Lehninger, מהדורה שישית, עמוד 123(The Beta Conformations).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: המבנה של חלבונים.
להרחבה – Lehninger, מהדורה שמינית, פרק 4, עמודים 502-504 (The Beta Conformations).
ביוכימיה 2 שאלה 24
ישנן חומצות אמינו המפריעות (ואף מונעות) ליצירת מבנה שניוני של אלפא-הליקס (alpha helix) בחלבונים, בעוד אחרות דווקא מייצבות מבנה זה.
על פי גודל ומטען שייר הצד, את מי מבין חומצות האמינו הבאות תצפה/י למצוא במבני אלפא-הליקס יציבים?
במה השאלה עוסקת: מבנים שניוניים
תשובה ד. אלאנין הינה חומצה אמינית אליפטית בעלת שייר קטן ולא מתיינן (CH3) אשר נוטה ליצור סלילי אלפא בקלות. מכיוון שהשייר קטן והידרופובי, אין דחייה חשמלית עם שיירים סמוכים, מה שמאפשר ליצור סליל אלפא יותר יציב.
שלילת מסיחים:
א. גליצין הינה חומצה אמינית קטנה ולא כיראלית. עובדה זו מאפשרת לגליצין הרבה קונפורמציות ובכך גליצין שוברת את סליל אלפא – ומכאן שגליצין לא תמצא בסליל אלפא.
ב. פרולין איננה משתתפת ביצירת סליל אלפא משני סיבות: א. הטבעת של פרולין קשיחה ולכן הקשר בין פחמן אלפא לחנקן לא יכול להסתובב. ב. פרולין אינה יכולה ליצור קשרי מימן לאחר יצירת הקשר הפפטידי. כזכור, סליל אלפא מיוצב ע”י קשרי מימן בין הקבוצה הקרבוקסילית לבין הקבוצה האמינית. פרולין, בניגוד לשאר החומצות האמיניות, היא חומצה אמינית טבעתית (השייר קשור לקבוצה האמינית) ולכן מכילה פחות פרוטון אחד. עובדה זו אומרת שלאחר יצירת הקשר הפפטידי החנקן בפרולין לא נושא פרוטונים, ומכאן שאינה יכולה ליצור קשרי מימן.
ג. ליזין זו חומצה אמינית טעונה חיובית ב-pH פיזיולוגי. רצף של מספר ליזין סמוכים משמעו רצף של מטענים חיוביים סמוכים – מכאן שיווצר בסליל דחייה חשמלית. הדחייה החשמלית תוביל לירידה ביציבות סליל אלפא, ומכאן שרצף של מטענים זהים לא מייצב סליל אלפא.
להרחבה – Lehninger, מהדורה שישית, עמוד 121-122 (Amino Acid Sequence Affects Stability of the alpha Helix).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: המבנה של חלבונים.
להרחבה – Lehninger, מהדורה שמינית, פרק 4, עמוד 498-502 (Amino Acid Sequence Affects Stability of the alpha Helix).
ביוכימיה 2 שאלה 25
קיפול חלבונים הינו תהליך מורכב ועשוי להיות מעוכב בעקבות תהליכי אגרגציה. מי מבין ההיגדים הבאים אודות קיפול חלבונים הינו שגוי?
במה השאלה עוסקת: מבנה חלבונים.
תשובה ג’ : אף על פי שמרבית החלבונים דורשים את עזרתם של שאפרונים (חלבונים אשר מסייעים בתהליך הקיפול של חלבונים) על מנת להתקפל כראוי, ישנם חלבונים המתקפלים באופן ספונטני לאחר שהם עוברים סינתזה בתא כך שקיפולם לא תלוי בנוכחות שאפרונים או השקעת אנרגיה. חשוב להבין כי אחד הגורמים המרכזיים שמניע קיפול חלבונים הוא אגרגציה של אזורים הידרופוביים כדי שלא יהיו חשופים לסביבה המימית. ניתן להניח אם כך, שחלבונים בעלי רצף ארוך או מורכב יזדקקו ליותר עזרה מאשר חלבונים קטנים בעלי מבנה פשוט.
שלילת מסיחים :
א. נוסחא שמאוד חשוב להכיר: ΔG = ΔH – TΔS, מתארת את האנרגיה החופשית של גיבס כתלות באנתרופיה (ΔS) ובאנתלפיה (ΔH). בתהליך קיפול חלבונים האנתרופיה עולה כתוצאה מירידה במספר מולקולות המים העוטפות את האזורים ההידרופובים בחלבון. ככל שהשינוי (ערך סופי פחות ערך התחלתי) באנתרופיה קטן יותר, השינוי באנרגיה החופשית גדול יותר במובן של חיובי יותר, והפוך.
פירוט – האנתלפיה היא תכולת החום הקיימת במערכת והיא משקפת את מספר וסוגי הקשרים הכימיים במגיבים ובתוצרים. ריאקציה אקסותרמית פולטת חום (תכולת החום של התוצרים נמוכה משל המגיבים) ותהיה בעלת ΔH שלילי. באופן דומה, ריאקציה אנדותרמית לוקחת חום מהסביבה ותהיה בעלת ΔH חיובי. אנתרופיה לעומת זאת, היא מדד לאי הסדר הקיים במערכת. כאשר תוצרי הריאקציה פחות מסודרים מהמגיבים האנתרופיה עולה והתגובה ספונטנית. למשל, אינטראקציות הידרופוביות מושפעות מכוח האנתרופיה – שחרור אנרגיה כתוצאה מעלייה באי הסדר במערכת.
ב. ישנם חלבונים בהם איזומריזציה היא חלק מתהליך הקיפול התקין. האנזים Protein Disulfide Isomerase או בקיצור PDI, משנה את מיקום הקשרים הדי סולפידיים הקיימים בתוך החלבון עד אשר נוצרים הקשרים הנכונים של הקונפורמציה הנטיבית (קיפול החלבון נקבע לפי רצף חומצות האמינו – מבנה ראשוני). שינוי מיקום הקשרים מתבצע על ידי כך שהאנזים מחזר את הקשר הקיים ובכך שובר אותו ולאחר מכן בונה אותו במקום חדש בתהליך בו יש חמצון של שני ציסטאינים ושחרור 2 פרוטונים. שינוי מיקום הקשרים נקרא איזומריזציה.
איזומריזציה הינו תהליך פנים מולקולארי בו נוצרים איזומרים ע”י כך שאנזימים מסוג איזומראזות מעבירים קבוצה ממקום למקום בתוך אותו החומר. לא להתבלבל עם טראנספראזות שמעבירים קבוצות בין חומרים שונים.
הערת מחבר – בנוסף לאנזים ה- PDI ישנו אנזים נוסף בעל תפקיד דומה שרצוי להכיר – (Peptide Prolyl Isomerase (PPI אשר מעביר פרולין ממצב ציס למצב טראנס במקטעי החלבון שאינם מקופלים נכון. גם PDI וגם PPI מאוד חשובים לתהליך הקיפול (וגם שאפרונים נוספים), בלעדיהם קיפול החלבון היה איטי יותר ומורכב.
ד. המבנה הראשוני של החלבון, אשר מורכב מרצף חומצות האמינו שמרכיבות אותו, קובע את המבנה הנטיבי של החלבון. לאחר שהחלבון תורגם הוא מתחיל להתקפל ויוצר את המבנה השניוני, קשרי מימן נוצרים בין מקטעים שונים בחלבון ויוצרים מבנים כמו סלילי אלפא (Alpha helix) ומשטחי בטא (beta-sheet).
הערת מחבר – הכוח המניע את קיפול החלבון הוא כוח האנתרופיה – חלקים הידרופוביים בחלבון רוצים להתרחק מסביבה מימית ולכן הם מתקפלים ויש צמצום של השטח החשוף למים. לכן, מספר מולקולות המים מסביב קטן, האנתרופיה עולה והתהליך מועדף מבחינה תרמודינאמית.
להרחבה – Lehninger , מהדורה שישית, עמודים 150-155.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: המבנה של חלבונים.
להרחבה – Lehninger , מהדורה שמינית, פרק 4, עמודים 553, 569-570 (PDI), עמ 481-482 (Packing hydrophobic amino acid away from water).
ביוכימיה 2 שאלה 26
יצירה של קשר פפטידי בין שתי חומצות אמינו הינה דוגמא לריאקציית ___________ :
במה השאלה עוסקת: קשר פפטידי
תשובה ב. ביצירה של קשר פפטידי יש חיבור בין שתי מולקולות (שתי חומצות אמיניות) תוך כדי הוצאה של מולקולת מים. ריאקציה כזו נקראת ריאקציה דחיסה (קונדנסציה).
שלילת מסיחים:
א. פרוטאוליזה זהו התהליך בו מפרקים חלבונים ע”י חיתוך קשרים פפטידים. זהו אינו תהליך של יצירת קשר פפטידי ולכן מסיח זה נפסל.
ג. בריאקציה מסוג העברת קבוצה האנזים לוקח קבוצה כלשהי ממולקולה אחת ומעביר אותה למולקולה אחרת. ביצירת הקשר הפפטידי יש חיבור בין שתי חומצות אמיניות (ולא לקיחת קבוצה מחומצה אמינית אחת והעברתה לשנייה) ולכן מסיח זה נפסל.
ד. בריאקציות חמצון-חיזור ביולוגית יש העברה של אלקטרונים ממולקולה אחת לנשא אלקטרונים. בקשר הפפטידי אין שימוש בנשאי אלקטרונים ולכן לא מדובר בריאקציה מסוג חמצון חיזור.
להרחבה – Lehninger, מהדורה שישית, עמוד 86 (Figure 3-13).
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: המבנה של חלבונים.
להרחבה – Lehninger, מהדורה שמינית, פרק 3, עמוד 380 (Figure 3-13).
ביוכימיה 2 שאלה 27
נמצא רצף חומצות האמינו הבא בחלבון מסוים: Ser-Pro-Ala-Thr. רצף זה מהווה, ככל הנראה, חלק מ:
במה השאלה עוסקת: מבנים שניוניים
תשובה ד. פניית בטא (beta turn) מורכבת מארבע חומצות אמיניות, כאשר בעמדה 2 יש לרוב פרולין או בעמדה 3 יש גליצין. פרולין מקבלת בקלות קונפיגורציה ציס (cis) ולכן היא מאפשרת את ביצוע הפנייה בפפטיד. בפפטיד בשאלה ניתן לראות רצף של 4 חומצות אמיניות כאשר החומצה האמינית השנייה היא פרולין – מה שמרמז לפניית בטא.
שלילת מסיחים:
א. במשטח בטא אנטי מקביל נוצרים קשרי מימן בין שני גדילים בכיוונים מנוגדים, בשאלה נתון רצף של 4 ח”א ולא ניתן להסיק ממנו לגבי משטחי בטא.
ב. במשטח בטא מקביל נוצרים קשרי מימן בין שני גדילים באותו כיוון, בשאלה נתון רצף של 4 ח”א ולא ניתן להסיק ממנו לגבי משטחי בטא.
ג. ברצף הנתון יש פרולין. פרולין אינה יכולה לבנות סליל אלפא מכיוון שאינה יכולה ליצור קשרי מימן לאחר יצירת הקשר הפפטידי.
להרחבה – Lehninger, מהדורה שישית, עמוד 124 (Figure 4-7)
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: המבנה של חלבונים.
להרחבה – Lehninger, מהדורה שמינית, פרק 4, עמודים 504-506 (Beta turns are common in proteins).
ביוכימיה 2 שאלה 28
במבנה של סליל אלפא (α-helix), שיירי הצד של חומצות האמינו:
במה השאלה עוסקת: מבנים שניוניים
תשובה ב. החלק הפנימי של סליל אלפא מלא באטומי השלד הפוליפפטידי (Main Chain). מסיבה זו, כל השיירים של החומצות האמיניות בסליל אלפא פונים כלפי חוץ.
שלילת מסיחים:
א. בתוך סליל אלפא אין מקום לשיירים של חומצות אמיניות ולכן כלל השיירים פונים כלפי חוץ הסליל.
ג. סליל אלפא מיוצב ע”י קשרי מימן הנוצרים בין הקבוצה הקרבוקסילית לבין הקבוצה האמינית של חומצות אמיניות בשרשרת הראשית. השיירים של החומצות האמיניות אינם משתתפים ביצירת קשרי המימן אשר מייצבים את הסליל.
ד. בתוך סליל אלפא אין מקום לשיירים של חומצות אמיניות ולכן כלל השיירים פונים כלי חוץ הסליל.
להרחבה – Lehninger, מהדורה שישית, עמוד 120 (Figure 4-4)
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: המבנה של חלבונים.
להרחבה – Lehninger, מהדורה שמינית, פרק 4, עמוד 494 (Figure 4-3).
ביוכימיה 2 שאלה 29
מה נכון לגבי סליל אלפא הליקס?
במה השאלה עוסקת: מבנים שניוניים
תשובה ג’. החלק הפנימי של סליל אלפא מלא באטומים היוצרים את השלד הפוליפטידי (Main Chain) ולכן בתוך הסליל אין מקום לשיירים של החומצות האמיניות. כל השיירים של החומצות האמיניות בסליל אלפא פונים כלפי חוץ הסליל.
שלילת מסיחים:
א. סליל שמאלי הינו פחות יציב מאשר סליל ימני, אך סליל שמאלי אינו קיים בחלבונים טבעיים. הסליל הקיים בחלבונים הוא סליל ימני.
ב. שיירים בעלי אותו מטען (למשל חיובי) הנמצאים בסמיכות אחד לשני מורידים מיציבות סליל אלפא מכיוון שמובילים לדחייה חשמלית ולהתרחקות חומצות האמיניות בסליל.
ד. קבוצות צדדיות נפחיות מובילה לדחייה סטרית (מרחבית) של חומצות אמיניות בסליל, מה שיוביל להתרחקות חומצות אמיניות אחת מהשנייה בסליל אלפא ולכן יציבות הסליל תרד.
להרחבה – Lehninger, מהדורה שישית, עמוד 121-122 (Amino Acid Sequence Affects Stability of the Alpha Helix)
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: המבנה של חלבונים.
להרחבה – Lehninger, מהדורה שמינית, פרק 4, עמוד 498-502 (Amino Acid Sequence Affects Stability of the alpha Helix).
ביוכימיה 2 שאלה 30
אנזים מסוים מזרז ריאקציות במנגנון של קטליזת חומצה-בסיס (acid-base catalysis). ידוע, שלשם פעילות האנזים, דרוש שייר גלוטמאט שהוא עם פרוטון (protonated) באתר הפעיל. על סמך מידע זה, איזה מהבאים סביר להיות ה-pH האופטימלי של אנזים זה? נתון כי ה-PKr של גלוטמאט הוא 4.25.
במה השאלת עוסקת: אנזימים, pH אופטימלי.
תשובה ג’. נאמר לנו שלשם פעילות אופטימאלית של האנזים נדרש שייר גלוטמאט שלא עבר דה-פרוטונציה באתר הפעיל. כמו-כן נאמר לנו שה – PKr של גלוטמאט הוא 4.25. כאשר ה-Ph יהיה שווה ל-PKr נקבל 50% גלוטמאט עם שייר COOH שלא איבד פרוטון ו-50% גלוטמאט עם שייר COO- שאיבד פרוטון. כאשר ה-Ph יהיה שווה ל-3.25 היחס יהיה 90% עם פרוטון 10% בלי פרוטון וכאשר ה-pH יהיה 2 כמו בתשובה ג’, כמעט 100% מהגלוטמאט יהיו עם פרוטון כפי שנדרש.
להרחבה: Lehninger 6th edition, ע”מ 212-213
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger, מהדורה שמינית, פרק 6, עמודים 798-799 ׁ(Enzyme activity depends on PH).
ביוכימיה 2 שאלה 31
מי מהבאים מתאר נכונה את הקשר הפפטידי?
תשובה: ב’ (לרוב הקשר נוצר בעמדת טראנס). הקשר הפפטידי נוצר בין הפחמן של הקבוצה הקרבוקסילית של חומצה אמינית אחת לבין חנקן הקבוצה האמינית של חומצה אמינית שנייה. כיוון שלקשר יש מאפיינים של קשר כפול, ניתן לקבל קונפיגורציה צ’יס (cis) או טראנס (trans). לרוב, הקונפיגורציה המתקבלת ביצירת הקשר הפפטידי היא טראנס. העדפה תרמודינאמית לעמדת טראנס כיוון שהקבוצות הקשורות לקשר הפפטידי נמצאות בכיוונים מנוגדים ובמצב זה הדחייה החשמלית מינימלית.
שלילת מסיחים:
א. הקשר הפפטידי מיוצב ע”י רזוננס, מה שנותן לו מאפיינים של קשר כפול ולכן אטומי הקשר אינם יכולים להסתובב.
ג. אטומי הקשר, יחד עם האטומים הקשורים אליהם ישירות, נמצאים באותו מישור שטוח.
ד. השיירים של הח”א אינן במישור המישורי של הקשר הפפטידי.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: המבנה של חלבונים.
להרחבה: Lehninger, מהדורה שמינית, פרק 3, עמודים 380-379.
ביוכימיה 2 שאלה 32
מה מהבאים איננו נכון בנוגע לאנזימים ?
תשובה : א’
הסבר: לנינגר ( עמ’ מהדורה 6 26-27). רובנו מכירים שהאנזימים בנויים חלבונים. הרוב המוחלט של האנזימים- הינם חלבונים. עם זאת, קיימים גם זרזים שהם אינם חלבונים, כגון מולקולות RNA בשם ריבוזימים, בהם תתקלו במולקולרית ג’. אלו מולקולות רנ”א שיכולות לזרז ריאקציות שונות ( שכפול\דרגרדציה\מודיפקציות שונות ).
שלילת מסיחים :
ב- נכון, אנזימים מפחיתים את אנרגיית השפעול- היא בעצם ההפרש בין מגיב במצבו ההתחלתי ובמצב המעבר. מגיב לא הופך מיד לתוצר, אלא הוא עובר דרך “תוצר ביניים”, שגם לו יש אנרגיה מסויימת. לרוב מה שמגביל ריאקציה מלהתרחש במהירות הוא הגעה למצב המעבר, שהינו יציב מאוד. אנזימים מפחיתים את האנרגיה הנדרשת כדי להתגבר על המחסום האנרגטי, ובכך לזרז את ההגעה אליו. ( יוצרים התאמה מרחבית טובה יותר בין האנזים למגיב במצב המעבר. הקישוריות של האנזים למצב המעבר היא אקסורגנית- משחררת אנרגיה, ואותה אנרגיה מקטינה את אנרגיית השפעול של הריאקציה ומחישה את קצב התרחשותה.
ג- ∆G° מראה מה יהיה שיווי המשקל הסופי של הריאקציה, אךהוא לא מגלה תוך כמה זמן הריאקציה תגיע לשיווי משקל – נכון, אנחנו מדברים בעצם על תרמודינמיקה שבה שואלים האם הריאקציה תתרחש ואם כן מה יהיה שיווי המשקל, אך לא מדברים במונחים קינטיים.
ד- במערכות ביולוגיות ריכוז הסובסטרט קרוב לערך ה-Km. קופקטורים לריאקציות ביולוגיות כמו למשל ATP, NADPH, NAD לרוב ריכוזם יהיה גבוה מערך ה-Km ובצורה זו הם לא מהווים גורם מגביל לתגובה. להרחבה ניתן לקרוא בעמוד 591 בספר מהדורה 6.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger, מהדורה שמינית, פרק 6, עמוד 730 (Most enzymes are proteins),
736-729.
ביוכימיה 2 שאלה 33
חומצות אמינו מוגדרות אמפוליטיות (ampholytes) היות והן יכולות לתפקד:
במה השאלה עוסקת: חומצות אמינו
תשובה א. המונח אמפוליטי מתייחס ליכולת של חומר לתפקד הן כחומצה והן כבסיס וחומצות אמינו מתנהגות באופן זה. ב- pH סטנדרטי, הקצה האמיני של החומצה טעון חיובי והוא עדיין לא שחרר פרוטון, ואילו הקצה הקרבוקסילי טעון שלילית כיון שהוא כבר שחרר את הפרטון שלו. כלומר, בערך pH מסוים המולקולה משמשת הן כחומצה והן כבסיס והדבר נובע מהבדלים בין הקבוצות הפונקציונאליות השונות המרכיבות את חומצת האמינו.
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו.
להרחבה – Lehninger, מהדורה שמינית, פרק 3, עמוד 372 (אמפוליט), 367-369 (תכונות של חומצות אמיניות).
ביוכימיה 2 שאלה 34
טיטרציה של חומצת האמינו ואלין באמצעות בסיס חזק, כדוגמת NaOH , חושפת שני pK’s . מהי ריאקציית הטיטרציה המתרחשת ב- pK2=9.62) ?pK2).
במה השאלה עוסקת: טיטרציות של ח.אמינו.
תשובה ג. ואלין משתייכת למשפחת חומצות האמינו הלא פולאריות, המשמעות היא ששייר ה-R שלה אינו יכול ליצור קשרי מימן ולכן אינו יכול להתיינן (למסור או לאבד את הפרוטון). משום כך אצל ואלין מדברים רק על שני ערכי pK. ככלל, בכל טיטרציה של חומצת אמינו הקבוצה הראשונה שתעבור יינון היא קבוצת הקרבוקסיל, וזאת מאחר ויש לה את ה- pK הנמוך ביותר. רק ב- pK הבא שייר ה- R או קבוצת האמין יעברו יינון. כלל נוסף הוא שכל חומצה אמינית מתחילה לעבור טיטרציה כאשר קבוצת הקרבוקסיל וקבוצת האמין עוד לא איבדו את הפרוטון (COOH ו- +NH3 בהתאמה) וזאת משום שמתחילים ב- pH של 0 ויש עודף פרוטונים בסביבה.
הרחבה – טיטרציה נועדה בשביל לקבוע את הריכוז של חומצה מסוימת בתמיסה מסוימת. לוקחים את התמיסה ומוסיפים ריכוזים עולים של בסיס חזק (לרוב NaOH) עד שהחומצה הופכת לניטראלית. בעזרת כמות הבסיס החזק שהוסף ניתן לחשב את ריכוז החומצה בתמיסה המקורית. עקומת טיטרציה מתארת זאת בגרף pH כפונקציה של ריכוז הבסיס שהוסף. חומצות אמינו יכולות לשמש הן כבסיס (תקבל פרוטון) והן כחומצה (תמסור פרוטון) כתלות ב- pH בו הן נמצאות. לכל חומצה אמינית יש לפחות 2 מצבי שיווי משקל/ 2 ערכי pK (של קבוצת האמין ושל קבוצת הקרבוקסיל). בחומצות אמינו להן שייר R שיכול להתיינן יש קבוע שיווי משקל שלישי. כאשר נמצאים ב- pH אשר שווה לערך ה- pK של אחת הקבוצות הדבר מעיד לנו על כך שישנו שיווי משקל בין מצב מיונן למצב לא מיונן. למשל, כאשר ה- pH שווה ל- pK של קבוצת הקרבוקסיל 50% מקבוצות הקרבוקסיל של אותה חומצת אמינו בתמיסה כבר מסרו את הפרוטון (-COO) ו- 50% עוד לא מסרו אותו (COOH).
הערת מחבר – Lehninger, מהדורה שישית, עמוד 78, מומלץ להציץ בטבלה שבה ערכי ה- pK של 20 חומצות האמינו. אין צורך לשנן את המספרים אך כן הכרחי לדעת לאלו מחומצות האמינו ישנו שייר R שיכול להתיינן.
שלילת מסיחים :
א. מסיח זה היה נכון אילו היו שואלים אותנו על ריאקציית הטיטרציה שהייתה מתרחשת ב- pK הראשון. במצב זה, קבוצת הקרבוקסיל הייתה מתחילה לאבד את הפרוטון שלה עד מצב ש- 50% כבר מסרו אותו.
ב. ריאקציית הטיטרציה מוגדרת על ידי הוספה הדרגתית של בסיס חזק שמסוגל לסתור את החומצה, כלומר לקחת ממנה פרוטון. NH2 אינו נחשב כלל כבסיס חזק. קבוצת ההידרוקסיל היא זו שמקבלת את הפרוטון והופכת למולקולת מים בתמיסה.
ד. קבוצת האמינו נמצאת בצורת +NH3 עד אשר מגיעים לערך ה- pK שלה ובו 50% מקבוצות האמינו שמשתייכות למולקולות שבתמיסה כבר איבדו את הפרוטון לצורת NH2.
הערת מחבר – דרך נוספת לשלול את הסעיף היא להגיד לעצמנו שכאשר ה- pH שווה ל- 7 (פיזיולוגי) ואלין היא ניטראלית והמצב מכונה צויטריון (קבוצת האמינו טעונה חיובית וקבוצת הקרבוקסיל טעונה שלילית וסך המטען 0), רק כאשר עולים בערך ה- pH של התמיסה קבוצת האמינו הופכת לניטראלית ומאבדת את הפרוטון שלה.
להרחבה – Lehninger , מהדורה שישית, עמודים 64-67 (הקדמה והסבר על טיטרציה באופן כללי), עמודים 82-85 (טיטרציה של חומצות אמינו)
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו, מים ו-PH.
להרחבה – Lehninger , מהדורה שמינית, פרק 2- עמודים 305-309 (הקדמה והסבר על טיטרציה באופן כללי), פרק 3- עמודים 372-375 (טיטרציה של חומצות אמינו).
ביוכימיה 2 שאלה 35
לאיזו חומצה אמינית שייכת עקומת הטיטרציה הבאה?
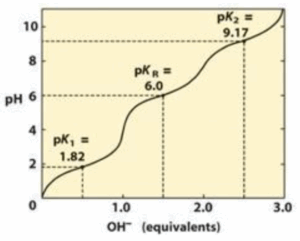
במה השאלה עוסקת: טיטרציה של חומצות אמינו
תשובה ד. חומצות אמינו הן אמפוליטיות (Ampholytes): יכולות לתפקד הן כחומצה והן כבסיס הודות ל- 2 קבוצות שיכולות למסור או לקבל פרוטון בסביבה מימית – קבוצת האמינו וקבוצת הקרבוקסיל. עבור כל חומצה אמינית יש לפחות 2 מצבי יינון (2 ערכי pKa): של הקבוצה הקרבוקסילית ושל הקבוצה האמינית ועבור חומצות אמינו שלהן שייר R שיכול לעבור יינון ישנם שלושה מצבים. מומלץ לזכור שה- pKa של הקבוצה האמינית הוא באזור 9 ושל הקבוצה הקרבוקסילית הוא באזור 2. כאשר ה- pH שווה ל- PKa של יש שו”מ בין מצב מיונן למצב לא מיונן, כלומר 50% מסה”כ הקבוצות בתמיסה איבדו את הפרוטון ו- 50% עוד לא איבדו אותו. סביב כל ערך pK ישנו טווח בופר של יחידה אחת פלוס/ מינוס סביב ערך זה. בעקומת הטיטרציה הנתונה בשאלה רואים כי ישנם שלושה ערכי pK (ובהתאמה, שלושה טווחי בופר) ומכאן שמדובר בחומצת אמינו לה יש שייר R טעון שיכול לעבור יינון (פסילת מסיח ג’). עוד רואים כי ה- pK של שייר ה- R הוא 6 ומכאן שמדובר בחומצת האמינו היסטדין (סעיף ד’). טווח הבופר של שייר ה- R של היסטדין הוא ב- pH הפיזיולוגי ומכאן שהיסטדין מתאימה לשמש בופר בתא.
הערת מחבר – מומלץ לזכור את ה- pK של שיירי ה- R של חומצות האמינו שיכול לעבור יינון (טבלה 3-1 בעמ’ 77 מהדורה 6/ עמ’ 365 מהדורה 8). יש סה”כ 7 כאלו: ח”א חיוביות, ח”א שליליות, טירוזין וציסטאין.
להרחבה – Lehninger,מהדורהשישית, עמודים 81-85.
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו.
להרחבה – Lehninger, מהדורה שמינית, פרק 3, עמודים 372-377.
ביוכימיה 2 שאלה 36
לצורך זיהוי חומצה אמינית בוצעה טיטרציה והתקבלה העקומה המצורפת. איזו חומצה אמינית עשויה להתאים לתוצאות?
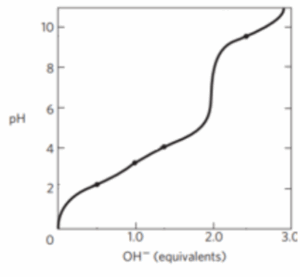
תשובה: ד’ (גלוטמאט). בעקומה המצורפת ניתן להבחין בשלושה אזורים המתנגדים לשינוי ב-pH מה שכבר מרמז על חומצה אמינית טעונה. ניתן לראות כי שניים מאזורי הבופר נמצאים בטווח החומצי, ואזור בופר אחד נמצא בטווח הבסיסי. עבור כל חומצה אמינית יש לפחות שני אזורי בופר: קצה קרבוקסילי (בטווח החומצי), וקצה אמיני (בטווח הבסיסי). אזור הבופר השלישי מתייחס לשייר (pKr) ומרמז לנו על הקבוצה לה משתייכת החומצה האמינית. במקרה זה, אזור הבופר השלישי נמצא בטווח החומצי ולכן העקומה שייכת לאחת מהחומצות האמיניות הטעונות שלילית – גלוטמאט או אספרטט. בשאלה זו, העקומה שייכת לגלוטמאט.
שלילת מסיחים:
א. איזולאוצין זוהי חומצה אמינית לא פולארית. חומצות אמיניות המשתייכות למשפחה זו חסרות מטען. לכן, בטיטרציה יתקבלו שני אזורי בופר. בעקומה הנ”ל ניתן להבחין בשלושה אזורי בופר.
ב. אספרגין זוהי חומצה אמינית פולארית. חומצות אמיניות פולאריות המשתייכות למשפחה זו חסרות מטען (למעט ציסטאין המתייננת ב-pH=8.2). לכן, בטיטרציה של אספרגין יתקבלו שני אזורי בופר. בעקומה הנ”ל ניתן להבחין בשלושה אזורי בופר.
ג. ליזין זוהי חומצה אמינית בסיסית (טעונה חיובית) ולכן תתן עקומה עם 3 אזורי בופר. עם זאת, השייר של ליזין מוסר פרוטון רק בpH בסיסי ולכן נצפה ששני אזורי בופר יהיו באזור הבסיסי (הקצה האמיני והשייר), ואזור בופר אחד בטווח החומצי (קצה קרבוקסילי). מסיח זה נפסל.
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו.
להרחבה:לנינג’ר מהדורה שמינית, פרק 3, עמוד 377 (Figure 3-12).
ביוכימיה 2 שאלה 37
בעקומת טיטרציה נצפתה התנגדות לשינוי ב-pH באזור pH=6. מי החומצה האמינית לה נעשתה טיטרציה?
תשובה: ד’ (אף מסיח אינו נכון). התנגדות ל-pH מתרחשת באזורי בופר, בו ערך ה-pH הוא פלוס/מינוס 1 מערך ה-pKa של אותה קבוצה פונקציונלית. עבור כל חומצה אמינית יש לפחות שני אזורי בופר – אזור בטווח החומצי של הקבוצה הקרבוקסילית, ואזור בטווח הבסיסי של הקבוצה האמינית. חלק מהחומצות האמיניות מכילות שייר שיכול למסור פרוטון, ולהם ערך pKr שיכול גם הוא להתנגד לשינויים ב-pH. ה-pKr של היסטידין הוא 6, ולכן באזור זה היסטידין תתנגד לשינויים ב-pH. מכאן, מסיחים א-ג שגויים.
שלילת מסיחים:
א.W זו האות המייצגת את טריפטופן. לטריפטופן אין pKr.
ב. Q זו האות המייצגת את גלוטמין. לגלוטמין אין pKr.
ג. Y זו האות המייצגת את טירוזין. לטירוזין pKr בעל ערך של 10~
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו, מים ו-PH.
להרחבה: לנינג’ר מהדורה שמינית, פרק 3, עמוד 377 (Figure 3-12), מהדורה שישית עמוד 111 (Table 3-1)- לחילופין מהדורה 8 עמ 365 אך הטבלה חתוכה, פרק 2- 313 (הסבר על בופר).
ביוכימיה 2 שאלה 38
נבדק מבנה של חלבון אשר הודגר בתמיסה של CCl4. מהצפוי להתקבל באנליזה?
תשובה:ב’ (חומצות אמיניות ליפופיביות יפנו לאזור הפנימי של החלבון). כאשרמים הם הממס, השיירים הפולארים/טעוניםשל ח”א לרוב יפנו לצד החיצוני של החלבון (שזהו הצד שבא במגע עם המים – פולארימתמוסס בפולארי) ושיירים הידרופוביםיפנו לחלק הפנימי של החלבון (הידרופובי מתמוסס בהידרופובי). כאשר משתמשים בממסאורגני שהוא ממש אפולרי(כמו CCl4)מקבלים סביבה הידרופובית. הסביבה ההידרופובית תוביל לדנטורציהשל החלבון ולהתקפלות שלו מחדש כך ששיירים הידרופוביםיפנו לצד החיצוני (יבואו במגע עם הממס ההידרופובי), והשיירים ההידרופיליםיהיו בסביבה הפנימית של החלבון. חומצות אמיניות ליפופוביותהינן חומצות אמיניות הידרופיליות ולכן כאשר משתמשים בממס אורגני הן יפנו לצדהפנימי של החלבון.
שלילת מסיחים:
א.CCl4לא יכול ליצור קשרי מימן ולכן השיירים בחלבון לא יצרו קשרי מימן עם הממס.
ג.בדנטורציהנאבד המבנה השלישוני וחלק מהמבנים השניוניים. חלק מהמבנים השניוניים יכולים להשמרבדנטורציהולכן מסיח זה נפסל.
ד.כאשר הסביבה היא הידרופילית הח”אההידרופיליות יפנו לאזור החיצוני של החלבון, אך כאשר הסביבה היא הידרופובית הח”אההידרופיליות יפנו לאזור הפנימי של החלבון
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו.
להרחבה: לנינג’ר מהדורה שמינית, פרק 3, עמודים 415-421 (The structure of proteins).
ביוכימיה 2 שאלה 39
איזה פפטיד יבלע אור בצורה המרבית ביותר באורך גל של 280nm?
תשובה: ג’ (RNWDWK). בליעת אורך גל של 280nm נעשית ע”י חומצות אמיניות ארומטיות בפפטיד – טריפטופן (W), טירוזין (Y), פנילאלנין (F). טריפטופן בולעת קרינה בעוצמה גבוהה, לאחר מכן טירוזין ופנילאלנין בולעת קרינה בצורה מאוד חלשה.
שלילת מסיחים:
א. הפפטיד מכיל פנילאלנין ולכן יבלע אור באורך גל של 280nm. פנילאלנין בקושי בולע קרינה לעומת טריפטופן וטירוזין, ולכן מסיח זה נפסל.
ב. הפפטיד אינו מכיל חומצות אמיניות ארומטיות ועל כן לא יבלע אורך גל של 280nm.
ד. הפפטיד מכיל טירוזין ולכן יבלע אורך באורגל גל של 280nm. טירוזין בולע קרינה פחות טוב מטריפטופן ולכן מסיח זה נפסל.
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו.
להרחבה: לנינג’ר מהדורה שמינית, פרק 3, עמודים 267-268.
ביוכימיה 2 שאלה 40
מה ניתן להזניח בקינטיקת מיכאליס מנטן?
תשובה: ד’ (k-2). קבוע הקצב k-2 מתאר הפיכה של תוצר (P) ואנזים ( E) חזרה לקומפלקס אנזים סובסטרט (ES). מכיוון שבקנטיקת מיכאליס מנטן נמדדת המהירות בתחילת הריאקציה, לא מצטבר מספיק תוצר בכדי שהריאקציה תפנה אחורה, ולכן ניתן להזניח שלב זה.
שלילת מסיחים:
א. הפיכת קומפלקס ES לתוצר ואנזים חופשי הינו שלב נחוץ בריאקציה האנזימטית, ולכן לא ניתן להזניח שלב זה.
ב. בריאקציה אנזימטית, סובסטרט לא הופך בבת אחת לתוצר אלא עובר דרך שלב ביניים של קומפלקס ES. בעוד אפשר להזניח הפיכה של תוצר לקומפלקס ES, לא ניתן להזניח את הפיכה של קומפלקס ES לאנזים חופשי וסובסטרט.
ג. קבוע הקצב k-1 מתאר את השלב בו קומפקלס ES מתפרק חזרה לאנזים + סובסטרט. יצירת קומפלקס ES זהו שלב מהיר, ולכן קומפלקס ES מצטבר מהר גם בתחילת הריאקציה, מה שמאפשר לריאקציה לחזור אחורה לE+S. לכן, לא ניתן להזניח שלב זה.
נושא: ביוכימיה. תת נושא: חלבונים מבנה ותפקיד. תת תת נושא: קינטיקה אנזימטית.
להרחבה: Lehninger מהדורה שמינית, פרק 6, עמודים 776-780.
