שאלון מערכת: שיעורי בית ביוכימיה 1
ביוכימיה 1 שאלה 1
מי מהתמיסות הבאות הינה החומצית ביותר?
במה השאלה עוסקת: חומצות ובסיסים
pH – מדד לריכוז יוני ההידרוניום (או הפרוטונים) בסביבה, חישוב לפי הנוסחא:
[+pH = -log[H.
pOH – מדד לריכוז יוני ההידרוקסיל בסביבה, חישוב לפי הנוסחא:
[-pOH = -log[OH.
תמיד : pH + pOH = 14 (לזכור זאת !).
למעשה, pH משמש מדד לחומציות ו- pOH לבסיסיות של תמיסה נתונה כאשר לפי ההגדרה המקובלת תמיסה שבה ה- pH גדול מ- 7 היא בסיסית (alkaline) ותמיסה שבה ה- pH נמוך מ- 7 היא חומצית (acidic), וככל שה- pH נמוך יותר כך נחשבת ליותר חומצית (ריכוז פרוטונים גבוה יותר) והפוך.
אם נתבונן בשאלה, עלינו לחפש את התמיסה שבה ה- pH הוא הנמוך ביותר. במסיח ב’ ה- pH שווה ל- 1 ולכן זוהי התשובה הנכונה. במסיח ג’ ה- pH שווה ל- 9 (תמיסה בסיסית).
הרחבה – קבוע פירוק המים (Kw), אשר מתאר את פירוק המים לפרוטונים ויוני הידרוקסיל, מחושב לפי הנוסחא: [-Kw = [H+][OH. בתמיסת מים טהורים ריכוז יוני ההידרוניום שווה לריכוז יוני ההידרוקסיל (7-^10) כך ש- Kw = 10^-14 ומהנוסחא לחישוב pH נקבל שה- pH של מים טהורים הוא 7 (בפועל 7.4 בעולם הביולוגי….). מדידת ה- pH בפלזמה משמשת הרבה פעמים להערכה קלינית. זאת משום שגופנו תלוי ב- pH, למשל הפעילות הקטליטית של האנזימים בגוף שלנו מושפעת רבות מה- pH. בחולי סכרת מוצאים בפלזמה ערך pH נמוך מ- 7.4, מצב המכונה acidosis ובמחלות אחרות מוצאים pH גבוה מ- 7.4, מצב המכונה alkalosis.
חשוב לשים לב שהסקאלה של ה- pH היא לוגריתמית. למשל, עלייה של ה- pH ביחידה אחת מקבילה לירידה פי 10 בריכוז הפרוטונים בסביבה (ובהתאם לעלייה פי 10 בריכוז יוני ההידרוקסיל בסביבה).
להרחבה – Lehninger, מהדורה שישית, עמוד 61-60 (The pH Scale).
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מים ו-PH.
להרחבה- Lehninger, מהדורה שמינית, פרק 2, עמודים 296-299 (The pH Scale).
ביוכימיה 1 שאלה 2
מי מהבאים מתפקד כבופר היעיל ביותר בתא?
במה השאלה עוסקת: בופרים
קודם כל, לפני שניגש לענות על השאלה נדבר על מה זה בכלל בופר. בופר זו תמיסה שמתנגדת לשינויים ב- pH. תאים ואורגניזמים שומרים על pH קבוע וספציפי של 7 (בפועל 7.4 בעולם הביולוגי), נובע בעיקר מכך שמרבית האנזימים הפועלים בתאי גופנו בעלי פעילות אופטימלית סביב pH זה. הבקרה על pH זה היא ע”י בופר ביולוגי – תערובת של חומצה חלשה והבסיס המצומד לה (או בסיס חלש והחומצה המצומדת לו) ביחס מאוד מסוים (שלא ניכנס אליו) שמתנגדים לשינויים ב- pH של המערכת בהוספת חומצה (+H) או בסיס (-OH). קיבולת הבופר מקסימלית כאשר ה- pH שווה ל- pK וטווח הבופר (buffering region) הוא יחידה אחת פלוס/מינוס מערך זה.
אם נחזור לשאלה, שואלים אותנו מי יתפקד בצורה היעילה ביותר כבופר בתא. מאחר ואנו יודעים שה- pH בתא הוא באזור 7 נחפש למי יש את ערך ה- pK שהכי קרוב לערך זה. פוספט מתאים לשמש בופר בטווח pH של 5.8-7.8 וקיבולת הבופר המקסימאלית שלו מאוד קרובה ל- pH הפיזיולוגי ולכן הוא התשובה הנכונה (סעיף ב’).
הערת מחבר – בנקודה בה ה- pH שווה ל- pK ריכוז מקבל הפרוטון שווה לריכוז מוסר הפרוטון, במילים אחרות ריכוז החומצה שווה לריכוז הבסיס וקיבולת הבופר מקסימאלית – כלומר יכולת ההתנגדות שלו לשינויים ב- pH של המערכת היא הגבוהה ביותר.
להרחבה – Lehninger, מהדורה שישית, עמודים 63-64.
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מים ו-PH, בופרים.
להרחבה – Lehninger, מהדורה שמינית, פרק 2, עמודים 312-315.
ביוכימיה 1 שאלה 3
חומצות אמינו מוגדרות אמפוליטיות (ampholytes) היות והן יכולות לתפקד:
במה השאלה עוסקת: חומצות אמינו
תשובה א. המונח אמפוליטי מתייחס ליכולת של חומר לתפקד הן כחומצה והן כבסיס וחומצות אמינו מתנהגות באופן זה. ב- pH סטנדרטי, הקצה האמיני של החומצה טעון חיובי והוא עדיין לא שחרר פרוטון, ואילו הקצה הקרבוקסילי טעון שלילית כיון שהוא כבר שחרר את הפרטון שלו. כלומר, בערך pH מסוים המולקולה משמשת הן כחומצה והן כבסיס והדבר נובע מהבדלים בין הקבוצות הפונקציונאליות השונות המרכיבות את חומצת האמינו.
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו.
להרחבה – Lehninger, מהדורה שמינית, פרק 3, עמוד 372 (אמפוליט), 367-369 (תכונות של חומצות אמיניות).
ביוכימיה 1 שאלה 4
טיטרציה של חומצת האמינו ואלין באמצעות בסיס חזק, כדוגמת NaOH , חושפת שני pK’s . מהי ריאקציית הטיטרציה המתרחשת ב- pK2=9.62) ?pK2).
במה השאלה עוסקת: טיטרציות של ח.אמינו.
תשובה ג. ואלין משתייכת למשפחת חומצות האמינו הלא פולאריות, המשמעות היא ששייר ה-R שלה אינו יכול ליצור קשרי מימן ולכן אינו יכול להתיינן (למסור או לאבד את הפרוטון). משום כך אצל ואלין מדברים רק על שני ערכי pK. ככלל, בכל טיטרציה של חומצת אמינו הקבוצה הראשונה שתעבור יינון היא קבוצת הקרבוקסיל, וזאת מאחר ויש לה את ה- pK הנמוך ביותר. רק ב- pK הבא שייר ה- R או קבוצת האמין יעברו יינון. כלל נוסף הוא שכל חומצה אמינית מתחילה לעבור טיטרציה כאשר קבוצת הקרבוקסיל וקבוצת האמין עוד לא איבדו את הפרוטון (COOH ו- +NH3 בהתאמה) וזאת משום שמתחילים ב- pH של 0 ויש עודף פרוטונים בסביבה.
הרחבה – טיטרציה נועדה בשביל לקבוע את הריכוז של חומצה מסוימת בתמיסה מסוימת. לוקחים את התמיסה ומוסיפים ריכוזים עולים של בסיס חזק (לרוב NaOH) עד שהחומצה הופכת לניטראלית. בעזרת כמות הבסיס החזק שהוסף ניתן לחשב את ריכוז החומצה בתמיסה המקורית. עקומת טיטרציה מתארת זאת בגרף pH כפונקציה של ריכוז הבסיס שהוסף. חומצות אמינו יכולות לשמש הן כבסיס (תקבל פרוטון) והן כחומצה (תמסור פרוטון) כתלות ב- pH בו הן נמצאות. לכל חומצה אמינית יש לפחות 2 מצבי שיווי משקל/ 2 ערכי pK (של קבוצת האמין ושל קבוצת הקרבוקסיל). בחומצות אמינו להן שייר R שיכול להתיינן יש קבוע שיווי משקל שלישי. כאשר נמצאים ב- pH אשר שווה לערך ה- pK של אחת הקבוצות הדבר מעיד לנו על כך שישנו שיווי משקל בין מצב מיונן למצב לא מיונן. למשל, כאשר ה- pH שווה ל- pK של קבוצת הקרבוקסיל 50% מקבוצות הקרבוקסיל של אותה חומצת אמינו בתמיסה כבר מסרו את הפרוטון (-COO) ו- 50% עוד לא מסרו אותו (COOH).
הערת מחבר – Lehninger, מהדורה שישית, עמוד 78, מומלץ להציץ בטבלה שבה ערכי ה- pK של 20 חומצות האמינו. אין צורך לשנן את המספרים אך כן הכרחי לדעת לאלו מחומצות האמינו ישנו שייר R שיכול להתיינן.
שלילת מסיחים :
א. מסיח זה היה נכון אילו היו שואלים אותנו על ריאקציית הטיטרציה שהייתה מתרחשת ב- pK הראשון. במצב זה, קבוצת הקרבוקסיל הייתה מתחילה לאבד את הפרוטון שלה עד מצב ש- 50% כבר מסרו אותו.
ב. ריאקציית הטיטרציה מוגדרת על ידי הוספה הדרגתית של בסיס חזק שמסוגל לסתור את החומצה, כלומר לקחת ממנה פרוטון. NH2 אינו נחשב כלל כבסיס חזק. קבוצת ההידרוקסיל היא זו שמקבלת את הפרוטון והופכת למולקולת מים בתמיסה.
ד. קבוצת האמינו נמצאת בצורת +NH3 עד אשר מגיעים לערך ה- pK שלה ובו 50% מקבוצות האמינו שמשתייכות למולקולות שבתמיסה כבר איבדו את הפרוטון לצורת NH2.
הערת מחבר – דרך נוספת לשלול את הסעיף היא להגיד לעצמנו שכאשר ה- pH שווה ל- 7 (פיזיולוגי) ואלין היא ניטראלית והמצב מכונה צויטריון (קבוצת האמינו טעונה חיובית וקבוצת הקרבוקסיל טעונה שלילית וסך המטען 0), רק כאשר עולים בערך ה- pH של התמיסה קבוצת האמינו הופכת לניטראלית ומאבדת את הפרוטון שלה.
להרחבה – Lehninger , מהדורה שישית, עמודים 64-67 (הקדמה והסבר על טיטרציה באופן כללי), עמודים 82-85 (טיטרציה של חומצות אמינו)
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו, מים ו-PH.
להרחבה – Lehninger , מהדורה שמינית, פרק 2- עמודים 305-309 (הקדמה והסבר על טיטרציה באופן כללי), פרק 3- עמודים 372-375 (טיטרציה של חומצות אמינו).
ביוכימיה 1 שאלה 5
מה נכון לגבי Nitric Oxide) NO) ו-Carbon Monoxide) CO)?
במה השאלה עוסקת: קוטביות של חומרים
תשובה ג. הגזים CO ו-NO מורכבים כל אחד משני אטומים שונים. מולקולה בעלת 2 אטומים שונים הינה פולארית מכיוון שיש הפרש בערך האלקטרושליליות (הנטייה של אטום למשוך אליו אלקטרונים בקשר קוולנטי). גזים אלו מאוד קטנים, ולכן למרות היותם פולארים הם יכולים לחצות ממברנה.
שלילת מסיחים:
א. הגזים הללו מורכבים כל אחד משני אטומים שונים, ולכן יש הפרש אלקטרושליליות במולקולות מה שהופך אותם לפולאריות.
ב. למרות שחומרים אלו פולארים הם יכולים לחצות ממברנה מכיוון שהם מספיק קטנים ובעלי פולאריות יחסית קטנה.
ד. גזים אלו פולארים ויכולים לחצות ממברנה כפי שהוסבר במסיחים הנ”ל.
להרחבה – Lehninger, מהדורה שישית, עמוד 51 (Nonpolar Gases Are Poorly Soluble in Water)
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מים ו-PH.
להרחבה – Lehninger, מהדורה שמינית, פרק 2, עמודים 265-266 (Nonpolar Gases Are Poorly Soluble in Water).
ביוכימיה 1 שאלה 6
לאיזו חומצה אמינית שייכת עקומת הטיטרציה הבאה?
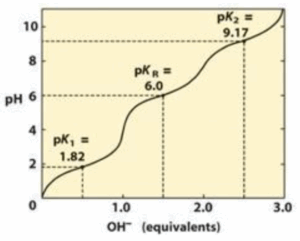
במה השאלה עוסקת: טיטרציה של חומצות אמינו
תשובה ד. חומצות אמינו הן אמפוליטיות (Ampholytes): יכולות לתפקד הן כחומצה והן כבסיס הודות ל- 2 קבוצות שיכולות למסור או לקבל פרוטון בסביבה מימית – קבוצת האמינו וקבוצת הקרבוקסיל. עבור כל חומצה אמינית יש לפחות 2 מצבי יינון (2 ערכי pKa): של הקבוצה הקרבוקסילית ושל הקבוצה האמינית ועבור חומצות אמינו שלהן שייר R שיכול לעבור יינון ישנם שלושה מצבים. מומלץ לזכור שה- pKa של הקבוצה האמינית הוא באזור 9 ושל הקבוצה הקרבוקסילית הוא באזור 2. כאשר ה- pH שווה ל- PKa של יש שו”מ בין מצב מיונן למצב לא מיונן, כלומר 50% מסה”כ הקבוצות בתמיסה איבדו את הפרוטון ו- 50% עוד לא איבדו אותו. סביב כל ערך pK ישנו טווח בופר של יחידה אחת פלוס/ מינוס סביב ערך זה. בעקומת הטיטרציה הנתונה בשאלה רואים כי ישנם שלושה ערכי pK (ובהתאמה, שלושה טווחי בופר) ומכאן שמדובר בחומצת אמינו לה יש שייר R טעון שיכול לעבור יינון (פסילת מסיח ג’). עוד רואים כי ה- pK של שייר ה- R הוא 6 ומכאן שמדובר בחומצת האמינו היסטדין (סעיף ד’). טווח הבופר של שייר ה- R של היסטדין הוא ב- pH הפיזיולוגי ומכאן שהיסטדין מתאימה לשמש בופר בתא.
הערת מחבר – מומלץ לזכור את ה- pK של שיירי ה- R של חומצות האמינו שיכול לעבור יינון (טבלה 3-1 בעמ’ 77 מהדורה 6/ עמ’ 365 מהדורה 8). יש סה”כ 7 כאלו: ח”א חיוביות, ח”א שליליות, טירוזין וציסטאין.
להרחבה – Lehninger,מהדורהשישית, עמודים 81-85.
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו.
להרחבה – Lehninger, מהדורה שמינית, פרק 3, עמודים 372-377.
ביוכימיה 1 שאלה 7
איזו צורה של ליפיד אמפיפאטי יוצר דו שכבה?
במה השאלה עוסקת: קוטביות של חומרים
תשובה א’. ליפיד אמפיפאטי בעל צורה של גליל, כגון פוספוליפיד לו ראש פולארי ושתי חומצות שומן, מתארגן למבנה של דו שכבה. דו שכבה זהו למעשה מבנה הממברנה, אשר בנויה משתי שכבות של פוספוליפידים. הצד הפולארי של כל שכבה פונה למים (חוץ התא – תווך בין תאי, תוך התא – ציטוזול) והצד ההידרופובי נמצא בתווך של הממברנה ומהווה מחסום לחומרים טעונים (אך לא רק).
שלילת מסיחים:
ב. אין ליפידים אמפיפאטים בעלי צורה משולשת.
ג. ליפיד אמפיפאטי בעל צורה של חרוט, כגון חומצת שומן, מתארגן למבנה של מיצלה. במבנה זה, הראש ההידרופלי (בחומצת שומן זוהי הקבוצה הקרבוקסילית) יפנה למים וכל הזנבות ההידרופובים (השייר הפחממני של חומצת השומן) יפנו לחלק הפנימי של המיצלה.
ד. אין ליפידים אמפיפאטים בעלי צורה כדורית.
להרחבה – Lehninger, מהדורה שישית, עמוד 52 (Figure 2-7)
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מים ו-PH.
להרחבה – Lehninger, מהדורה שמינית, פרק 2- עמוד 269 (Figure 2-7).
ביוכימיה 1 שאלה 8
מה מתרחש כאשר ליפידים אמפיאפטים באים במגע עם מים?
במה השאלה עוסקת: מסיסות
תשובה ג’. המסה של חומר אמפיפאטי (או הידרופובי) במים מחולק לשני שלבים. בשלב הראשון מולקולות מים מתארגנות מסביב לחלק ההידרופובי בצורה מאוד מסודרת (ומכאן ששלב זה מוביל לירידה באנטרופיה), ולמעשה יוצרים מעין כלוב שמטרתו לבודד את החומר ההידרופובי (המים יוצרים קשרי מימן מאוד מסודרים בינם לבין עצמם אך לא יוצרים קשרים עם החלק ההידרופבי). בשלב השני, החלקים ההידרופובים נדחים מהמים ומתקבצים יחד, כך שחלק ממולקולות המים שיצרו את הכלוב משתחררות חופשיות לתמיסה ומעלות את אי הסדר. השלב השני מוביל לעלייה באנטרופיה, וסה”כ מדובר בתהליך מועדף אנרגטית.
שלילת מסיחים:
א. מכיוון שמדובר בליפיד אמפיאפאטי לא נוצר אגרגרט ששוקע, אלא הליפידים יתארגנו למבנה של מיצלה (כשמדובר בליפיד בעל מבנה של חרוט) אשר מסיס במים.
ב. האפקט ההידרופובי אינו נוצר מתגובה של ליפידים יחד אלא מדחייה של ליפידים ע”י מים.
ד. החלק ההידרופובי של הליפיד אינו יכול להגיב עם המים מכיוון שאינו פולארי.
להרחבה – Lehninger, מהדורה שישית, עמוד 52 (Figure 2-7)
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מים ו-PH.
להרחבה – Lehninger, מהדורה שמינית, פרק 2, עמוד 269 (Figure 2-7).
ביוכימיה 1 שאלה 9
השחרור של פחמן דו חמצני כתוצאה מהחמצון המלא של פירובט (pyruvate) עשוי ליצור בעיות בתאים.
איזו מולקולה יכולה להיווצר בקלות מפחמן דו חמצני, ולשמש כתורמת של פחמן ובנוסף כבופר ביולוגי?
במה השאלה עוסקת: מים כמגיב
תשובה ד. פחמן דו חמצני יכול להגיב עם מים ע”י האנזים קרבוניק אנהידראז (Carbonic Anhydrase) ולהפוך לחומצה פחמתית (H2CO3). לאחר שחומצה פחמתית מוסרת פרוטון היא הופכת לביקרבונט (-HCO3). ביקרבונט הינו בופר ביולוגי, ובנוסף משמש כתורם פחמנים בריאקציות ביולוגיות שונות. כמוסר פחמן, ביקרבונט תחילה עובר שפעול ע”י קישור לקבוצת פוספט (תוך ניצול ATP), ולאחר מכן נקשר לקואנזים ביוטין בצורה של CO2. ביוטין לאחר מכן מעביר את קבוצת הפחמן לסובסטרט.
שלילת מסיחים:
א. אצטט זו יחידה של שני פחמנים היכולה להיווצר מפירובט תוך הוצאה של פחמן דו חמצני. ה-CO2 יוצא בתהליך זה ואינו בונה את האצטט.
ב. גליצראלדהיד-3-פוספט מורכב משלושה פחמנים ונוצר מביקוע של פרוקטוז 1,6-ביספוספט.
ג. גליצין זו חומצה אמינית הבנויה משני פחמנים ונבנית מהחומצה אמינית סרין.
להרחבה – Lehninger, מהדורה שישית, עמוד 69 (Water as a Reactant), עמוד 571 (Figure 14-19)
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מים ו-PH.
להרחבה – Lehninger, מהדורה שמינית, פרק 2, עמודים 324-325 (בופר ביקרבונט), פרק 14- 1952 (Figure 14-8).
ביוכימיה 1 שאלה 10
לפניך המבנה של תיופנטאל (Thiopental). לקבוצת התיול (-SH) ערך pKa של 7.5. היכן תתרחש הספיגה המרבית של חומר זה בגוף?
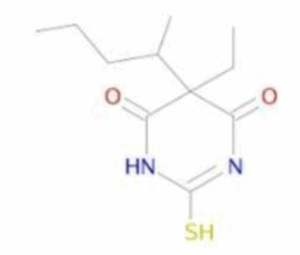
במה השאלה עוסקת: מסיסות
תשובה ב’. על מנת שחומר יספג בגוף עליו לחצות ממברנה, ובכדי שהחומר יוכל לחצות ממברנה עליו להיות ללא מטען (חומרים טעונים לא יכולים לחצות ממברנה). לתיופנטאל יש קבוצה תיול בעלת ערך pKa של 7.5, ולכן כל עוד ערך ה-pH נמוך מערך ה-pKa המולקולה תהיה נטרלית, ומעל ערך pKa המולקולה תהיה טעונה שלילית. ערך ה-pH בקיבה הינו חומצי (בערך 1.5), ולכן רוב מולקולות התיופנטאל יהיו לא טעונות כאשר יגיע לקיבה. מסיבה זו, תיופנטאל יוכל לחצות את הממברנה של תאי הקיבה ולהיספג לזרם הדם.
שלילת מסיחים:
א. בחלל הפה ה-pH ניטרלי (אזור 7). ערך ה-pKa של תיופנטאל הינו 7.5. מכיוון שערך ה-pH קרוב לערך ה-pKa הספיגה בחלל הפה תהיה מינימלית ביחס לקיבה.
ג. פוספטידילכולין הוא מרכיב עיקרי של ממברנות ומסונתז ע”י תאים הומנים.
ד. במעי ה-pH הוא בערך 6. ערך ה-pKa של תיופנטאל הינו 7.5. אמנם גם במעי תיופנטאל תהיה לא טעונה, אך בקיבה ה-% הלא מיונן של תיופנטאל יותר גבוה ולכן בקיבה תתרחש ספיגה מרבית יותר מאשר במעי.
להרחבה – Lehninger, מהדורה שישית, עמוד 72 (pH and Drug Absorption)
תיוג שאלה:
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מים ו-PH.
להרחבה – Lehninger, מהדורה שמינית, פרק 2, עמוד 341(pH and Drug Absorption).
ביוכימיה 1 שאלה 11
ידוע כי בעזרת מספר ריאקציות, תראונין הופך לאיזולאצין. מה יקרה במצב של היזון חוזר ( Feedback inhibition ) ?
תשובה: א
הסבר: היזון חוזר- feedback inhibtion, מטרתו לבקר תהליכים המתרחשים בתא, ובעיקר על רמת המגיבים והתוצרים. כפי שניתן לראות בדוגמה, תראונין- ח”א, מובילה בסדרה של ריאקציות להיווצרות של ח”א אחרת- איזולאוצין. איזולאוצין היא ח”א אמינית מסועפת, שנדרשת בתהליכים רבים בגוף, ביניהם בניית מסת שריר. ישנו שלב בו איזולאוצין נמצא בכמות גבוהה מדי, ותראונין בכמות לא מספקת, שעלול לסכן את התא מאשל להועיל. במצב כזה, התא מגיב במנגנון היזון חוזר, או במילים אחרות, מעכב את יצירת התוצר. ישנם הרבה דרכים לעיכוב תהליך ( זרחון\שימוש במעכב תחרותי\דגרדציה של אנזים). לכן, במצב של היזון חוזר נצפה לעלייה בכמות המגיב- תראונין, וירידה בכמות התוצר- איזולאוצין
שלילת מסיחים:
ב- באם נעכב את האנזים המשתתף בריאקציה שקשורה בהמרת תראונין לאיזולאוצין, נגרום לעלייה בתראונין, ווכן כמות האיזולאוצין תירד
ג- אמנם כמות האיזולאוצין תירד, אך כמות התראונין תעלה
ד- לא ייתכן שעיכוב של מגיב או תוצר יובילו לעלייה בשניהם בעבור ריאקציה מסוימת.
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מבוא לביוכימיה יסודות כימיים ופיזיקליים.
להרחבה – Lehninger, מהדורה שמינית, פרק 1, עמוד עמודים 184-185 (Metabolism is regulated to achieve balance and economy).
ביוכימיה 1 שאלה 12
מה לא נכון לגבי שיווי המשקל בריאקציה כימית?
תשובה:ד.
הסבר: במערכת סגורה, הנטייה של ריאקציה כימית להגיע לשיווי המשקל. קבוע שיווי המשקל, מתאר את הנטייה של הריאקציה להגיע לסיומה, כאשר בסוף הריאקציה המערכת נתונה לשיווי משקל. קבוע שיווי המשקל תלוי בריכוז התוצרים, ובמולים שלהם כשהמערכת הגיעה לשיווי המשקל.
להרחבה:לנינג’ר מהדורה 6 עמ’ 22-27.
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מבוא לביוכימיה יסודות כימיים ופיזיקליים.
להרחבה:לנינג’ר מהדורה שמינית, פרק 1, עמודים 169-171.
ביוכימיה 1 שאלה 13
מה מהבאים נכון לגבי המקרומולקולות הקיימות בטבע?
תשובה: ב’
הסבר: לנינג’ר ( עמ’ 27) מרקומולקולות בנויות מיחידות מונומריות שונות ( למשל חלבון טטרמרי), כאמור אם נחשוב על כך. מבחינה תרמודינמית ( אנתרופיה בעיקר), המקרומולקולות פחות יציבות, הם נוטים לריאקציות שונות, יכולים להימצא במצבי מעבר שונים שלא תמיד מועדפים עבור הסביבה והמולקולה. לעומת זאת, מבחינה קינטית, הן מאוד יציבות, כלומר המהירות בה ייקח להם לבצע ריאקציה עם מגיב אחר היא מאוד נמוכה ( עד כדי שנים). חשוב לזכור : לשם כך קיימים אנזימים, שמשפיעים על הקינטיקה, אך לא על התרמודיניקה. שמגבירים את הקצב של הריאקציה הכימית מבלי להתכלות בתהליך.
שלילת מסיחים:
א-כפי שנאמר, המקרומולקולות אינן יציבות תרמודינמית בשל הריאקטיביות הגבוהה שלהם ליצור קשרים רבים עם מולקולות אחרות
ג- יציבות קינטית ולא תרמודינמית
ד- לא נכון, מקרומולקולות יציבות קינטית כפי שנכתב לעיל, אך לא יציבות תרמודינמית
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מבוא לביוכימיה יסודות כימיים ופיזיקליים.
להרחבה:לנינג’ר מהדורה שמינית, פרק 1, עמוד 178 (Enzymes promote sequences of chemical reactions).
ביוכימיה 1 שאלה 14
מה משמעות הצימוד האנרגטי?
תשובה:ב.
הסבר:בתרמודינמיקה קיימים שני סוגי ריאקציות: ריאקציה אקסרגונית, ריאקציה שפולטת אנרגיהלסביבה, כלומר ריאקציה שבה האנרגיה החופשית שלילית והיא ריאקציה ספונטנית.
ריאקציהאנדרגונית, ריאקציה שמקבלת אנרגיה מהסביבה, כלומר ריאקציה שבה האנרגיה החופשיתחיובית והיא ריאקציה לא ספונטנית.
על מנתשריאקציה אנדרגונית תתרחש, ניתן לצמד אותה לראיקציה אקסרגונית שתתרום לה אתהאנרגיה שלה. דוגמא לכך (שימו לב, נשאלתם למשמעות ולא לדוגמא) היא הצימוד שלהאנרגיה מפירוק ATPלגלוקוז, על מנת לסייע בפירוק הגלוקוז (על כך נלמד בשיעור 4).
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מבוא לביוכימיה יסודות כימיים ופיזיקליים.
להרחבה:לנינג’ר מהדורה שמינית, פרק 1, עמוד 168 (Figure 1-26a).
ביוכימיה 1 שאלה 15
לצורך זיהוי חומצה אמינית בוצעה טיטרציה והתקבלה העקומה המצורפת. איזו חומצה אמינית עשויה להתאים לתוצאות?
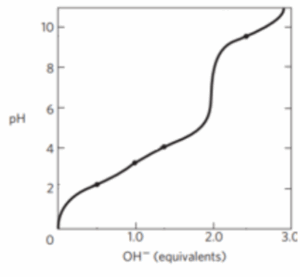
תשובה: ד’ (גלוטמאט). בעקומה המצורפת ניתן להבחין בשלושה אזורים המתנגדים לשינוי ב-pH מה שכבר מרמז על חומצה אמינית טעונה. ניתן לראות כי שניים מאזורי הבופר נמצאים בטווח החומצי, ואזור בופר אחד נמצא בטווח הבסיסי. עבור כל חומצה אמינית יש לפחות שני אזורי בופר: קצה קרבוקסילי (בטווח החומצי), וקצה אמיני (בטווח הבסיסי). אזור הבופר השלישי מתייחס לשייר (pKr) ומרמז לנו על הקבוצה לה משתייכת החומצה האמינית. במקרה זה, אזור הבופר השלישי נמצא בטווח החומצי ולכן העקומה שייכת לאחת מהחומצות האמיניות הטעונות שלילית – גלוטמאט או אספרטט. בשאלה זו, העקומה שייכת לגלוטמאט.
שלילת מסיחים:
א. איזולאוצין זוהי חומצה אמינית לא פולארית. חומצות אמיניות המשתייכות למשפחה זו חסרות מטען. לכן, בטיטרציה יתקבלו שני אזורי בופר. בעקומה הנ”ל ניתן להבחין בשלושה אזורי בופר.
ב. אספרגין זוהי חומצה אמינית פולארית. חומצות אמיניות פולאריות המשתייכות למשפחה זו חסרות מטען (למעט ציסטאין המתייננת ב-pH=8.2). לכן, בטיטרציה של אספרגין יתקבלו שני אזורי בופר. בעקומה הנ”ל ניתן להבחין בשלושה אזורי בופר.
ג. ליזין זוהי חומצה אמינית בסיסית (טעונה חיובית) ולכן תתן עקומה עם 3 אזורי בופר. עם זאת, השייר של ליזין מוסר פרוטון רק בpH בסיסי ולכן נצפה ששני אזורי בופר יהיו באזור הבסיסי (הקצה האמיני והשייר), ואזור בופר אחד בטווח החומצי (קצה קרבוקסילי). מסיח זה נפסל.
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו.
להרחבה:לנינג’ר מהדורה שמינית, פרק 3, עמוד 377 (Figure 3-12).
ביוכימיה 1 שאלה 16
מי מהתמיסות הבאות בעלת ה-pH הגבוה ביותר?
תשובה: א’ (pKa=12.39). כאשר נתונות תרכובות שונות באותו ריכוז, ניתן להשוות בין ערכי ה-pKa/pKb בכדי לדעת מי מהתמיסות תהיה הבסיסית ביותר (על מנת לדעת את ה-pH המדויק יש לבצע חישוב מעט מורכב יותר).
בכדי שיהיה נוח לענות על השאלה, נעביר את כל הערכים לסקלת pKa. נזכור כי הקשר בין pKa ל-pKb הוא: pKa + pKb = Pw = 14
לאחר שנעבור לסקלת pKa נקבל:
א. pKa=12.39
ב. pKa = -1.67
ג. pKa=4.65
ד. pKa= 12.16
בסקלת pKa ככל שהערך גבוה יותר כך מדובר בתרכובת יותר בסיסית ולכן pKa=12.39 ייתן את התמיסה הבסיסית יותר.
*ניתן לפתור את השאלה גם עפ”י סקלת pKb.
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מים ו-PH.
להרחבה:לנינג’ר מהדורה שמינית, פרק 2, עמודים 304-312.
ביוכימיה 1 שאלה 17
מה נכון לגבי הגזים H2S ואמוניה?
תשובה: ד’ (אמוניה הידרופילית ו-H2S ליפופובי). אמוניה ו-H2S הם שתי מולקולות פולאריות, שם מקביל לפולארי זה הידרופילי או ליפופובי. מולקולות הידרופיליות מתמוססות בקלות במים.
שלילת מסיחים:
א. אמוניה ו-H2S שניהם פולאריים ועל כן מתמוססים בקלות במים.
ב. לחנקן אלקטרושליליות גבוהה (בין אטומי NOF) ויכול ליצור קשרי מימן חזקים, גופרית, שלמרות שאיננה משלושת האטומים בעלי האלקטרושליליות הגבוהה ביותר, יכולה ליצור קשרי מימן גם כן אך מדובר בקשרי מימן יחסית חלשים.
ג. אמוניה ו-H2S שניהם פולאריים ועל כן מתמוססים בקלות במים.
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מים ו-PH.
להרחבה:לנינג’ר מהדורה שמינית, פרק 2, עמוד 266 (Table 2-2).
ביוכימיה 1 שאלה 18
המקדם הדיאלקטרי (ε) של בנזן הוא 4.6. מה ניתן להסיק מכך?
תשובה: א’ (בנזן בעל קוטביות מאוד נמוכה). מקדם דיאלקטרי מעיד על היכולת של הממס למסך אינטרקציה בין מומסים שונים בתמיסה. ככל שהערך גבוה יותר, כך המיסוך גבוה יותר. מיסוך גבוה נוצר בעקבות קשרים שיוצר הממס עם המומסים השונים – במים למשל, הקבוע הדיאלקטרי הוא 78.5. הפולאריות (קוטביות) הגבוהה של המים היא זו שמאפשרת ליצור את הקשרים החזקים עם המומסים. הקבוע הדיאלקטרי המאוד נמוך של בנזן מעיד על כך שהוא אינו פולארי, ולכן כאשר בנזן יהווה ממס של חלבונים הוא יוביל לדנטורציה שלהם.
שלילת מסיחים:
ב. מקדם דיאלקטרי גבוה מעיד על יכולת מיסוך גבוהה. המקדם הדיאלקטרי של בנזן הוא 4.6, שזהו ערך מאוד נמוך בהשוואה למים (77.8), ולכן בנזן לא ממסך אינטרקציה בין מטענים ביעילות גבוהה.
ג. בנזן מורכב מטבעת פחממנית ומימנים, מכיוון שהמימנים אינם קשורי לאטומי NOF בבנזן, לבנזן אין יכולת ליצור קשרי מימן עם מומסים.
ד. ככל שהמרחק בין המומסים קטן כך האינטרקציה ביניהם גבוהה יותר.
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: מים ו-PH.
להרחבה: לנינג’ר מהדורה שמינית, פרק 2, עמודים 264-265.
ביוכימיה 1 שאלה 19
בעקומת טיטרציה נצפתה התנגדות לשינוי ב-pH באזור pH=6. מי החומצה האמינית לה נעשתה טיטרציה?
תשובה: ד’ (אף מסיח אינו נכון). התנגדות ל-pH מתרחשת באזורי בופר, בו ערך ה-pH הוא פלוס/מינוס 1 מערך ה-pKa של אותה קבוצה פונקציונלית. עבור כל חומצה אמינית יש לפחות שני אזורי בופר – אזור בטווח החומצי של הקבוצה הקרבוקסילית, ואזור בטווח הבסיסי של הקבוצה האמינית. חלק מהחומצות האמיניות מכילות שייר שיכול למסור פרוטון, ולהם ערך pKr שיכול גם הוא להתנגד לשינויים ב-pH. ה-pKr של היסטידין הוא 6, ולכן באזור זה היסטידין תתנגד לשינויים ב-pH. מכאן, מסיחים א-ג שגויים.
שלילת מסיחים:
א.W זו האות המייצגת את טריפטופן. לטריפטופן אין pKr.
ב. Q זו האות המייצגת את גלוטמין. לגלוטמין אין pKr.
ג. Y זו האות המייצגת את טירוזין. לטירוזין pKr בעל ערך של 10~
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו, מים ו-PH.
להרחבה: לנינג’ר מהדורה שמינית, פרק 3, עמוד 377 (Figure 3-12), מהדורה שישית עמוד 111 (Table 3-1)- לחילופין מהדורה 8 עמ 365 אך הטבלה חתוכה, פרק 2- 313 (הסבר על בופר).
ביוכימיה 1 שאלה 20
נבדק מבנה של חלבון אשר הודגר בתמיסה של CCl4. מהצפוי להתקבל באנליזה?
תשובה:ב’ (חומצות אמיניות ליפופיביות יפנו לאזור הפנימי של החלבון). כאשרמים הם הממס, השיירים הפולארים/טעוניםשל ח”א לרוב יפנו לצד החיצוני של החלבון (שזהו הצד שבא במגע עם המים – פולארימתמוסס בפולארי) ושיירים הידרופוביםיפנו לחלק הפנימי של החלבון (הידרופובי מתמוסס בהידרופובי). כאשר משתמשים בממסאורגני שהוא ממש אפולרי(כמו CCl4)מקבלים סביבה הידרופובית. הסביבה ההידרופובית תוביל לדנטורציהשל החלבון ולהתקפלות שלו מחדש כך ששיירים הידרופוביםיפנו לצד החיצוני (יבואו במגע עם הממס ההידרופובי), והשיירים ההידרופיליםיהיו בסביבה הפנימית של החלבון. חומצות אמיניות ליפופוביותהינן חומצות אמיניות הידרופיליות ולכן כאשר משתמשים בממס אורגני הן יפנו לצדהפנימי של החלבון.
שלילת מסיחים:
א.CCl4לא יכול ליצור קשרי מימן ולכן השיירים בחלבון לא יצרו קשרי מימן עם הממס.
ג.בדנטורציהנאבד המבנה השלישוני וחלק מהמבנים השניוניים. חלק מהמבנים השניוניים יכולים להשמרבדנטורציהולכן מסיח זה נפסל.
ד.כאשר הסביבה היא הידרופילית הח”אההידרופיליות יפנו לאזור החיצוני של החלבון, אך כאשר הסביבה היא הידרופובית הח”אההידרופיליות יפנו לאזור הפנימי של החלבון
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו.
להרחבה: לנינג’ר מהדורה שמינית, פרק 3, עמודים 415-421 (The structure of proteins).
ביוכימיה 1 שאלה 21
איזה פפטיד יבלע אור בצורה המרבית ביותר באורך גל של 280nm?
תשובה: ג’ (RNWDWK). בליעת אורך גל של 280nm נעשית ע”י חומצות אמיניות ארומטיות בפפטיד – טריפטופן (W), טירוזין (Y), פנילאלנין (F). טריפטופן בולעת קרינה בעוצמה גבוהה, לאחר מכן טירוזין ופנילאלנין בולעת קרינה בצורה מאוד חלשה.
שלילת מסיחים:
א. הפפטיד מכיל פנילאלנין ולכן יבלע אור באורך גל של 280nm. פנילאלנין בקושי בולע קרינה לעומת טריפטופן וטירוזין, ולכן מסיח זה נפסל.
ב. הפפטיד אינו מכיל חומצות אמיניות ארומטיות ועל כן לא יבלע אורך גל של 280nm.
ד. הפפטיד מכיל טירוזין ולכן יבלע אורך באורגל גל של 280nm. טירוזין בולע קרינה פחות טוב מטריפטופן ולכן מסיח זה נפסל.
נושא: ביוכימיה. תת נושא: מבוא כימי ופיזיקלי לביוכימיה. תת תת נושא: חומצות אמינו.
להרחבה: לנינג’ר מהדורה שמינית, פרק 3, עמודים 267-268.
